Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теплоемкость при постоянном давленииСодержание книги
Поиск на нашем сайте
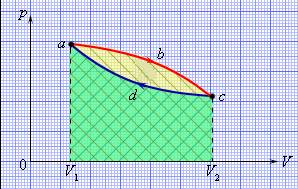
+А. больше теплоемкости при постоянном объеме Б. равна теплоемкости при постоянном объеме В. меньше теплоемкости при постоянном объеме Г. среди предложенных вариантов нет верного ответа, т.к. такое сравнение невозможно. Теплоемкость газообразного вещества А. зависит только от изменения его внутренней энергии +Б. зависит от характера термодинамического процесса В. зависит только от работы, совершенной телом. Г. не зависит от изменения его внутренней энергии и характера процесса 6.) Для процесса при постоянном давлении первый закон термодинамики дает: А. Qp = CрΔT - υΔр +Б. Qp = ΔU - p(V2 – V1) В. Qp = CvΔT + VΔp В. Qp = ΔU +V(p2 – p1) Из первого закона термодинамики для 1 моля газа следует +А. Qp = ΔU – pΔV Б. QV = ΔU + pΔV В. Qp = ΔU-VΔp Г. QV = ΔU 8.) В какой из предложенных формул Сp имеет размерность [Дж/кг·К]: +А. Ср=Cv+R Б. Ср=(Cvμ+R)/μ В. Ср=(Cvμ-R)/μ Г. Ср=Cv-R Второй закон термодинамики 1.) Второй закон термодинамики определяет условия, при которых… А. теплота сохраняется неизменной +Б. теплота может как угодно долго преобразовываться в работу В. теплота расходуется на изменение внутренней энергии и совершение работы. Г. не возможен процесс исчезновения энергии. 2.) Укажите выражение, характеризующее принцип существования энтропии (dQr – количество теплоты, обусловленное необратимостью): +А. dSоб = dQ/T Б. dSнеобр = dQ/T В. dSнеобр = (dQ+ dQr)/T Г. dSобр = dQ+ dQr/T 3.) Укажите выражение, характеризующее принцип возрастания энтропии (dQr – количество теплоты, обусловленное необратимостью): А. dSоб = dQ/T Б. dSнеобр = dQ/T +В. dSнеобр = (dQ+ dQr)/T Г. dSобр = dQ+ dQr/T 4.) Количество теплоты, обусловленное необратимостью… А. всегда отрицательно +Б. всегда положительно В. равно нулю Г. среди предложенных вариантов нет верного ответа. 5.) Реальные неравновесные процессы… А. могут протекать только в сторону уменьшения энтропии Б. могут протекать, только когда энтропия равна нулю +В. могут протекать только в сторону увеличения энтропии Г. могут протекать как в сторону уменьшения энтропии, так и в сторону увеличения энтропии 6.) Непрерывное преобразование теплоты в работу… А. можно осуществить в любом термодинамическом процессе +Б. можно осуществить только в круговом термодинамическом процессе В. осуществить невозможно Г. среди предложенных вариантов нет верного ответа. 7.)При передаче тепла от менее нагретого тела более нагретому телу… А. изменение энтропии больше нуля Б. процесс идет самопроизвольно +В. чтобы осуществить процесс необходимо затратить энергию Г. энтропия меньше нуля, необходимо отнять энергию Круговой термодинамический процесс. 1.) Круговой процесс на диаграмме (p, V).
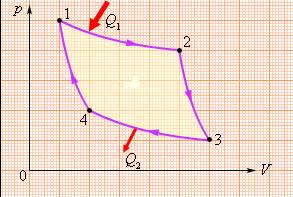
Полная работа L в круговом процессе равна площади фигуры А.) abcd Б.) V1 adcV2 В.) V1 abcV2 + Г.) среди предложенных вариантов нет верного ответа. Из первого закона термодинамики для кругового процесса следует А. dq = dU – d l Б. Q = dU + d l +В. Q = L Г. Q = ∆U 3.) На диаграмме (p, V) изображен цикл Карно. Какому процессу соответствует линия 1-2:
+А.) изотермическое расширение Б.) изотермическое сжатие В.) адиабатическое расширение Г.) адиабатическое сжатие 4.) На диаграмме (p, V) изображен цикл Карно. Какой линии соответствует процесс адиабатического сжатия:
А.) 1-2 Б.) 2-3 В.) 3-4 +Г.) 4-1 Термодинамические процессы 1.) Адиабатный процесс характеризуется условием: А. dU = 0 Б. d l = 0 +В. dq = 0 Г. d l = dU 2.) Для какого процесса располагаемая работа равна нулю (lp = 0): А. изотермический +Б. изобарный В. политропный Г. адиабатный 3.) Удельное количество теплоты, участвующей в изотермическом процессе,равно: А. ∆U + Б. RT ln p1/p2 В. ∆Н Г. 0 4.) Удельное количество теплоты, участвующей в изобарном процессе, равно: А. ∆U Б. RT ln p1/p2 +В. ∆Н Г. 0 5.) Удельное количество теплоты, участвующей в изохорном процессе, равно: +А. ∆U Б. RT ln p1/p2 В. ∆Н Г. 0 6.) Изменение энтропии в изохорном процессе равно: +А. Сv ln T2/T1 Б. Ср ln T2/T1 В. Сv ln p1/p2 Г. Ср ln p2/p1 7.) Изменение энтропии в изобарном процессе равно: А. Сv ln T2/T1 +Б. Ср ln T2/T1 В. Сv ln p1/p2 Г. Ср ln p2/p1 8.) Изменение энтропии в изотермическом процессе равно: А. RT ln v2/v1 Б. R ln p2/p1 +В. R ln p1/p2 Г. R ln v1/v2 9.) Изменение энтропии в адиабатном процессе равно: А. Сn ln T2/T1 Б. Сv ln T2/T1 + В. 0 Г. Ср ln T2/T1
|
||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 405; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.248.150 (0.009 с.) |