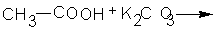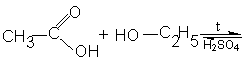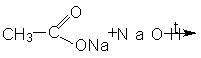Содержание книги
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Алгоритм составления названий карбоновых кислот
Карбоновые кислоты - органические вещества, молекулы которых содержат одну или несколько карбоксильных групп. Карбоксильная группа По числу карбоксильных групп карбоновые кислоты делятся на одноосновные, двухосновные и т.д. Общая формула одноосновных карбоновых кислот R—COOH. Пример двухосновной кислоты - щавелевая кислота HOOC—COOH. По типу радикала карбоновые кислоты делятся на предельные (например, уксусная кислота CH3COOH), непредельные [например, акриловая кислота CH2=CH—COOH, олеиновая CH3—(CH2)7—CH=CH—(CH2)7—COOH] и ароматические (например, бензойная C6H5—COOH). Изомеры и гомологи Одноосновные предельные карбоновые кислоты R—COOH являются изомерами сложных эфиров г HCOOH CH3COOH HCOOCH3 CH3CH2COOH HCOOCH2CH3 CH3COOCH3 CH3(CH2)2COOH
HCOOCH2CH2CH3 CH3COOCH2CH3 CH3CH2COOCH3 и з о м е р ы 1. Найдите главную углеродную цепь - это самая длинная цепь атомов углерода, включающая атом углерода карбоксильной группы. 2. Пронумеруйте атомы углерода в главной цепи, начиная с атома углерода карбоксильной группы. 3. Назовите соединение по алгоритму для углеводородов. 4. В конце названия допишите суффикс "-ов", окончание "-ая" и слово "кислота". В молекулах карбоновых кислот p-электроны атомов кислорода гидроксильной группы взаимодействуют с электронами
Последнее способствует образованию прочных водородных связей между молекулами карбоновых кислот. Физические свойства предельных одноосновных карбоновых кислот в значительной степени обусловлены наличием между молекулами прочных водородных связей (более прочных, чем между молекулами спиртов). Поэтому температуры кипения и растворимость в воде у кислот больше, чем у соответствующих спиртов.
Химические свойства кислот Упрочнение 1. Горение: CH3COOH + 2O2
2. Кислотные свойства.
HCOOH
HCOOH
CH3COOH
CH2ClCOOH
CHCl2COOH
CCl3COOH уксусная кислота монохлоруксусная кислота дихлоруксусная кислота трихлоруксусная кислота
Карбоновые кислоты проявляют все свойства, присущие слабым кислотам:
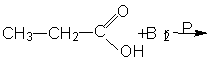
Mg + 2CH3COOH
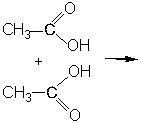
3. Этерификация (реакция карбоновых кислот со спиртами, приводящая к образованию сложного эфира):
+ H2O муравьиная кислота этанол этиловый эфир 4.
+
+ 3H2O глицерин карбоновые кислоты триглицерид 5. Жиры представляют собой смеси триглицеридов. Предельные жирные кислоты (пальмитиновая C15H31COOH, стеариновая C17H35COOH) образуют твердые жиры животного происхождения, а непредельные (олеиновая C17H33COOH, линолевая C17H31COOH и др.) - жидкие жиры (масла) растительного происхождения.
6. Замещение в углеводородном радикале: CH3—CH2—COOH + Cl2
CH3—CHCl—COOH + HCl пропионовая кислота
7.
Особенность муравьиной кислоты HCOOH состоит в том, что это вещество - двуфункциональное соединение, оно одновременно является и карбоновой кислотой, и альдегидом: 8. 9. 10. HCOOH + Ag2O(аммиачный раствор) Получение карбоновых кислот 1. Окисление альдегидов. Лабораторные окислители: Ag2O, Cu(OH)2, KMnO4, K2Cr2O7 и др.
2. Окисление спиртов: RCH2OH + O2
3. Окисление углеводородов: 2C4H10 + 5O2
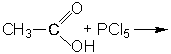
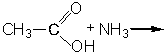
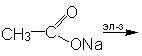
4. Из солей (лабораторный способ): CH3COONaкр. + H2SO4 конц. Задание. Приведите структурные формулы соединений: -пропандиовая кислота -гидроксипропановая кислота - пропионилхлорид. - бутилат кальция - ангидрид пропионовой кислоты - формамид -фениловый эфир пропионовой кислоты - n-хлорбензойная кислота 2.Допишите уравнения реакций: 1. 2. 3. 4. 5. 6. 7. 8. 3.Какие вещества получатся при гидролизе следующих соединений: 1. этилформиат 4. уксусный ангидрид 2. изоамилацетат 5. фтористый формил 3. пропионитрил 6. бутириламид 4.Какие свойства отличают муравьиную кислоту от других карбоновых кислот? Приведите уравнения реакций.
|
||||||
|
Последнее изменение этой страницы: 2024-06-17; просмотров: 5; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.151.44 (0.006 с.) |
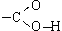 (сокращенно —COOH) - функциональная группа карбоновых кислот - состоит из карбонильной группы и связанной с ней гидроксильной группы.
(сокращенно —COOH) - функциональная группа карбоновых кислот - состоит из карбонильной группы и связанной с ней гидроксильной группы.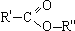 (сокращенно R'—COOR'') с тем же числом атомов углерода. Общая формула и тех, и других CnH2nO2.
(сокращенно R'—COOR'') с тем же числом атомов углерода. Общая формула и тех, и других CnH2nO2.
 -связи карбонильной группы, в результате чего возрастает полярность связи O—H, упрочняется
-связи карбонильной группы, в результате чего возрастает полярность связи O—H, упрочняется  +) на атоме углерода и увеличивается частичный заряд (
+) на атоме углерода и увеличивается частичный заряд ( 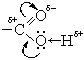
 2CO2 + 2H2O
2CO2 + 2H2O HCOO- + H+ (точнее HCOOH + H2O
HCOO- + H+ (точнее HCOOH + H2O 
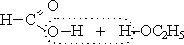
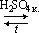
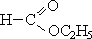
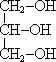
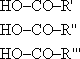
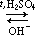
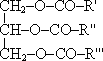
 -хлорпропионовая кислота
-хлорпропионовая кислота
 CO2 + H2O + 2Ag
CO2 + H2O + 2Ag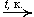 2RCOOH
2RCOOH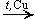 RCOOH + H2O
RCOOH + H2O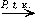 4CH3COOH + 2H2O
4CH3COOH + 2H2O