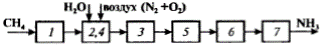Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физическая культура. (ФК 1(11) 2 (9))Стр 1 из 9Следующая ⇒
Академическая группа: ОФ-118-263-3-1 / ОФ-218-263-4-1 Физическая культура. (ФК 1(11) 2 (9)) Учебная дисциплина: «Химия». Преподаватель: Передриенко Георгий Анатольевич e - mail преподавателя: peredrienkoga@cspu.ru Задания для самостоятельного изучения учебной дисциплины: «Химия» до 28 декабря 2021 г. (4 часа) После 28 декабря 2021 года на проверку работы не принимаются. Раздел 3. Химия в жизни общества. Тема 3.1. Применение химических веществ. Выполнить задания №№ 1 – 4. ЗАДАНИЕ 1. (практическая часть – самостоятельная работа студентов) – 2 часа 1. Задания для самостоятельного решения, используя теоретический материал. Ответить на вопросы: 1. Что такое технология? 2. Что такое сырье, промежуточный продукт, побочный продукт и отходы химического производства? 3. Каковы основные требования к химическому производству? 4. Что такое системный подход? 5. Что такое химико-технологическая система? 6. Что такое химическая безопасность? Приведите примеры. 7. Каковы научные основы химического производства? 8. Какова роль воды для химического производства? 9. Каковы основные стадии химического производства? Опишите их характеристики. 10. Что называется химически опасным объектом? 11. Какие процессы химической технологии являются потенциально опасными? 12. Какие отходы существуют на химических предприятиях? ЗАДАНИЕ 2. Изучить теоретический материал.
Лекция № 1 - 2 часа. План. 1. Химия и производство. Химическая промышленность и химические технологии. Сырье для химической промышленности. 2.Вода в химической промышленности. Энергия для химического производства. 3. Научные принципы химического производства. Защита окружающей среды и охрана труда при химическом производстве. 4. Основные стадии химического производства. 5. Сравнение производства аммиака и метанола. 1. «Технология – учение о выгодных (т. е. поглощающих наименее труда людского и энергии природы) приемах переработки природных ресурсов в продукты, потребные (необходимые, или полезные, или удобные) для применения в жизни людей», – так начинается статья «Технология», написанная Д. И. Менделеевым в Энциклопедическом словаре под редакцией Ф. А. Брокгауза и И. А. Ефрона. Происхождение слова «технология» (гр. technos – искусство, ремесло и
«logos» – учение, наука) вполне отвечает его содержанию: учение об умении, искусстве перерабатывать исходные вещества в полезные продукты. Химическая технология – естественная, прикладная наука о способах и процессах производства продуктов (предметов потребления и средств производства), осуществляемых с участием химических превращений технически, экономически и социально целесообразным путем. Как естественная наука химическая технология изучает материальные явления и объекты. Как прикладная наука – изучает производство. По своей сути химическая технология представляет собой переработку, в процессе которой превалируют химические и физико-химические явления, что приводит к коренному изменению состава, свойств и строения веществ. В химии соединения, участвующие в химическом превращении, назы- ваются веществами. В химической технологии компоненты реагирующей системы получают технологическое наименование. Сырьем называют исходный материал, поступающий на переработку и обладающий стоимостью. Образующиеся в ходе реакций вещества называют продуктами. Сырье обычно состоит из полезного компонента и примесей: сырье = полезный компонент + примеси. Продукт, ради которого организовано производство, называется целевым, и соответственно реакция, в которой он образуется, называется целевой. Все остальные продукты получают наименование побочных. Полупродукт (полуфабрикат) – продукт, прошедший частичную промышленную обработку. Вспомогательные материалы – это вещества, которые не принимают участия в химическом превращении, но используются при разделении реакционных смесей или очистке продукта или исходного сырья от примесей (растворители, адсорбенты, экстрагенты и пр.). В группу вспомогательных материалов включают также катализаторы, ингибиторы, инициаторы. Отходы – примеси и остатки сырья, отработанные вспомогательные материалы, побочные продукты, которые частично или полностью утратили свои качества и более не соответствуют стандартам. Понятие технологический режим означает оптимальные условия проведения процесса.
Химическую технологию классифицируют на основе различных признаков – по характеру используемых технологических процессов, происхождению и характеру сырья, характеру и потребительским свойствам продуктов. По отраслям, как они исторически сформировались в хозяйственной жизни, химическую технологию разделяют на два класса: А. Неорганическая химическая технология: 1) основной неорганический синтез – производство кислот, щелочей, солей и минеральных продуктов; 2) тонкий неорганический синтез – производство неорганических препаратов, реактивов, редких элементов, материалов электроники, лекар- ственных веществ и др.; 3) ядерно-химическая технология; 4) металлургия – производство черных и цветных металлов; 5) силикатные производства – производства вяжущих материалов, ке- рамических изделий, стекла. Б. Органическая химическая технология: 1) переработка нефти и газа – первичная переработка (первичное разделение, очистка, облагораживание) газообразных, жидких и твердых природных углеводородов (ископаемого топливного сырья); 2) нефтехимический синтез – производство органических продуктов и полупродуктов на основе переработки газообразных жидких и твердых углеводородов, а также на основе оксидов углерода и водорода; 3) основной органический синтез – производство органических продуктов на основе, главным образом, углеводородного сырья; 4) биотехнология – производство кормовых дрожжей, аминокислот, ферментов, антибиотиков и др. на основе биологических процессов; 5) тонкий органический синтез – производство органических препаратов, реактивов, лекарственных веществ, средств защиты растений и др.; 6) высокомолекулярная технология – получение высокомолекулярных соединений (синтетический каучук, пластмассы, химические волокна, пленкообразующие вещества); 7) технологии переработки растительного и животного сырья. Приведенная классификация основана на том, что в указанных процессах переработки сырья в продукты происходит коренное изменение состава, свойств и строения участвующих веществ, т. е. химическое превращение или физико-химический процесс. Объектом исследования химической технологии является химическое производство. Основное назначение химического производства – получение продукта, при этом химическое производство является многофункциональным. Общие требования к химическому производству: · получение в процессе производства необходимого продукта; · экологическая безопасность; · безопасность и надежность эксплуатации; · максимальное использование сырья и энергии; · максимальная производительность труда. Химическое производство – совокупность машин, аппаратов и других устройств, связанных между собой материальными трубопроводами и паропроводами, линиями электрическими, транспортными и связи (для информации и управления). Все они взаимосвязаны и функционируют вместе, обеспечивая получение продукции и выполняя другие функции производства. Такой объект называется системой. Система – совокупность элементов и связей между ними, функционирующая как единое целое. Системный подход ( гр. susthma – сочетание) является наиболее современным методом исследования. Основная задача в методологии системного подхода заключается в определении элементного состава и такой структуры системы, которые обеспечат полную совместимость элементов внутри системы и совместимость последней с внешней средой, а также достижение высоких результатов функционирования системы.
В химическом производстве элементы – это машины, аппараты и другие устройства; связи – это материальные трубопроводы, паропроводы и прочие, которые соединяют машины, аппараты, устройства. В элементах происходит превращение потоков (изменение их состояния – разделение, смешение, сжатие, нагрев, химические превращения и т. д.). По связям потоки (материальные, тепловые, энергетические) передаются из одного элемента в другой. Это позволяет представить химическое производство как химико-технологическую систему. Для изучения состава и структуры систем используют метод декомпозиции (расчленение целого на части); для изучения свойств системы используют метод стратификации. В настоящее время при описании систем используют их стратифицированное (послойное) представление. Название «стратификация» происходит от латинского stratum – настил и facere – делать. Появление метода связано с невозможностью получения детального описания системы из-за великого множества свойств самой системы и ее элементов, а также неоднозначного их поведения при изменении условий функционирования. К числу основных уровней стратификации можно отнести морфологический (изучение структуры системы), функциональный (изучение состояния системы как совокупности свойств, позволяющее прогнозировать ее поведение), процессуальный (изучение протекающих в системе процессов) и информационный (как знание информационных характеристик системы, связанных с ее управлением). Системный подход включает три уровня (страты) изучения системы в целом: - собственный уровень, т. е. изучение общего поведения системы, ее интегративных характеристик, исключая вопросы структуры; - высший уровень, на котором изучаемая система рассматривается в ее взаимодействии с другими системами (окружающей средой), т. е. исследуется влияние внешних связей на характеристики системы; - низший уровень, когда исследуются все элементы и внутренние связи системы, эффективность функционирования элементов, выявляются их недостатки (диагностика), определяется степень влияния низшего уровня структуры на интегративные свойства системы и пр.
Под химической безопасностью понимается совокупность определенных свойств объектов окружающей среды и создаваемых регламентируемых условий, при которых, с учетом экономических и социальных факторов и научно обоснованных допустимых дозовых нагрузок химических вредных веществ, удерживается на разумно низком, минимально возможном, уровне риск возникновения аварии на химическом опасном объекте, а также риск прямого или косвенного воздействия этих веществ на окружающую среду и человека, и исключаются отдаленные последствия воздействия химических вредных веществ для настоящих и последующих поколений. Учитывая специфические особенности химической опасности, проявляющиеся в аварийном и/или систематическом загрязнении окружающей природной среды В. А. Легасов сформулировал принципы химической безопасности. Один из которых гласит: система обеспечения химической безопасности должна опираться на анализ и управление химическими рисками, исходя из базового положения о приемлемых уровнях риска взамен существовавших ранее подходов к обеспечению полной (абсолютной) безопасности. В основу выбора подходов к оценке риска положена концепция многосредового воздействия с учетом взаимного влияния сред. Экологические факторы 1. С целью наиболее полного использования исходного сырья и ресурсов в химическом производстве применяется также принцип циркуляции вещества. За время прохождения через реакционную установку, то есть за один технологический цикл, исходные вещества не всегда успевают полностью израсходоваться, поэтому непрореагировавшие вещества снова возвращают в аппарат. Например, при синтетическом получении аммиака в контактном аппарате реагирует только 30–37 % смеси азота и водорода; поэтому оставшиеся газы отделяют от образовавшегося жидкого аммиака и с помощью специальных насосов опять направляются в контактный аппарат. Кроме того, наиболее важный и дорогой ресурс - вода, также должен использоваться в производственном процессе многократно. С одной стороны, вода используется в технологических процессах для охлаждения продуктов реакции и нагревания исходных веществ, то есть выполняет функции теплоносителя, обеспечивая выполнение принципа теплообмена. Такие операции повторяются многократно. С другой стороны, вода используется непосредственно в химических реакциях, как растворитель или реагент. Если концентрация загрязняющих веществ в сточных водах не очень высокая, то после очистки реакционная вода также может быть возвращена в технологический цикл. Циркуляционный принцип использования химических веществ и воды – также один из основных принципов организации современного химического производства. 2. Для обеспечения экологической безопасности на химическом производстве используется целый комплекс мероприятий, обеспечивающих защиту окружающей среды. К таким мероприятиям, в первую очередь, относится использование современного очистного оборудования, организация замкнутых сырьевых и ресурсных циклов производства, использование безопасного сырья и др. Все перечисленные факторы и общие принципы организации современных химических производств основываются на закономерностях химических процессов и обеспечивают экологическую безопасность производства, энерго- и ресурсосбережение.
Таким образом, к химико-технологическим и экологическим факторам, обеспечивающим выполнение научной организации современных химических производств относятся: · увеличение поверхности реагирующих веществ, · теплообмен (утилизация тепла), · массообмен (противоток), · циркуляция реагирующих веществ, · изменение скорости и направления химических реакций (использование катализатора, оптимальных температур, давления и концентрации), · исключение ручных операций и автоматизация производства; · очистка выбросов и сбросов и утилизация отходов производства
Химическое производство многофункционально – это производство продуктов, экономное использование сырья, материалов и энергии, экологическая безвредность, социальное совершенство. Основные операции или стадии любого химического производства – подготовка сырья, химическое превращение, выделение продуктов, обезвреживание и утилизация отходов тепло и энергообеспечения, водоподготовка, система управления. Первой группой операций является подготовка сырья: измельчение, растворение, нагревание, обогащение, концентрирование, очистка и т.п. Вторая группа операций. После подготовки сырья проводится собственно химическое превращение, в результате чего образуется смесь, химический состав которой отличается от состава исходного сырья. Наличие химического превращения сырья является признаком химического производства. Химическое превращение или химико-технологический процесс разделяется на ряд следующих взаимосвязанных элементарных стадий: а) Физический транспорт веществ; б) Химические реакции могут быть простые и сложные, последовательные и параллельные, сопровождаемые тепло- и массообменными явлениями; в) Отвод может совершаться также как и подвод реагирующих компонентов диффузией, конвекцией и переходом вещества из одной фазы в другую. Третья группа превращений – выделение и очистка полезного продукта от примесей. Для этого используют разнообразные массообменные процессы, такие как абсорбция, ректификация, экстракция, фильтрование, центрефицирование. Продукты реакции направляют на склад готовой продукции или на дальнейшую переработку. Не прореагировавшее сырьё вновь используют в процессе, организуя его рецикл. На заключительных этапах проводят также рекуперацию энергии и очистку промышленных выбросов, чтобы извлечь из отходящих газов, сточных вод и твёрдых отходов все ценные компоненты, а такжеликвидировать опасные загрязнения окружающей среды. В системе аппаратов химического производства перерабатываются потоки вещества и энергии, которые называются компонентами химического производства. К ним относятся: сырьё, энергия, продукты, полупродукты, отходы. Химико-технологическая система (ХТС) – искусственная техническая система, предназначенная для выпуска химических продуктов высокого качества с минимальными затратами ресурсов и минимальным воздействием на окружающую среду. На практике ХТС соответствуют производственные объединения, химические заводы, химические комбинаты. Рассмотрим в качестве примера ХТС производство аммиака и метанола. Химико-технологическая система (ХТС)производства аммиака. Химическая схема представлена основными реакциями (химическими уравнениями), которые обеспечивают переработку сырья в продукт. Синтез аммиака из водорода и азота представлен одним химическим уравнением: 3Н2 + N2 = 2NН3. Производство аммиака из природного газа (метана) требует проведения нескольких химических реакций: СН4 + Н2О = СО+ 3Н2 – конверсия метана с водяным паром; СО + Н2О = СО2 + Н2 – конверсия оксида углерода; 3Н2 + N2 = 2NН3 – синтез аммиака. Эти уравнения – химическая схема – показывают генеральный путь превращения сырья в продукт. Но реализация превращения не ограничивается только данными уравнениями – необходимы еще стадии, обеспечивающие химические преобразования или детализирующие их. 1. Очистка природного газа от серосодержащих соединений адсорбцией сероводорода, который мешает дальнейшим превращениям: H 2 S + ZnO = ZnS + Н2О. 2. Конверсия метана с водяным паром. И природный газ СН4, и вода Н2О являются сырьем для получения одного из компонентов для синтеза аммиака – водорода Н2. В этом превращении протекают одновременно две реакции: СН4 + Н2О = СО + 3Н2; СО + Н2О = СО2 + Н2. 3. Конверсия оксида углерода с водяным паром (в предыдущем процессе оксид углерода СО не полностью превращается в СО2 из-за равновесных ограничений): СО + Н2О = СО2 + Н2. После этого процесса достигается максимально возможное извлечение водорода из исходного сырья – метана СН4 и воды Н2О. 4. Получение азота N 2 – второго исходного компонента для синтеза аммиака. В современных схемах его получают «выжиганием» из воздуха кислорода: 3О2 + 2СН4 = 2СО + 4Н2О. Это наиболее простой способ освободить азот воздуха от кислорода, тем более что сжигание части природного газа все равно необходимо для обеспечения теплом всего процесса. Продукты горения – СО и Н2О – участники получения водорода. 5. Абсорбция диоксида углерода – удаление СО2 при получении водорода. Его поглощают раствором моноэтаноламина: СО2 + 2RNH2 + Н2О = (RNН3)2 СО3. 6. Очистка газа от оксида углерода СО. После конверсии небольшое количество СО остается, и он мешает дальнейшим превращениям. Освобождаются от него, превращая в метан: СО + 3Н2 = СН4 + Н2О. 7. Синтез аммиака (после всех стадий получена чистая азотоводородная смесь; примесь СН4, полученная в предыдущей стадии, мала): 3Н2 + N2 = 2NН3. Функциональная схема (рис.1) строится на основе химической и наглядно отражает основные стадии химико-технологического процесса и их взаимосвязи. Каждая из них представлена прямоугольником, линии между ними – связи. Структурную и операторную схемы производства аммиака иллюстрирует рис. 2.
Рис. 1. Функциональная схема производства аммиака
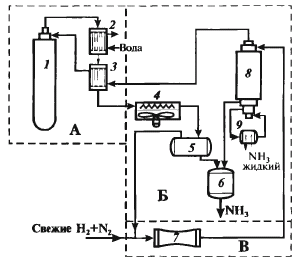
Рис. 2. Структурная (а) и операторная (б) схемы синтеза аммиака На технологической схеме показывают элементы системы, порядок их соединения и последовательность технологических операций. В технологической схеме каждый элемент (агрегат, аппарат, машина) имеетобщепринятое изображение, соответствующее его внешнему виду. Связи изображены обычно линиями со стрелками или даже в виде трубопроводов. Нередко расположение аппаратов соответствует их примерной расстановке в цехе. На технологической схеме кратко могут быть приведены данные о параметрах процесса. Несколько сокращенная технологическая схема синтеза аммиака приведена на рис. 3. Азотоводородная смесь поступает в реактор 1. Нагретая за счет теплоты экзотермической реакции прореагировавшая реакционная смесь охлаждается в трех теплообменниках. В первом из них (2) газ охлаждается водой – частично используется теплота реакции. В теплообменнике 3 подогревается газ, направляемый в реактор. Окончательное охлаждение происходит в воздушном холодильнике 4. Это наиболее простое и безопасное решение. Если охлаждать водой, вода может загрязняться, и необходимо создать сложную замкнутую систему водооборота, работающую на чуть теплой воде. В охлажденном газе конденсируется аммиак (частично), и его отделяют в сепараторе 5. Жидкий аммиак собирается в сборнике 6 как продукт. Охлаждение до температуры окружающей среды недостаточно для полного выделения аммиака, и газ из сепаратора направляется в конденсационную колонну 8. В ней газ охлаждается до – (2 ¸ 3) °С, так что в нем остается 3–5 % аммиака. Охлаждение осуществляют за счет испарения жидкого аммиака в испарителе 9 (подобно аммиачному холодильнику). Испаритель может быть конструктивно совмещен с конденсационной колонной. В ней же аммиакотделяют от газа и направляют в сборник. Холодный газ затем подогревают в теплообменнике 3 и возвращают в колонну синтеза 1. Обеспечивают циркуляцию потока циркуляционным компрессором 7. Перед ним в циркулирующий реакционный газ добавляют свежую азотоводородную смесь. Отметим наглядность отображения конкретного производства, дающую почти осязаемое представление о нем. Технологические схемы входят в проектную и техническую документацию каждого производства.
Рис. 3. Технологическая схема синтеза аммиака: 1 – колонна (реактор) синтеза NH3; 2 – водяной холодильник; 3 – теплообменник; 4 – воздушный холодильник; 5 – сепаратор; 6 – сборник аммиака; 7 – циркуляционный компрессор; 8 – конденсационная колонна; 9 – испаритель. Химико-технологическая система (ХТС)производства метанола. Основным аппаратом в синтезе метанола служит реактор – контактный аппарат, конструкция которого зависит, главным образом, от способа отвода тепла и принципа осуществления процесса синтеза. В современных технологических схемах используются реакторы трех типов: · - трубчатые реакторы, в которых катализатор размещен в трубах, через которые проходит реакционная масса, охлаждаемая водным конденсатом, кипящим в межтрубном пространстве; · - адиабатические реакторы, с несколькими слоями катализатора, в которых съем тепла и регулирование температуры обеспечивается подачей холодного газа между слоями катализатора; · - реакторы, для синтеза в трехфазной системе, в которых тепло отводится за счет циркуляции жидкости через котел-утилизатор или с помощью встроенных в реактор теплообменников. Вследствие большого объема производства и весьма крупных капитальных затрат в производстве метанола сейчас используют все три типа технологических процессов. На рис. 4 представлена технологическая схема производства метанола при низком давлении на цинк-медь-алюминиевом катализаторе из синтез-газа состава: Hg - 67%, СО - 22%, СО2 - 9% -объемных, полученного конверсией метана, производительностью 400 тыс. т в год. Очищенный от сернистых соединений синтез-газ сжимается в компрессоре 1 до давления 5-9 МПа, охлаждается в холодильнике 3 и поступает в сепаратор 4 для отделения сконденсировавшейся воды. Пройдя сепаратор, синтез-газ смешивается с циркуляционным газом, который поджимается до рабочего давления в компрессоре 2. Газовая смесь проходит через адсорбер.
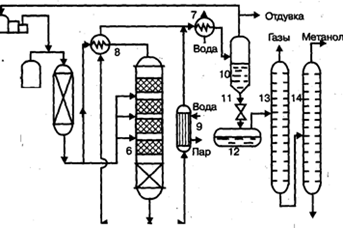
Рис. 4. Технологическая схема производства метанола при низком давлении: 1 - турбокомпрессор, 2 - циркуляционный компрессор, 3, 7 - холодильники, 4 - сепаратор, 5 - адсорбер, 6 - реактор адиабатического действия, 8 - теплообменник, 9 - котел-утилизатор, 10 - сепаратор, 11 - дроссель, 12 - сборник метанола-сырца, 13, 14 - ректификационные колонны Циркуляционый газ 5, где очищается от пентакарбонила железа, образовавшегося при взаимодействии оксида углерода(II) с материалом аппаратуры, и разделяется на два потока. Один поток подогревают в теплообменнике 8 и подают в верхнюю часть реактора 6, а другой поток вводят в реактор между слоями катализатора для отвода тепла и регулирования температуры процесса. Пройдя реактор, реакционная смесь при температуре около 300°С также делится на два потока. Один поток поступает в теплообменник 8, где подогревает исходный синтез-газ, другой поток проходит через котел-утилизатор 9, вырабатывающий пар высокого давления. Затем, потоки объединяются, охлаждаются в холодильнике 7 и поступают в сепаратор высокого давления 10, в котором от циркуляционного газа отделяется спиртовой конденсат. Циркуляционный газ дожимается в компрессоре 2 и возвращается на синтез. Конденсат метанола-сырца дросселируется в дросселе 11 до давления близкого к атмосферному и через сборник 12 поступает на ректификацию. В ректификационной колонне 13 от метанола отгоняются газы и. диметиловый эфир, которые также сжигаются. Полученный товарный метанол с выходом 95% имеет чистоту 99,95%. На рис. 5. приведена технологическая схема производства метанола по трехфазному методу на медь-цинковом катализаторе из синтез-газа, полученного газификацией каменного угля, производительностью 650 тыс. т в год.
Рис. 5. Технологическая схема производства метанола в трехфазной системе: 1 - компрессор, 2 - циркуляционный компрессор, 3,9 - насосы, 4 -реактор кипящего слоя, 5,6 - теплообменники, 7 - холодильник-конденсатор, 8 - сепаратор, 10 - котел-утилизатор. Очищенный от соединений серы синтез-газ сжимается в компрессоре 1 до давления 3-10 МПа, подогревается в теплообменнике 5 продуктами синтеза до 200-280°С, смешивается с циркуляционным газом и поступает в нижнюю часть реактора 4. Образовавшаяся в реакторе парогазовая смесь, содержащая до 15% метанола, выходит из верхней части реактора, охлаждается последовательно в теплообменниках 5 и 6 и через холодильник-конденсатор 7 поступает в сепаратор 8, в котором от жидкости отделяется циркуляционный газ. Жидкая фаза разделяется в сепараторе на два слоя: углеводородный и метанольный. Жидкие углеводороды перекачиваются насосом 9 в реактор, соединяясь с потоком углеводородов, проходящих через котел-утилизатор 10. Таким образом жидкая углеводородная фаза циркулирует через реактор снизу вверх, поддерживая режим кипящего слоя тонкодисперсного катализатора в нем, и одновременно обеспечивая отвод реакционного тепла. Метанол-сырец из сепаратора 8 поступает на ректификацию или используется непосредственно как топливо или добавка к топливу. Разработанный в 70-х годах трехфазный синтез метанола используется в основном, для производства энергетического продукта. В качестве жидкой фазы в нем применяются стабильные в условиях синтеза и не смешивающиеся с метанолом углеводородные фракции нефти, минеральные масла, полиалкилбензолы. К указанным выше преимуществам трехфазного синтеза метанола следует добавить простоту конструкции реактора, возможность замены катализатора в ходе процесса, более эффективное использование теплового эффекта реакции. Вследствие этого установки трехфазного синтеза более экономичны по сравнению с традиционными двухфазными как высокого так и низкого давления. В таблице 1 приведены показатели работы установок трех- и двухфазного процесса одинаковой производительности 1800 т/сут.Таблица 1. Показатели работы установок синтеза метанола
Лекция № 2 – 2 часа План. 1. Химия в сельском хозяйстве. Химизация сельского хозяйства и ее направления. Растения и почва, почвенный поглощающий комплекс. 2. Удобрения и их классификация. Химические средства защиты растений. Отрицательные последствия применения пестицидов и борьба с ними. 3. Химизация животноводства. 4. Химия и экология. Химическое загрязнение окружающей среды. 5. Охрана гидросферы от химического загрязнения. Охрана почвы от химического загрязнения. Охрана атмосферы от химического загрязнения. Охрана флоры и фауны от химического загрязнения. Биотехнология и генная инженерия. 1. Химизация — это одно из направлений научно-технического прогресса, основанное на широком применении химических веществ, процессов и методов в различных отраслях, на-пример в сельском хозяйстве Основные направления химизации сельского хозяйства: 1. Производство минеральных макро- и микроудобрений, а также кормовых фосфатов. 2. Внесение извести, гипса и других веществ для улучшения структуры почв. 3. Применение химических средств защиты растений: гербицидов, зооцидов и инсектицидов и т. д. 4. Использование в растениеводстве стимуляторов роста и плодоношения растений. 5. Разработка способов выращивания экологически чистой сельскохозяйственной продукции. 6. Повышение продуктивности животных с помощью стимуляторов роста, специальных кормовых добавок. 7. Производство и применение полимерных материалов для сельского хозяйства. 8. Производство материалов для средств малой механизации, использующихся в сельском хозяйстве. Около половины всех элементов Периодической системы Д. И. Менделеева применяется в сельском хозяйстве. Влияние многих из них еще неизвестно, и тем из вас, кто станет в будущем специалистами сельского хозяйства, предстоит выяснить это. Основная цель химизации сельского хозяйства — обеспечение роста производства, улучшение качества и продление сроков сохранности сельскохозяйственной продукции, повышение эффективности земледелия и животноводства. Важным направлением химизации сельского хозяйства является использование методов биотехнологии и генной инженерии для решения продовольственных проблем. Регуляторы роста растений Значительным резервом увеличения производства сельскохозяйственной продукции является использование регуляторов роста растения. Это химические вещества, которые ускоряют (или замедляют) рост и сроки цветения, кущения и плодоношения многолетних культур. Ретарданты. Это — вещества, замедляющие рост растений. Они вызывают укорачивание и утолщение стебля, способствуют росту корневой системы и наряду с этим благотворно влияют на плодоношение, часто повышая продуктивность растений. Ретарданты широко применяют в основном на посевах зерновых культур для предотвращения их полегания. Химизация животноводства Химизация животноводства — это комплекс мер, способствующих повышению качества кормов и продуктивности животных. Основные ее направления: • производство химических консервантов и стабилизаторов кормов; • производство кормовых дрожжей и микробиологического белка; • использование мочевины и других кормовых добавок: • применение стимуляторов роста животных. Так, для создания прочной кормовой базы важно не только увеличить заготовку кормов, но и улучшить их качества снизить потери при уборке и хранении. Наиболее прогрессии ная форма заготовки зеленых кормов — химическое консервирование, так как оно обеспечивает хорошую сохранность питательных веществ, подавляет развитие гнилостных и лянокислых бактерий, предотвращает нежелательные ментативные процессы. В качестве консервантов используют пропионовую и бензойную кислоты, дисульфат натрия Na2S2O7 и гидросульфат натрия NaHSO4, концентрат низкомолекулярных кислот. Химические добавки при силосовании трав, кукурузы, подсолнечника и бобово-злаковых смесей повышают качество корма и значительно сокращают потери питательных веществ. Для повышения содержания перевариваемого протеина в рационах скота и птицы используют кормовые дрожжи, белки микробного происхождения, мочевину и другие вещества. Так, применение 1 т кормовых дрожжей в рационе птицы позволяет дополнительно получить по 2 т мяса или 35 тыс. яиц. При составлении пищевых рационов для откорма животных в настоящее время экологически более обоснованно вводить в растительную пищу незаменимые аминокислоты, которые получают ферментативным или полным синтезом. Так, добавкой 0,4% лизина к пшеничной муке можно повысить ее биологическую ценность не менее чем на 50%. В птицеводстве и свиноводстве в качестве источника белка выбрана соевая мука, обогащенная метионином. В нашей стране налажено промышленное производство кормового концентрата лизина — одной из незаменимых аминокислот. Включение в рацион двухмесячных поросят по 40 г этого концентрата (2,5 г в пересчете на чистый лизин) обеспечивает прирост живой массы на 15,6%, а затраты кормов на единицу прироста уменьшаются при этом на 15%. Недостаток протеина в рационе животных можно восполнить, используя мочевину, бикарбонат аммония и другие аммонийные соли органических и минеральных кислот, безопасные в экологическом отношении. Скармливание животным мочевины позволяет экономить от 20 до 35% кормового белка.
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-01-22; просмотров: 21; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.14.70.203 (0.165 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||