
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Рассеяние света. Закон Рэлея. Нефелометрия
Рассеяние света - рассеяние электромагн. волн видимого диапазона при их взаимодействии с веществом. При этом происходит изменение пространств. распределения, частоты, поляризации оптического излучения.
Нефелометрия —метод исследования и анализа вещества по интенсивности светового потока, рассеиваемого взвешенными частицами данного вещества. Большое значение при нефелометрии имеет объём частиц, рассеивающих свет. Продукт реакции должен быть практически нерастворим и быть суспензией. Для удержания твёрдых частиц во взвешенном состоянии применяются различные стабилизаторы (например, желатин),предотвращающие коагуляцию частиц. 39) С труктура энергетических уровней атомов и молекул Энергия атома или молекулы может принимать лишь некоторые определенные (дискретные) значения, которым соответствуют энергетические уровни. Переход атома с одного энерг. уровня на другой совершается скачком (квантовый переход). Он может происходить при взаимодействии атомов и молекул с оптическим излучением. Атомы каждого хим. элемента характеризуются своей системой энерг. уровней. Система энерг. уровней атома отражает особенности движения электронов в данном атоме. Структура энерг. уровней молекулы отражает три типа движений: электронные движения, колебания атомов в молекуле, вращение молекулы. Поэтому система уровней у молекулы сложнее, чем у атома. Наряду с уровнями, отвечающими электронным движениям, существуют колебательные (расстояние между уровнями порядка 0,1эВ) и вращательные уровни (расстояние между уровнями порядка 0,01 эВ и меньше). Теория Бора 1: атом и атомные сис. могут длительно пребывать только в опред. стационарных сост. Находясь в таких сост., атом не излучает и не поглощает энергии. Стационарным сост. соответствуют дискретные значения энергии: E1, Е2 Любое изменение энергии атома или атомной сис. связано со скачкообразным переходом из одного стационарного сост. в другое. Второй постулат: при переходе атома из одного сост. в другое атом испуск. или поглощает фотон частоты v, энергия кот. определяется разностью энергий Еi, Ек атомных состояний: hv = Ei - Ek. Переход из сост. с больш. энергией в сост. с меньш. энергией сопровождается излучением фотона. Обратн. процесс - при поглощении фотона. По теор. Б., электрон в атоме Н вращ. по круговой орбите вокруг ядра. Из всех возможных орбит стационар. сост. соответствуют только тем, для кот. момент импульса (орбитальный механич. момент) = цел. числу h/2π: mvnrn= h/2π, где n=1,2,3 и тд, m — масса электрона, vn— его скорость на n-й орбите, rn — ее радиус. На электрон, вращающ. по круговой орбите в атоме (ионе), действует кулоновская сила притяж. со стороны + заряженного ядра, кот., по 2 з-ну Ньютона, = произвед. массы электрона на центростремит. ускорение: Ze·e/4πεorn2=Ze2/4πεorn2=mvn2/rn где е — заряд электрона, Ze — заряд ядра. Для водорода Z = 1, для водородоподобных ионов Z > 1. rn =ε0h2n2/πZe2m. Находим кинетич. энергию электрона: Eк=mvn2/2=Ze2/8πεorn. Cумма кинетической и потенциальной энергий дает полную энергию электрона: E=Eк+Eп= Ze2 /8πεorn – Ze2/4πεorn=-Ze2/8πεorn. Дискретные знач. энергии Еп= -me4Z2/8εo2h2n2. На основании 2 пост. Б. получил формулу, объясняющую сериальные закономерности спектра атома H и водородоподобных ионов. ν = me4/8ε02h3[1/nk2-1/ni2]. Несмотря на успех теор. Б., не удалось объяснить различия интенсивностей спектральных линий (почему одни переходы между энергетич. уровнями более вероятны, чем другие). Теор. Б. не раскрыла спектральн. закономерностей более сложн. атомных сис. Недостаток теор. Б. - ее внутр. противоречивость. Эта теория объединяла в себе положения принципиально отличных теорий: классич. и квантовой физики. В первой четверти двадцатого века стало ясно, что теория Бора должна быть заменена другой теорией атома, в связи с чем и появилась квантовая механика.
|
|||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 304; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.226.169.94 (0.006 с.) |

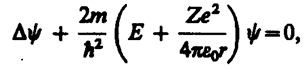 Закон Рэлея: интенсивность I рассеиваемого средой света обратно пропорциональна 4-й степени длины волны l падающего света (I ~ l-4) в случае, когда среда состоит из частиц- диэлектриков, размеры которых много меньше l.
Закон Рэлея: интенсивность I рассеиваемого средой света обратно пропорциональна 4-й степени длины волны l падающего света (I ~ l-4) в случае, когда среда состоит из частиц- диэлектриков, размеры которых много меньше l.


