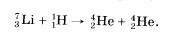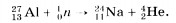Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Альфа-, бета- и гамма-излученияСодержание книги
Поиск на нашем сайте
После открытия радиоактивных элементов началось исследование физической природы их излучения. Кроме Беккереля и супругов Кюри, этим занялся Резерфорд. Классический опыт, позволивший обнаружить сложный состав радиоактивного излучения, состоял в следующем. Препарат радия помещали на дно узкого канала в куске свинца. Против канала находилась фотопластинка. На выходившее из канала излучение действовало сильное магнитное поле, линии индукции которого перпендикулярны лучу (рис. 13.6). Вся установка размещалась в вакууме. В отсутствие магнитного поля на фотопластинке после проявления обнаруживалось одно темное пятно точно напротив канала. В магнитном поле пучок распадался на три пучка. Две составляющие первичного потока отклонялись в противоположные стороны. Это указывало на наличие у этих излучений электрических зарядов противоположных знаков. При этом отрицательный компонент излучения отклонялся магнитным полем гораздо сильнее, чем положительный. Третья составляющая совсем не отклонялась магнитным полем. Положительно заряженный компонент получил название альфа-лучей, отрицательно заряженный — бета-лучей и нейтральный - гамма-лучей (
Эти три вида излучения очень сильно различаются по проникающей способности, т. е. по тому, насколько интенсивно они поглощаются различными веществами. Наименьшей проникающей способностью обладают Гораздо меньше поглощаются при прохождении через вещество Интенсивность поглощения Гамма-лучи. По своим свойствам
На шкале электромагнитных волн Бета-лучи. С самого начала Основная задача экспериментаторов состояла в определении заряда и массы частиц. При исследовании отклонения Альфа-частицы. Труднее было выяснить природу Но заряд Резерфорд поместил на пути
Таким образом, он устаиовил, что у Не довольствуясь достигнутым результатом, Резерфорд затем еще прямыми опытами доказал, что при радиоактивном При радиоактивном распаде возникают 49 вопрос РАДИОАКТИВНЫЕ ПРЕВРАЩЕНИЯ Что же происходит с веществом при радиоактивном излучении? Ответить на этот вопрос в начале XX в. было очень не просто. Уже в самом начале исследований радиоактивности обнаружилось много странного и необычного. Во-первых, удивительным было постоянство, с которым радиоактивные элементы уран, торий и радий испускают излучения. На протяжении суток, месяцев и даже лет интенсивность излучения заметно не изменялась. На нее не оказывали никакого влияния такие обычные воздействия, как нагревание и увеличение давления. Химические реакции, в которые вступали радиоактивные вещества, также не влияли на интенсивность излучения. Во-вторых, очень скоро после открытия радиоактивности выяснилось, что радиоактивность сопровождается выделением энергии. Пьер Кюри поместил ампулу с хлоридом радия в калориметр. В нем поглощались Откуда же берется энергия, на выделение которой не оказывают никакого влияния все известные воздействия? По-видимому, при радиоактивности вещество испытывает какие-то глубокие изменения, совершенно отличные от обычных химических превращений. Было сделано предположение, что превращения претерпевают сами атомы. Сейчас эта мысль не может вызвать особого удивления, так как о ней ребенок может услышать еще раньше, чем научится читать. Но в начале XX в. она казалась фантастической, и нужна была большая смелость, чтобы решиться высказать ее. В то время только что были получены бесспорные доказательства существования атомов. Идея Демокрита об атомистическом строении вещества наконец восторжествовала. И вот почти сразу же вслед за этим неизменность атомов счавится под сомнение. Не будем рассказывать подробно о тех экспериментах, которые привели в конце концов к полной уверенности в том, что при радиоактивном распаде происходит цепочка последовательных превращений атомов. Остановимся только на самых первых опытах, начатых Резерфордом и продолженных им совместно с английским химиком Ф. Содди.
Резерфорд обнаружил, что активность тория, определяемая как число Отсасывая воздух из ампулы, содержащей торий, Резерфорд выделил радиоактивный газ и исследовал его ионизирующую способность. Оказалось, что активность этого газа (в отличие от активности тория, урана и радия) очень быстро убывает со временем. Каждую минуту активность убывает вдвое, и через десять минут она становится практически равной нулю. Содди исследовал химические свойства этого газа и установил, что он не вступает ни в какие реакции, т. е. является инертным газом. Впоследствии этот газ был назван радоном и помещен в периодической системе Д. И. Менделеева под порядковым номером 86. Превращения испытывали и другие радиоактивные элементы: уран, актиний, радий. Общий вывод, который сделали ученые, был точно сформулирован Резерфордом: «Атомы радиоактивного вещества подвержены спонтанным1 видоизменениям. В каждый момент небольшая часть общего числа атомов становится неустойчивой и взрывообразно распадается. В подавляющем большинстве случаев выбрасывается с огромной скоростью осколок атома — Было обнаружено, что в результате атомного превращения образуется вещество совернгенно нового вида, полностью отличное по своим физическим и химическим свойствам от первоначального вещества. Это новое вещество, однако, само также неустойчиво и испытывает превращение с испусканием характерного радиоактивного излучения2. Таким образом, точно установлено, что атомы некоторых элементов подвержены спонтанному распаду, сопровождающемуся излучением энергии в количествах, огромных по сравнению с энергией, освобождающейся при обычных молекулярных видоизменениях».
После того как было открыто атомное ядро, сразу же cталo ясно, что именно оно претерпевает изменения при радиоактивных превращениях. Ведь Итак, радиоактивность представляет собой самопроизвольное превращение одних ядер в другие, сопровождаемое испусканием различных частиц. Правило смещения. Превращения ядер подчиняются так называемому правилу смещения, сформулированному впервые Содди: при
Здесь элемент обозначается, как и в химии, общепринятыми символами: заряд ядра записывается в виде индекса слева внизу у символа, а атомная масса — в виде индекса слева вверху у символа. Например, водород обозначается символом После Согласно правилу смещения при радиоактивном распаде сохраняется суммарный электрический заряд и приближенно сохраняется относительная атомная масса ядер. Возникшие при радиоактивном распаде новые ядра могут быть также радиоактивны и испытывать дальнейшие превращения. При радиоактивном распаде происходит превращение атомных ядер. ЗАКОН РАДИОАКТИВНОГО РАСПАДА. ПЕРИОД ПОЛУРАСПАДА Спад активности, т. е. числа распадов в секунду, в зависимости от времени для одного из радиоактивных препаратов изображен на рисунке 13.8. Период полураспада этого вещества равен 5 сут.
Выведем теперь математическую форму закона радиоактивного распада. Пусть число радиоактивных атомов в начальный момент времени (t= 0) равно N0. Тогда по истечении периода полураспада это число будет равно Спустя еще один такой же интервал времени это число станет равным:
Период полураспада — основная величина, определяющая скорость радиоактивного распада. Чем меньше период полураспада, тем меньше времени «живут» ядра, тем быстрее происходит распад. Для разных веществ период полураспада имеет сильно различающиеся значения. Так, период полураспада урана Чтобы, пользуясь формулой (13.1), определить период полураспада, надо знать число атомов N0 в начальный момент времени и число нераспавшихся атомов N спустя определенный интервал времени t. Сам закон радиоактивного распада довольно прост. Но физический смысл этого закона уяснить себе нелегко. Действительно, согласно этому закону за любой интервал времени распадается одна и та же доля имеющихся атомов (за период полураспада половина атомов). Значит, с течением времени скорость распада нисколько не меняется? Радиоактивные ядра «не стареют». Так, ядра радона, возникающие при распаде радия, претерпевают радиоактивный распад как сразу же после своего образования, так и спустя 10 мин после этого. Распад любого атомного ядра — это, так сказать, не «смерть от старости», а «несчастный случай» в его жизни. Для радиоактивных ядер не существует понятия возраста. Можно определить лишь их среднее время жизни Время существования отдельных ядер может варьироваться от долей секунды до миллиардов лет. Атом урана, например, может спокойно пролежать в земле миллиарды лет и внезапно взорваться, тогда как его соседи благополучно продолжают оставаться в прежнем состоянии. Среднее время жизни Говорить об определенном законе радиоактивного распада для малого числа ядер атомов не имеет смысла. Этот закон справедлив в основном для большого количества частиц. ИЗОТОПЫ Изучение явления радиоактивности привело к важному открытию: была выяснена природа атомных ядер. В результате наблюдения огромного числа радиоактивных превращений постепенно обнаружилось, что существуют вещества, тождественные по своим химическим свойствам, но имеющие совершенно различные радиоактивные свойства (т. е. распадающиеся по-разному). Их никак не удавалось разделить ни одним из известных химических способов. На этом основании Содди в 1911 г. высказал предположение о возможности существования элементов с одинаковыми химическими свойствами, но различающихся, в частности, своей радиоактивностью. Эти элементы нужно помещать в одну и ту же клетку периодической системы Д. И. Менделеева. Содди назвал их изотопами (т. е. занимающими одинаковые места). Предположение Содди получило блестящее подтверждение и глубокое толкование год спустя, когда Дж. Дж. Томсон провел точные измерения массы ионов неона методом отклонения их в электричеелсом и магнитном полях. Он обнаружил, что неон представляет собой смесь двух видов атомов. Большая часть их имеет относительную массу, равную 20. Но существует незначительная часть атомов с относительной атомной массой 22. В результате относительная атомная масса смеси была принята равной 20,2. Атомы, обладающие одними и теми же химическими свойствами, различались массой. Оба вида атомов неона, естественно, занимают одно и то же место в таблице Д. И. Менделеева и, следовательно, являются изотопами. Таким образом, изотопы могут различаться не только своими радиоактивными свойствами, но и массой. Именно поэтому у изотопов заряды атомных ядер одинаковы, а значит, число электронов и оболочках атомов и, следовательно, химические свойства изотопов одинаковы. Но массы ядер различны. Причем ядра могут быть как радиоактивными, так и стабильными. Различие свойств радиоактивных изотопов связано с тем, что их ядра имеют различную массу. В настоящее время установлено существование изотопов у всех химических элементов. Некоторые элементы имеют только нестабильные (т.е. радиоактивные) изотопы. Изотопы есть у самого тяжелого из существующих в природе элементов — урана (относительные атомные массы 238, 235 и др.) и у самого легкого — водорода (относительные атомные массы 1, 2, 3). Особенно интересны изотопы водорода, так как они различаются по массе в 2 и 3 раза. Изотоп с относительной атомной массой 2 называется дейтерием. Он стабилен (т. е. не радиоактивен) и входит в качестве небольпюй примеси (1: 4500) в обычный водород. При соединении дейтерия с кислородом образуется так называемая тяжелая вода. Ее физические свойства заметно отличаются от свойств обычной воды. При нормальном атмосферном давлении она кипит при 101,2 °С и замерзает при 3,8 °С. Изотоп водорода с атомной массой 3 называется тритием. Он Существование изотопов доказывает, что заряд атомного ядра определяет не все свойства атома, а лишь его химические свойства и те физические свойства, которые зависят от периферии электронной оболочки, например размеры атома. Масса же атома и его радиоактивные свойства не определяются порядковым номером в таблице Д. И. Менделеева. Примечательно, что при точном измерении относительных атомных масс изотопов выяснилось, что они близки к целым числам. А вот атомные массы химических элементов иногда сильно отличаются от целых чисел. Так, относительная атомная масса хлора равна 35,5. Это значит, что в естественном состоянии химически чистое вещество представляет собой смесь изотопов в различных пропорциях. Целочисленность (приближенная) относительных атомных масс изотопов очень важна для выяснения строения атомного ядра. Все химические элементы имеют изотопы. Заряды атомных ядер изотопов одинаковы, но массы ядер различны. 50 вопрос СТРОЕНИЕ АТОМНОГО ЯДРА. ЯДЕРНЫЕ СИЛЫ Протонно-нейтронная модель ядра. Согласно протонно-нейтронной модели ядра состоят из элементарных частиц двух видов — протонов и нейтронов. Так как в целом атом электрически нейтрален, а заряд протона равен модулю заряда э-иектрона, то число протонов в ядре равно числу электронов в атомной оболочке. Следовательно, число протонов в ядре равно атомному номеру элемента Z в периодической системе элементов Д. И. Менделеева. Сумму числа протонов Z и числа нейтронов N в ядре называют массовым числом и обозначают буквой А: Изотопы представляют собой ядра с одним и тем же значением но с различными массовыми числами А, т. е. с различными числами нейтронов N. Ядерные силы. Так как ядра весьма устойчивы, то протоны и нейтроны должны удерживаться внутри ядра какими-то силами, причем очень большими. Что это за силы? Сразу можно сказать, что это не гравитационные силы, которые слишком слабые. Устойчивость ядра не может быть объяснена также электромагнитными силами, так как между одноименно заряженными протонами действует электрическое отталкивание. А нейтроны не имеют электрического заряда. Значит, между ядерными частицами — протонами и нейтронами (их называют нуклонами) — действуют особые силы, называемые ядерными силами. Каковы основные свойства ядерных сил? Ядерные силы примерно в 100 раз превышают электрические (кулоновские) силы. Это самые мощные силы из всех сущес;гнующих в природе. Поэтому взаимодействия ядерных частиц часто называют сильными взаимодействиями. Сильные взаимодействия проявляются не только во взаимодействиях нуклонов в ядре. Это особый тип взаимодействий, присущий большинству элементарных частиц наряду с электромагнитными взаимодействиями. Другая важная особенность ядерных сил — их коротко-действие. Электромагнитные силы сравнительно медленно ослабевают с увеличением расстояния. Ядерные силы заметно проявляются лишь на расстояниях, равных размерам ядра (10-12—10-13 см), что показали уже опыты Резерфорда по рассеянию Ядра атомов состоят из протонов и нейтронов. Эти частицы удерживаются в ядре ядерными силами. НЕРГИЯ СВЯЗИ АТОМНЫХ ЯДЕР Важнейшую роль во всей ядерной физике играет понятие энергии связи ядра. Энергия связи позволяет объяснить устойчивость ядер, выяснить, какие процессы ведут к выделению ядерной энергии. Нуклоны в ядре прочно удерживаются ядерными силами. Для того чтобы удалить нуклон из ядра, надо совершить довольно большую работу, т. е. сообщить ядру значительную энергию. Под энергией связи ядра понимают ту энергию, которая необходима для полного расщепления ядра на отдельные нуклоны. На основе закона сохранения энергии можно также утверждать, что энергия связи ядра равна той энергии, которая выделяется при образовании ядра из отдельных частии. Энергия связи атомных ядер очень велика. Но как ее определить? В настоящее время рассчитать энергию связи теоретически, подобно тому как это можно сделать для электронов в атоме, не удается. Выполнить соответствующие расчеты можно, лишь применяя соотношение Эйнштейна между массой и энергией: Е = mс2. (13.3) Точнейшие измерения масс ядер показывают, что масса покоя ядра М21 всегда меньше суммы масс входящих в его состав протонов и нейтронов: Мя< Zmp + Nmn. (13.4) Существует, как говорят, дефект масс: разность масс
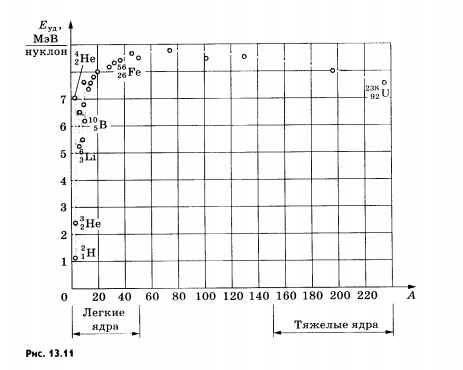
положительна. В частности, для гелия масса ядра на 0,75% меньше суммы масс двух протонов и двух нейтронов. Соответственно для гелия в количестве вещества один моль Уменьшение массы при образовании ядра из нуклонов означает, что при этом уменьшается энергия этой системы нуклонов на значение энергии связи Есв: Есв = Но куда при этом исчезают энергия Есв и масса При образовании ядра из частиц последние за счет действия ядерных сил на малых расстояниях устремляются с огромным ускорением друг к другу. Излучаемые при этом Энергия связи — это энергия, которая выделяется при образовании ядра из отдельных частиц, и соответственно это та энергия, которая необходима для расщепления ядра на составляющие его частицы. О том, как велика энергия связи, можно судить по такому примеру: образование 4 г гелия сопровождается выделением такой же энергии, что и при сгорании 1,5—2 вагонов каменного угля. Важную информацию о свойствах ядер содержит зависимость удельной энергии связи от массового числа А. Удельной энергией связи называют энергию связи, приходящуюся на один нуклон ядра. Ее определяют экспериментально. Из рисунка 13.11 хорошо видно, что, не считая самых легких ядер, удельная энергия связи примерно постоянна и равна 8 МэВ/нуклон. Отметим, что энергия связи электрона и ядра в атоме водорода, равная энергии ионизации, почти в миллион раз меньше этого значения. Кривая на рисунке 13.11 имеет слабо выраженный максимум. Максимальную удельную энергию связи (8,6 МэВ/нуклон) имеют элементы с массовыми числами от 50 до 60, т. е. железо и близкие к нему но порядковому номеру элементы. Ядра этих элементов наиболее устойчивы. У тяжелых ядер удельная энергия связи уменьшается за счет возрастающей с увеличением Z кулоновской энергии отталкивания протонов. Кулоновские силы стремятся разорвать ядро. Частицы в ядре сильно связаны друг с другом. Энергия связи частиц определяется по дефекту масс. 51 вопрос ЯДЕРНЫЕ РЕАКЦИИ Атомные ядра при взаимодействиях испытывают превращения. Эти превращения сопровождаются увеличением или уменьшением кинетической энергии участвующих в них частиц. Ядерными реакциями называют изменения атомных ядер при взаимодействии их с элементарными частицами или друг с другом. С примерами ядерных реакций вы уже ознакомились в § 103. Ядерные реакции происходят, когда частицы вплотную приближаются к ядру и попадают в сферу действия ядерных сил. Одноименно заряженные частицы отталкиваются друг от друга. Поэтому сближение положительно заряженных частиц с ядрами (или ядер друг с другом) возможно, если этим частицам (или ядрам) сообщена достаточно большая кинетическая энергия. Эта энергия сообщается протонам, ядрам дейтерия — дейтронам, Для осуществления ядерных реакций такой метод гораздо эффективнее, чем использование ядер гелия, испускаемых радиоактивными элементами. Во-первых, с помощью ускорителей частицам может быть сообщена энергия порядка 105 МэВ, т. е. гораздо большая той, которую имеют а-частицы (максимально 9 МэВ). Во-вторых, можно использовать протоны, которые в процессе радиоактивного распада не появляются (это целесообразно потому, что заряд протонов вдвое меньше заряда Первая ядерная реакция на быстрых протонах была осуществлена в 1932 г. Удалось расщепить литий на две
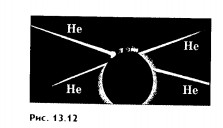
Как видно из фотографии треков в камере Вильсона (рис. 13.12), ядра гелия разлетаются в разные стороны вдоль одной прямой согласно закону сохранения импульса (импульс протона много меньше импульса возникающих Энергетический выход ядерных реакций. В описанной выше ядерной реакции кинетическая энергия двух образующихся ядер гелия оказалась больше кинетической энергии вступившего в реакцию протона на 7,3 МэВ. Превращение ядер сопровождается изменением их внутренней энергии (энергия связи). В рассмотренной реакции удельная энергия связи в ядрах гелия больше удельной энергии связи в ядре лития. Поэтому часть внутренней энергии ядра лития превращается в кинетическую энергию разлетающихся
Энергетическим выходом ядерной реакции называется разность энергий покоя ядер и частиц до реакции и после реакции. Согласно вышесказанному энергетический выход ядерной реакции равен также изменению кинетической энергии частиц, участвующих в реакции. Если суммарная кинетическая энергия ядер и частиц после реакции больше, чем до реакции, то говорят о выделении энергии. В противном случае реакция идет с поглощением энергии. Именно такая реакция происходит при бомбардировке азота Выделяющаяся при ядерных реакциях энергия может быть огромной. Но использовать ее при столкновениях ускоренных частиц (или ядер) с неподвижными ядрами мишени практически нельзя. Ведь большая часть ускоренных частиц пролетает мимо ядер мишени, не вызывая реакцию. Ядерные реакции на нейтронах. Открытие нейтрона было поворотным пунктом в исследовании ядерных реакций. Так как нейтроны не имеют заряда, то они беспрепятственно проникают в атомные ядра и вызывают их изменения. Например, наблюдается следующая реакция:
Великий итальянский физик Энрико Ферми первым начал изучать реакции, вызываемые нейтронами. Он обнаружил, что ядерные превращения обусловлены не только быстрыми, но и медленными нейтронами. Причем эти медленные нейтроны оказываются в большинстве случаев даже гораздо более эффективными, чем быстрые. Поэтому быстрые нейтроны целесообразно предварительно замедлять. Замедление нейтронов до тепловых скоростей происходит в обыкновенной воде. Этот эффект объясняется тем, что в воде содержится большое число ядер водорода — протонов, масса которых почти равна массе нейтров. Следовательно, нейтроны после соударений движутся со скоростью теплового движения. При центральном соударении нейтрона с покоящимся протоном он целиком передает протону свою кинетическую энергию. Реакции, в которые вступают атомные ядра, очень разнообразны. Нейтроны не отталкиваются ядрами и поэтому особенно эффективно вызывают превращения ядер. ДЕЛЕНИЕ ЯДЕР УРАНА |

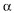 -лучи,
-лучи, 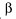 -лучи,
-лучи, 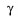 -лучи).
-лучи).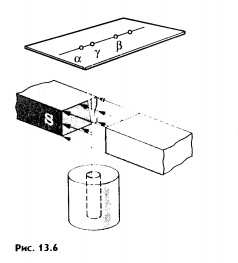
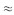 1,66057 • 10-27 кг.
1,66057 • 10-27 кг.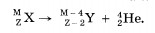
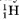 . Для
. Для 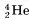 и т. д. При
и т. д. При 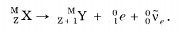
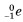 обозначает электрон: индекс 0 вверху означает, что масса его очень мала по сравнению с атомной единицей массы,
обозначает электрон: индекс 0 вверху означает, что масса его очень мала по сравнению с атомной единицей массы, 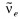 — электронное антинейтрино — нейтральная частица с очень малой (возможно, нулевой) массой, уносящая при
— электронное антинейтрино — нейтральная частица с очень малой (возможно, нулевой) массой, уносящая при 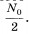

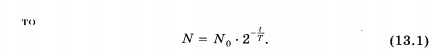
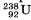 равен 4,5 млрд лет. Именно поэтому активность урана на протяжении нескольких лет заметно не меняется. Период полураспада радия значительно меньше — он равен 1600 лет. Поэтому активность радия значительно больше активности урана. Есть радиоактивные элементы с периодом полураспада в миллионные доли секунды.
равен 4,5 млрд лет. Именно поэтому активность урана на протяжении нескольких лет заметно не меняется. Период полураспада радия значительно меньше — он равен 1600 лет. Поэтому активность радия значительно больше активности урана. Есть радиоактивные элементы с периодом полураспада в миллионные доли секунды.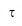 .
. М = Zmp + Nmn - Мя
М = Zmp + Nmn - Мя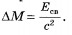 .
.