Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Компоненты дыхательной цепи митохондрий, их роль в переносе протонов и электронов
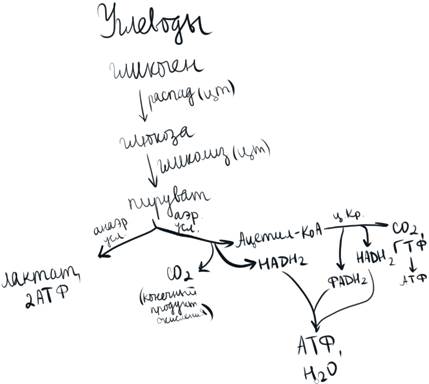
Дыхательная цепь - это участок внутренне й мембраны митохондрий, содержащий компоненты белковой и небелковой природы, которые участвуют протонов и электронов к кислороду. 1) I - комплекс: фермент НАДН-дегидрогеназа, коферментом является ФМН (флавиномононуклеотид - производное витамина В2) 2) Железосерные белки - FeS - белки, перенос электронов осуществляет атом железа, при этом меняется степень окисления железа: Fe +3 + e = Fe+2 Fe+2 - e = Fe+3 3) Липид - убихинон, или коэнзим Q 4) III комплекс: цитохромы b и c1 5) Цитохром С 6) IV комплекс: цитохромы А и А3 7) II комплекс: включается сукцинат (в качестве субстрата), фермент сукцинатдегидрогеназа (СДГ) - коферментом является ФАД. Цитохромы - это сложные белки - гемопротеины, у которых небелковая часть представлена гемом, в центре гема расположен атом железа, который участвует в переносе электронов, при этом меняется степень окисления железа. Цитохром А3 содержит медь, которая также участвует в переносе электронов: Cu +2 + e = Cu +1 Cu +1 - e = Cu +2 3 - В эксперименте с изолированными митохондриями в качестве окисляемого субстрата использовали малат. Чему равен коэффициент Р/О для этой реакции? как повлияет на скорость реакций окисления и коэффициент Р/О добавление амитала натрия? Как изменятся эти параметры при добавлении сукцината? 1) Малат превращается в цикле кребса с участием кофермента над, в результате образуется надн2 и оксалоацетат. надн2 окисляется на дыхательной цепи с образованием 3 атф, р/о = 3 2) при добавлении амитала натрия происходит ингибирование 1го комплекса дыхательной цепи, окисление не идёт, атф не образуется. р/о = 0 3) сукцинат является участником цикла кребса, в результате реакции с участием кофермента фад образуется фумарат и фадн2. фадн2 окисляется на дыхательной цепи с образованием 2 атф. р/о =2 Возможно ли длительное выполнение физической нагрузки в условиях низких температур? Нет. При длительном пребывании на холоде главное для организма-согреться. Появляются разобщители. Большая часть энергии идёт на тепло. Меньше на АТФ БИЛЕТ 2: 1 - Общая схема распада углеводов.
Механизм синтеза АТФ на дыхательной цепи митохондрий 1961 г - теория Митчелла - хемиоосмотическая концепция, объясняющая механизм синтеза АТФ на дыхательной цепи митохондрий. Согласно теории Митчела на внутренней мембране митохондрий формируется электрохимический потенциал.
Он состоит из 2 компонентов: 1) электрический: сторона внутренне мембраны, обращенная в ММП, заряжена положительно из-за скопления протонов а ММП; сторона внутренней мембраны, обращенная в матрикс, заряжена отрицательно из-за дефицита протонов и скопления ОН-. 2) химический: сторона внутренней мембраны, обращенная в ММП, контактирует с кислой средой из-за скопления протонов в ММП; сторона внутренней мембраны, обращенная в матрикс, контактирует с щелочной средой из-за дефицита протонов и скопления ОН-. Электро-химический потенциал внутренней мембраны митохондрий побуждает протоны двигаться из ММП в матрикс, но внутренняя мембрана непроницаема для протонов в любом месте. Протоны могут пересечь внутреннюю мембрану по каналам фермента АТФ - синтетазы. АТФ - синтетаза состоит из 2 частей: 1) Гидрофобная часть - Fo; является каналом для перемещения протонов из ММП в матрикс. 2) Гидрофильная часть - F1; содержит активный центр, где происходит реакция: АДФ + Ф = АТФ. Движение протонов по каналу АТФ - синтетазы приводит к активации активного центра фермента, и происходит синтез АТФ их АДФ и Ф, то есть, протоны являются активаторами АТФ - синтетазы и, соответственно, синтеза АТФ. В эксперименте с изолированными митохондриями в качестве окисляемого субстрата использовали цитрат. Чему равен коэффициент Р/О для этой реакции? Как повлияет на скорость реакций окисления и коэффициент Р/О добавление амитала натрия? Как изменятся эти параметры при добавлении аскорбиновой кислоты? Цитрат образуется в цикле Кребса, дальше он окисляется до изоцитрата, изоцитрат окисляется до альфа-кетоглутарата. При превращении изоцитрата в альфа кетоглутарат образуется надн2, который окисляется на дыхательной цепи с образованием 3 атф РО=3 Добавили амитал натрия, который блокирует первый комплекс дых.цепи, окисление не идёт, энергия не образуется.т.е Р/о=0. Аскорбиновая кислота восстанавливает цитохром С, значит, от кислоты электроны переходят на цитохром С. Далее, от него электроны переходят на 4 комплекс, далее на кислород. Цепь активна от цитохрома С по 1/2 молекулы кислорода, где образуется 1 молекула АТФ.
|
|||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 139; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.202.167 (0.004 с.) |