
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Простые и сложные вещества. Химический элементСодержание книги
Поиск на нашем сайте Простые и сложные вещества. Химический элемент
Углерод С | Графит

| ||||
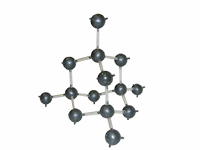
Алмаз

|
Сложные вещества часто называют химическими соединениями, например оксид ртути(II) HgO (получается путем соединения атомов простых веществ - ртути Hg и кислорода O2), бромид натрия(получается путем соединения атомов простых веществ - натрия Na и брома Br2).
Итак, подытожим вышесказанное. Молекулы вещества бывают двух видов:
1. Простые – молекулы таких веществ состоят из атомов одного вида. В химических реакциях не могут разлагаться с образованием нескольких более простых веществ.
2. Сложные – молекулы таких веществ состоят из атомов разного вида. В химических реакциях могут разлагаться с образованием более простых веществ.
Различие понятий “химический элемент” и “простое вещество”
Отличить понятия “химический элемент” и “простое вещество” можно при сравнении свойств простых и сложных веществ. Например, простое вещество – кислород – бесцветный газ, необходимый для дыхания, поддерживающий горение. Мельчайшая частица простого вещества кислорода – молекула, которая состоит из двух атомов. Кислород входит также всостав оксида углерода (угарный газ) и воды. Однако, в состав воды и оксида углерода входит химически связанный кислород, который не обладает свойствами простого вещества, в частности он не может быть использован для дыхания. Рыбы, например, дышат не химически связанным кислородом, входящим в состав молекулы воды, а свободным, растворенным в ней. Поэтому, когда речь идет о составе каких – либо химических соединений, следует понимать, что в эти соединения входят не простые вещества, а атомы определенного вида, то есть соответствующие элементы.
При разложении сложных веществ, атомы могут выделяться в свободном состоянии и соединяясь, образовывать простые вещества. Простые вещества состоят из атомов одного элемента. Различие понятий «химический элемент» и «простое вещество» подтверждается и тем, что один и тот же элемент может образовывать несколько простых веществ. Например, атомы элемента кислорода могут образовать двухатомные молекулы кислорода и трехатомные – озона. Кислород и озон – совершенно различные простые вещества. Этим объясняется тот факт, что простых веществ известно гораздо больше, чем химических элементов.
Пользуясь понятием «химический элемент», можно дать такое определение простым и сложным веществам:
Задания для закрепления
ОТНОСИТЕЛЬНАЯ АТОМНАЯ МАССА
Историческая справка: Английский ученый Джон Дальтон (1766–1844) на своих лекциях демонстрировал студентам выточенные из дерева модели атомов, показывая, как они могут соединяться, образуя различные вещества. Когда одного из студентов спросили, что такое атомы, он ответил: «Атомы – это раскрашенные в разные цвета деревянные кубики, которые изобрел мистер Дальтон».
Конечно, Дальтон прославился не своими «кубиками» и даже не тем, что в двенадцатилетнем возрасте стал школьным учителем. С именем Дальтона связано возникновение современной атомистической теории. Впервые в истории науки он задумался о возможности измерения масс атомов и предложил для этого конкретные способы. Понятно, что непосредственно взвесить атомы невозможно. Дальтон рассуждал только о «соотношении весов мельчайших частиц газообразных и других тел», то есть об относительных их массах. И поныне, хотя масса любого атома в точности известна, ее никогда не выражают в граммах, так как это исключительно неудобно. Например, масса атома урана – самого тяжелого из существующих на Земле элементов – составляет всего 3,952·10–22 г. Поэтому массу атомов выражают в относительных единицах, показывающих, во сколько раз масса атомов данного элемента больше массы атомов другого элемента, принятого в качестве стандарта. Фактически это и есть «соотношение весов» по Дальтону, т.е. относительная атомная масса.
· Массы атомов очень малы.
Абсолютные массы некоторых атомов:
m (C) =1,99268 ∙ 10-23 г
m (H) =1,67375 ∙ 10-24 г
m (O) =2,656812 ∙ 10-23 г
· В настоящее время в физике и химии принята единая система измерения.
Введена атомная единица массы (а.е.м.) (выписать)
m (а.е.м.) = 1/12 m (12 C) = 1,66057 ∙ 10- 24 г.
· Ar(H) = m(атома) / m (а.е.м.) =
= 1,67375 ∙ 10-24 г/1,66057 ∙ 10-24 г = 1,0079 а.е.м.
· Ar – показывает, во сколько раз данный атом тяжелее 1/12 части атома 12С, это безразмерная величина. (выписать определение)
ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ ТЕМЫ
№1 (устно)
Используя ПСХЭ составьте пары из знаков химических элементов и соответствующих русских названий:
- N, Ar, P, Al, S, Mg, Cr
- Алюминий, сера, азот, хром, фосфор, аргон, магний
№2 (устно)
Используя ПСХЭ определите относительные атомные массы химических элементов с порядковыми номерами: 80, 23, 9, 2
№3 (устно).
Дайте характеристикухимическому элементам – О, Na, Cr по его положению в ПСХЭ согласно плану:
- Название русское
- Порядковый номер
- Произношение
- Значение относительной атомной массы
№4 (устно)
Разгадайте новое слово, которое можно получить, если от начала или конца названия химического элемента убрать число букв, соответствующее числу точек.
Например, •Cr, убираем из названия "хром" одну начальную букву и получаем "ром"
а): Na.
б) Mg:.
в). F
г) Ba:
№5 (устно)
Разгадайте новое слово,которое можно получить, если от начала или конца названия химического элемента убрать число букв, соответствующее числу точек.
А):. Pd:
Б). Sn.
В): Co:
Г):: C
№6.
"Химический диктант" (проверить себя, работа с родителями)
Ваша задача при ответе на данный вопрос записать химические знаки (символы) элементов, русские названия которых будут приведены ниже (при написании ответа, записывайте символы через запятую и пробел, например, Ti, Co, Al):
Сера
Азот
Водород
Медь
Углерод
Калий
Кальций
Фосфор
№7.
Поработайте с тренажёром "Относительные атомные массы"
Предлагаю Вам ознакомиться и разобраться
с типами заданий по теме и их решениями
Законспектируйте
№1. Используя ПСХЭ (таблицу элементов Менделеева) составьте пары из знаков химических элементов и соответствующих русских названий:
• Ca, Cu, Ag, Sn, Pb, Na, Zn
• Олово, свинец, медь, натрий, кальций, цинк, серебро
Решение: Ca - кальций, Cu - медь, Ag - серебро, Sn - олово, Pb - свинец, Na - натрий, Zn - цинк.
№2. Используя ПСХЭ определите относительные атомные массы с порядковыми номерами: 26, 16, 7, 8
Решение:
26 - Ar(Fe) = 56;
16 - Ar(S) = 32;
7 - Ar(N) = 14;
8 - Ar(O) = 16.
№3. Дайте характеристику химическому элементу – S по его положению в ПСХЭ согласно плану:
1. Название русское
2. Порядковый номер
3. Произношение
4. Значение относительной атомной массы
Решение:
1) Сера, 2) №16, 3) «эс», 4) Ar(S) = 32.
№4. Дайте русские названия Химическим элементам:
Br, Fe
Вычислите значения относительных атомных масс их атомов.
Решение:
Br – бром, Ar(Br) = 80,
Fe – железо, Ar(Fe) = 56.
№5. Разгадайте новое слово, которое можно получить, если от начала или конца названия химического элемента убрать число букв, соответствующее числу точек.
а): Au б): Ag в) U. г): Rn
Решение:
А) Лото,
Б) Ребро,
В) Ура,
Г) Дон
№6. Вычислите абсолютную массу атома углерода.
Дано:
Ar(C) = 12 (из таблицы)
m(а.е.м.) = 1/12 m(12C) = 1,66057 ∙ 10-24 г.
_____________
Найти:
mC -?
____________
Решение:
m(атома) = Ar ∙ 1,66 ∙ 10 -27 кг
m(С) = 12 ∙ 1,66 ∙ 10 -27 кг = 19,92∙ 10 -27 кг
Ответ: m(С) = 19,92∙ 10 -27 кг
Простые и сложные вещества. Химический элемент
Об атомах и химических элементах
Другого ничего в природе нет
ни здесь, ни там, в космических глубинах:
все — от песчинок малых до планет —
из элементов состоит единых.
С. П. Щипачев, «Читая Менделеева».
В химии кроме терминов “атом” и “молекула” часто употребляется понятие “элемент”. Что общего и чем эти понятия различаются?
Химический элемент – это атомы одного и того же вида. Так, например, все атомы водорода – это элемент водород; все атомы кислорода и ртути – соответственно элементы кислород и ртуть.
В настоящее время известно более 107 видов атомов, то есть более 107 химических элементов. Нужно различать понятия “химический элемент”, “атом” и “простое вещество”
Простые и сложные вещества
По элементному составу различают простые вещества, состоящие из атомов одного элемента (H2, O2,Cl2, P4, Na, Cu, Au), и сложные вещества, состоящие из атомов разных элементов (H2O,NH3, OF2, H2SO4, MgCl2,K2SO4).
В настоящее время известно 115 химических элементов, которые образуют около 500простых веществ.
Самородное золото - простое вещество.
Способность одного элемента существовать в виде различных простых веществ, отличающихся по свойствам, называется аллотропией.Например, элемент кислород O имеет две аллотропные формы - дикислород O2 и озон O3с различным числом атомов в молекулах.
Аллотропные формы элемента углерод C - алмаз и графит - отличаются строение их кристаллов.Существуют и другие причины аллотропии.
|
Углерод С



Сложные вещества часто называют химическими соединениями, например оксид ртути(II) HgO (получается путем соединения атомов простых веществ - ртути Hg и кислорода O2), бромид натрия(получается путем соединения атомов простых веществ - натрия Na и брома Br2).
Итак, подытожим вышесказанное. Молекулы вещества бывают двух видов:
1. Простые – молекулы таких веществ состоят из атомов одного вида. В химических реакциях не могут разлагаться с образованием нескольких более простых веществ.
2. Сложные – молекулы таких веществ состоят из атомов разного вида. В химических реакциях могут разлагаться с образованием более простых веществ.
Различие понятий “химический элемент” и “простое вещество”
Отличить понятия “химический элемент” и “простое вещество” можно при сравнении свойств простых и сложных веществ. Например, простое вещество – кислород – бесцветный газ, необходимый для дыхания, поддерживающий горение. Мельчайшая частица простого вещества кислорода – молекула, которая состоит из двух атомов. Кислород входит также всостав оксида углерода (угарный газ) и воды. Однако, в состав воды и оксида углерода входит химически связанный кислород, который не обладает свойствами простого вещества, в частности он не может быть использован для дыхания. Рыбы, например, дышат не химически связанным кислородом, входящим в состав молекулы воды, а свободным, растворенным в ней. Поэтому, когда речь идет о составе каких – либо химических соединений, следует понимать, что в эти соединения входят не простые вещества, а атомы определенного вида, то есть соответствующие элементы.
При разложении сложных веществ, атомы могут выделяться в свободном состоянии и соединяясь, образовывать простые вещества. Простые вещества состоят из атомов одного элемента. Различие понятий «химический элемент» и «простое вещество» подтверждается и тем, что один и тот же элемент может образовывать несколько простых веществ. Например, атомы элемента кислорода могут образовать двухатомные молекулы кислорода и трехатомные – озона. Кислород и озон – совершенно различные простые вещества. Этим объясняется тот факт, что простых веществ известно гораздо больше, чем химических элементов.
Пользуясь понятием «химический элемент», можно дать такое определение простым и сложным веществам:
|
| Поделиться: |




