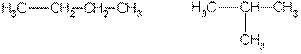Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гомологи и гомологический ряд определение.Содержание книги
Поиск на нашем сайте Гомологи – это вещества близкие по строению и свойствам, которые отличаются на одну или несколько групп – СН2. Гомологический ряд- последовательность соединений, расположенных в порядке возрастания относительно молекулярных масс,сходных по строению и свойствам, но отличающихся от соседних гомологов (группа – СН2) – гомологической разностью. Изомеры и их примеры Явление изомерии было открыто Ю. Либихом и Ф. Вёлером в 1823г. Научное обоснование явлению изомерии было дано А. М. Бутлеровым в рамках теории строения. Изомеры – это вещества, имеющие одинаковый качественный и количественный состав, но различное строение и, следовательно, разные свойства. Явление существования изомеров называется изомерией. Количество изомеров одного вещества зависит от количества атомов углерода в молекуле. Чем длиннее цепь, тем больше вариантов изомерии.
Существуют два вида изомерии: I. Структурная – заключается в различной последовательности соединения атомов в цепи молекулы:
межклассовую изомерию, которая, по сути, зависит от положения функциональной группы. В некоторых случаях при перенесении атома, например, с конца в середину молекулы, образуется вещество другого класса. При этом молекулярная формула веществ остаётся одинаковой. Например, CH3-CH2-OH – это этанол, а CH3-O-CH3 – диметиловый эфир. Молекулярная формула обоих веществ – С2Н6О.
II. Пространственная (стерео) – обусловлена различным положением атомов или групп относительно двойной связи или цикла, исключающих свободное вращение соединённых атомов углерода Геометрическая 2. Оптическая (хар-на для соединений с двойной связью ) Явление изомерии возникает, если молекула несовместима со своим изображением в зеркале. Геометрическая изомерия подразделяется на два типа: · цис-изомерию – радикалы располагаются по одну сторону условной плоскости, разделяющей молекулу пополам; · транс-изомерию – радикалы лежат по разным сторонам условной плоскости. Строение органических веществ Атомы углерода отличаются от атомов других элементов тем, что способны образовывать устойчивые химические связи друг с другом. Они могут связываться в цепи разной длины. Цепи бывают линейные и разветвлённые. Атомы углерода соединяются также в циклы разной величины. Молекулы органических веществ состоят обычно из атомов неметаллов, поэтому в них присутствуют ковалентные связи. Число ковалентных связей, которые образует атом, определяет его валентность В основе органической химии лежит теория химического строения органических веществ А. М. Бутлерова. Её основные положения Теорию химического строения органических соединений впервые представил Александр Бутлеров в 1861 году, заложив основу органической химии. Он показал, что свойства веществ зависят не только от качественного и количественного состава, но и от структуры молекулы. Атомы в молекулах органических веществ соединены в определённом порядке в соответствии с их валентностью. Углерод в органических соединениях всегда четырёхвалентен, кислород — двухвалентен, а водород и галогены — одновалентны.
В молекуле метилового спирта атом углерода соединён ковалентными связями с четырьмя другими атомами, атом кислорода — с двумя, а каждый атом водорода образует одну ковалентную связь.
|
||||||||||||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 141; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.41 (0.006 с.) |
|||||||||||||||