
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Выберите два реактива с правильными аналитическими эффектами. ⇐ ПредыдущаяСтр 7 из 7
{ = BaCl2 -- белый осадок нерастворимый в кислотах ~ Na2 HPO4 + NH4 OH -- белый кристаллический осадок = K4 [Fe(CN)6 ] -- белый студенистый осадок ~ Na2 S -- желтый кристаллический осадок ~AgNO3 -- белый осадок, растворимый в р-ре аммиака }
В аптеке изготовлена микстура по рецепту: Калия бромида Кофеин-бензоата натрия по 0,5 Воды до 200 мл. Подтвердите наличие ионов K + и Br -- в растворе, используя фармакопейные реакции. Выберите два реактива с правильными аналитическими эффектами. { = H2 (C4H4O6) – белый кристаллический осадок ~ Na3[Cо(NO2)6] -- белый кристаллический осадок ~ AgNO3 -- белый осадок, растворимый в р-ре аммиака = AgNO3 -- св-желтый осадок, малорастворммый в р-ре аммиака ~ (NH4)2 C2 O4 -- белый осадок }
В аптеке изготовлен раствор для инъекций Раствор натрия тиосульфата 30%- 200мл Подтвердите наличие ионов Na { ~ BaCl2 -- белый осадок нерастворимый в кислотах ~ HCl – выделение углекислого газа = HCl –выделение св.-желтого осадка серы = окрашивание пламени в желтый цвет ~ окрашивание пламени в фиолетовый цвет }
В аптеке изготовлен концентрат натрия гидрокарбоната 5%. - 200мл Подтвердите наличие ионов Na { ~ BaCl2 -- белый осадок нерастворимый в кислотах = HCl – выделение углекислого газа ~ HCl –выделение св.-желтого осадка серы = окрашивание пламени в желтый цвет ~ окрашивание пламени в фиолетовый цвет }
В аптеке изготовлена микстура по рецепту: Микстура Бурже состава: Натрия гидрокарбоната 8,0 Натрия фосфата 4,0 Натрия сульфата 2,0 Воды очищенной 500 мл. Подтвердите наличие ионов PO { ~ H2 (C4H4O6) – белый кристаллический осадок = BaCl2 - белый осадок нерастворимый в кислотах ~ AgNO3 -- белый осадок, растворимый в р-ре аммиака = AgNO3 -- желтый осадок растворимый в азотной кислоте
~ (NH4)2 C2 O4 -- белый осадок } В аптеке изготовлена микстура по рецепту: Раствор кислоты хлористоводородной 3% - 100 мл. Пепсина 3,0 Выберите метод титриметрического анализа для кислоты хлористоводородной { = алкалиметрия ~ ацидиметрия ~ перманганатометрия ~йодометрия ~аргентометрия } Задача Рассчитайте массу навески для приготовления 1л раствора NaOH С=0,1моль/л (M { ~ 1,58г ~ 3,16г =4,0г ~ 2,48г }
Задача Рассчитайте массу навески KMnO { = 1,58г ~ 3,16г ~ 4,0г ~ 2,48г }
Задача Рассчитайте массу навески Na { ~ 1,58г ~ 3,16г ~ 4,0 г = 1.24г }
|
|||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 91; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.145.173 (0.006 с.) |
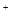 и S
и S 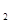 O
O 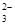 в растворе, используя фармакопейные реакции. Выберите два реактива с правильными аналитическими эффектами.
в растворе, используя фармакопейные реакции. Выберите два реактива с правильными аналитическими эффектами. в растворе, используя фармакопейные реакции. Выберите два реактива с правильными аналитическими эффектами.
в растворе, используя фармакопейные реакции. Выберите два реактива с правильными аналитическими эффектами.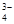 и SO 4 2-, используя фармакопейные реакции. Выберите два реактива с правильными аналитическими эффектами.
и SO 4 2-, используя фармакопейные реакции. Выберите два реактива с правильными аналитическими эффектами. ꞊ 40г/моль). Выберите правильный ответ.
꞊ 40г/моль). Выберите правильный ответ.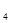 для приготовления 500 мл раствора Сэ=0,2 моль/л (М
для приготовления 500 мл раствора Сэ=0,2 моль/л (М 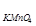 =158 г/моль). Выберите правильный ответ.
=158 г/моль). Выберите правильный ответ. * 5 H
* 5 H 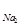

 =248 г/моль). Выберите правильный ответ.
=248 г/моль). Выберите правильный ответ.


