
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение длины световой волны с помощью дифракционной решетки
Поместить дифракционную решетку на пути лазерного излучения. При этом на экране будет изображение в виде далеко отстоящих одно от другого светлых пятен. Измерить с возможно большей точностью угловое положение середин максимумов и по формуле (10) определить длину световой волны. Используемая в работе дифракционная решетка имеет 100 штрихов (щелей) на 1 мм длины (z = 100 штр/мм), поэтому постоянная решетки d = 1/z = 1/100 (мм) = 10 мкм. Измерения повторить несколько раз и результаты занести в таблицу 3. Вычислить ошибку измерений длины волны. Таблица 3
2.2. Определение среднего радиуса эритроцитов Установить на пути лазерного излучения стеклянную пластинку с мазком крови. Измерить угловые положения максимумов и минимумов, т.е. середин светлых и темных кольцевых полос. Объект рекомендуется подвинуть ближе к экрану, чтобы наблюдать более яркую картину и видеть большее число колец. По формулам таблицы 2 (см. «дифракцию на круглом отверстии») вычислить радиус частиц. При расчетах использовать значение длины волны, полученное из измерений по пункту 3.1 (среднее значение). Результаты измерений и вычислений занести в таблицу 4. Таблица 4
Здесь R – радиус эритроцитов. Радиус ρn необходимо измерить не менее 5 раз. Вычислить ошибку измерений R. 2.3. Дополнительное задание С помощью микроскопа измерить диаметр 10 эритроцитов и найти их средний размер. Сравнить со значением, полученным в основном задании. 3. Контрольные вопросы 1. Что называется дифракцией? 2. Сформулировать принцип Гюйгенса-Френеля. 3. Как находятся положения главных максимумов при дифракции света на дифракционной решетке? библиографический список
Лабораторная работа № 4: ВЗАИМОДЕЙСТВИЕ НИЗКОИНТЕНСИВНОГО ЛАЗЕРНОГО ИЗЛУЧЕНИЯ (НЛИ) С БИОЖИДКОСТЯМИ ЧЕЛОВЕКА Цель работы: экспериментального исследования – определение изменений в поведении биожидкостей человека взаимодействующих с НЛИ методом биокристаллографии. КРАТКАЯ ТЕОРИЯ В медицине на основе дегидратации строится множество методик научных исследований и лабораторной диагностики. Одним из прогрессивных методов является кристаллография биологических жидкостей (БЖ). Этот метод – кристаллография биологических жидкостей, основан на изучении различных характеристик фаций биологических жидкостей. Кристаллография базируется на исследовании и изучении структуры, атомно–молекулярного строения, физических свойств, образования и роста кристаллов и других характеристик фации биологической жидкости. Биологические жидкости (чаще всего используемые) это такие жидкости которые проще всего собрать – кровь, плазма крови, слюнная жидкость, слезная жидкость и др. Можно выделить принципиально только три варианта: свободная кристаллизация, в случае, если высушиванию подвергается непосредственно анализируемая биологическая жидкость; инициированный кристаллогенез, – визуализируется результат дегидратации системы «биосреда – базисное кристаллообразующее вещество» преимущественно на основании исследования структурогенеза последнего; парциальная кристаллизация (метод модельных композитов) – совокупность способов воссоздания отдельных составляющих кристаллоскопической картины определенного биологического субстрата.
К настоящему времени в современной кристаллоскопии предложены следующие методы: 1. классическая кристаллоскопия – один из наиболее распространенных вариантов выполнения дегидратационного теста, сущностью которого является непосредственная кристаллизация биологических жидкостей. 2. тезиграфия относится к наиболее общим способам выполнения кристаллоскопического теста и представляет собой дополнительное введение в высушиваемую биожидкость организма человека различных химических веществ с целью инициации процессов кристаллообразования с использованием широкого спектра кристаллообразователей (NaCl, CaCl2, MgCl2 и другие), в большинстве своем обладающих комплексообразующими свойствами, причем концентрации у различных авторов в значительной степени варьируются 3. профильная дегидратация. Подразумевает нанесение биологических жидкостей на предметное стекло, предварительно обработанное раствором лецитина определенной концентрации. С помощью лецитина представляется возможным, по мнению авторов, изменить сродство кристаллов к основе, а, следовательно, трансформировать термодинамические характеристики дегидратируемого биосубстрата. 4. вакуумная кристаллоскопия предусматривает приготовление (высушивание) препаратов в условиях вакуума. Этим достигается изолированность дегидратируемого образца от внешней среды, создается относительно закрытая система, в которой и осуществляется непосредственно удаление жидкой части биосреды и процессы биокристаллизации. 5. кристаллизация биологических жидкостей в закрытой ячейке. Обеспечивается изоляция формирующегося образца от внешней среды аналогично вакуумной кристаллоскопии, однако технически данный способ более удобен для практического применения, так как не требует создания условий вакуума, а лишь использования закрытой ячейки, в которой возможным представляется проводить непосредственный микроскопический анализ. 6. поясная кристаллоскопия – кристаллографический метод исследования, основанный на изучении поясов кристаллов и отдельных кристаллических образований. Физико-химическим базисом способа является неоднородность компонентного состава биологических жидкостей в зависимости от молекулярных масс веществ, являющихся элементами данной биосреды, а, следовательно, различной их способности к передвижению по фации в процессе ступенчатой дегидратации образца и формирования фации. Это приводит к образованию одного или (значительно чаще) нескольких поясов кристаллизации, регистрация которых и позволяет судить о данной характеристике биологической жидкости. 7. метод клиновидной дегидратации. Способ дегидратации капли биологической жидкости, размещенной на прозрачной плоскости. Капля имеет форму клина на поперечном разрезе, что создает условия неравномерной скорости дегидратации в радиальном направлении. Это вызывает осмофоретическое перемещение растворенных веществ в объеме дегидратируемой капли в соответствии с физико-химическими параметрами и формирование четких, строго индивидуализированных структур, соответствующих состоянию организма, из которого была получена исследуемая жидкость.
8. поляризационная микроскопия – способ оценки результатов свободного или инициированного кристаллообразования биологической жидкости в поляризованном свете, позволяющий выявить некоторые дополнительные особенности как фации в целом, так и отдельных ее структурных элементов, а также охарактеризовать ее текстуру. Представляет собой универсальную модификацию подхода к визуализации результатов кристаллогенеза и может быть использован как дополнение к любому из кристаллографических методов исследования биосред. 9. субстратная конгрегация – вспомогательный кристаллографический метод, позволяющий моделировать кристаллообразование отдельных компонентов, являющихся составляющими биологических субстратов (липидов, белков, полисахаридов). В данном случае, по сравнению с методом «модельных композитов», достигается большее приближение к реальному составу биологической среды по ассортименту, но не по точному соотношению компонентов, однако имеется возможность учета изменений биожидкости по основным ее биохимическим элементам. 10. жидкокристаллическая термография – перспективная методика кристаллографических исследований, принципиальным моментом которой является использование холестерических жидкокристаллических (температурный интервал плавления 33,5-38,20С или 36,8-41,20С) покрытий изучаемых поверхностей системами с холестерилпеларголеатом, холестерилолеатом и т. д. В качестве «подложки» при этом используется кожа, на которую наносится состав. Интерпретация преобразования состояния жидких кристаллов оценивается при помощи специализированного спектрофотометра. 11. метод энергоинформационного переноса с биологических жидкостей на носитель заключается в переносе информации с биосред на «чистые горошины молочного сахара», затем на предметном стекле производится их соединение с 0,1 мл базисного вещества (5% водного раствора медного купороса). Приготовление микропрепаратов выполняется в темном помещении в течение 24 ч. Наиболее удобны и часто используемы следующие методы биокристаллографии: · клиновидной, · краевой, · профильной дегидратации; · с помощью поляризационной микроскопии, в закрытой ячейке. Метод клиновидной дегидратации наиболее прост и не требует больших материальных затрат, что, конечно, имеет немаловажную роль. Его изучением занимались такие специалисты как Шаболин В.Н., Шатохина С.Н. и многие другие.
Кристаллизация – это физико-химическая реакция, при которой осуществляется переход каких-либо частиц (атомов, молекул, ионов) в кристаллическую фазу. Наиболее изученным и интересующим нас является способ кристаллизации из жидких фаз, хотя этот процесс возможен из любых дисперсных фаз, в том числе и газообразных.
открытой поверхности. Формирование зон при испарении жидкости в форме, близкой к полусфере, происходит равномерно по всей открытой поверхности капли (рис. 1). Оттого, что полусфера имеет разную толщину слоя в центре и на периферии, в исследуемой капле при испарении воды происходит неравномерное распределение концентрации растворенных веществ: в периферических отделах возрастает более быстрыми темпами по сравнению с центральной частью капли. При этих изменениях проявляются силы осмотические и онкотические. Из-за того, что мощность осмотических сил выше онкотических, соли более быстро перемещаются к центру капли, в сторону зоны меньшей концентрации растворенных веществ, и в борьбе за оставшуюся воду они "выдавливают" органические вещества на периферию капли. В итоге, после высыхания капли биологической жидкости, в ее твердой фазе количественное содержание солей повышается от периферии к центру, а органические вещества сосредоточены в краевой зоне (рис.2). Рисунок 2. Распределение неорганических солей и органических веществ в процессе высыхания капли биологической жидкости на твердой подложке: а – сагиттальный разрез; б – вид сверху
Кристаллизация начинается при определенных внешних условиях: переохлаждении жидкости, перенасыщении пара, дегидратации раствора, когда постепенно возникает множество мелких кристаллов вокруг центров кристаллизации и др. Кристалл растёт, присоединяя атомы или молекулы из жидкости или пара. Большинство природных и технических твердых материалов являются поликристаллами, одиночные кристаллы называют монокристаллами. Образование такой структуры можно объяснить тем, что испарение молекул воды с поверхности «куполообразного» жидкого препарата ведет к возникновению градиента концентраций растворенных в препарате веществ. Под действием гравитации и сил сцепления между молекулами кристаллизующейся пробы, а также между молекулами биопробы и подложки, на которой расположен препарат, в объеме капли возникают неустойчивости Бернара для концентрирующихся при испарении микрочастиц, что ведет к появлению в препарате видимых даже при небольшом увеличении аутоволн. Такие волны считают концентрационными самоорганизующимися структурами с развитой системой связей дальнего порядка.
Процессы первичной кристаллизации БЖ идут в соответствии с естественными программами и технологией кристаллизации из раствора. Начало формирования аморфных структур, кристаллоидов, кристаллов характеризуется появлением первичных центров (зерен) кристаллизации в отдельных тонких слоях. Затем кристаллизация распространяется на следующие слои, что ведет к возникновению линейных, столбчатых или дендритных кристаллических структур. В начале этого процесса, в еще жидком препарате, наблюдается формирование ряда волновых процессов, и лишь на этом фоне по краю препарата, возникают зерна кристаллизации. Наличие жидкой фазы в ходе синтеза обуславливает образование дендритных структур. Из начальных центров кристаллизации развиваются новые элементарные первичные кристаллиты, которые сначала растут по краю окружности препарата, а затем превращаются в центростремительные линейные структуры с характерной ориентировкой зерен, столбчатых и дендритных и аморфных специфических структур. Затем процесс изменения концентраций быстро нарастает, и при этом сложные и длинные белковые молекулы меняют свое концентрическое направление на центростремительное. Это происходит потому, что линейные и нелинейные «каналы» формируются с неравномерными скоростями в зонах с разными градиентами концентраций. Это и вынуждает их ветвиться или образовывать фрактальные структуры. В жидкости, сложной по составу с преобладанием солей, последние занимают среднюю и центральную часть в пробе, а преимущественно органические молекулы – более периферическую его часть. Дегидратация органических составных частей идет медленнее, и после испарения основной части свободной воды начинает активизироваться процесс «борьбы субстратов» за связанную воду. В итоге отложения белков – линейные кристаллиты – раскалываются продольно, а процесс ретракции превращает их в (своего рода) каналы или трещины. В цельной крови на образование описанной структуры влияет наличие форменных элементов – эритроцитов. В препаратах цельной крови, в отличие от сыворотки или плазмы, на процесс самоорганизации тезиограммы искажающее влияние оказывает присутствие клеток. При этом, отдельные клетки могут играть роль центров кристаллизации, но больше проявляется влияние вышедшего в плазму крови из эритроцитов гемоглобина и др. компонентов клеточного содержимого. В этом случае в состав линейных кристаллитов, образованных фибрином и другими белками, имеющими длинные линейные размеры, поступает железосодержащий белок – гемоглобин. Это изменяет характер фрактализации линейных кристаллитов, сокращая их линейные размеры. У линейных кристаллитов цельной крови появляется значительно большее число остроконечных выпячиваний в наружные стороны и отростков, которые вследствие присутствия ионов железа становятся оптически более плотными. В отличие от препаратов цельной крови в ее плазме и сыворотке нет искажающего кристаллизацию влияния клеток, и поэтому формируется типичная кольцевидно-фрактальная структура. Крупные кристаллиты в пробах плазмы крови здорового человека или животного растут в центростремительном направлении, пока не сходятся в центре капли (в препаратах среднего и крупного объема). В процессе бурного роста кристаллитов и кристаллов солей навстречу друг другу, при их слиянии на стыках появлялись полости с газами или жидкостью, в которых вторично, мог идти процесс кристаллизации. В медицинской и биологической практике для чистоты эксперимента целесообразно выделять и делать упор на анализе наиболее стабильных и регулярно проявляющихся признаков. Чем меньше по объему и площади препараты, тем меньше в них случайных флуктуаций и тем выше взаимная обусловленность поведения ее частей. Малообъемные препараты формируют гораздо более неравновесные системы, в которых наблюдаются новые формы кристаллизации веществ. Если возбудить в пластинах малых размеров, с изгибами соизмеримыми длине волны, колебания (как в процессе кристаллизации БЖ), то при благоприятном соотношении параметров возбуждения (длины волны, частоты возбуждения, размера пластины, модуля упругости), на поверхности пластины в местах пересечения узловых линий образуются вращающиеся акустические зоны, обусловленные взаимодействием поверхностных и объемных волн. Кровь является типичным примером ткани организма, где одни коллоиды (клетки) находятся внутри других (плазма). Эти биоколлоиды, или жидкие кристаллы, обусловливают вязкость крови, которая в 5 раз превышает вязкость воды. Жидкокристаллические свойства составных частей крови, плазмы и других БЖ являются основой моделирования самых различных их ответных реакций на воздействие химических, физических и других факторов. Что во многом определяют способность БЖ к согласованному взаимодействию (синэргетике) и к самоорганизации. Синергетика, одна из основ самоорганизации, в противоположность кибернетике, исследует механизмы возникновения новых состояний, структур и форм в динамичных процессах структурообразования, а не сохранения или поддержания старых форм. Поэтому она опирается на принцип положительной обратной связи, когда изменения, возникшие на наноуровне в системе, под действием температурных, механических и других влияний, не подавляются или корректируются, а, наоборот, постепенно накапливаются и в итоге приводят к разрушению старой и возникновению новой макросистемы. Разрушение старой (водной) и самоорганизацию новой (воднообедненной) системы наблюдаются при постановке экспериментов с кровью, гемопрепаратами и другими БЖ. В основе этого динамичного процесса лежат фазовые переходы в биополимерах со свойствами жидких кристаллов (ЖК) в белках, нуклеиновых кислотах и т.п., в кооперативных системах (фосфолипидных мембранах, субклеточных биологических структурах), а также конформационные изменения биомолекул. Исследуемый образец БЖ в открытой системе становится самоорганизующейся диссипативной структурой. Свой вклад в формирование тезиографической картины (ТЗГ) биосубстратов может вносить кластеризация молекул воды. В зависимости от своей кластерной структуры вода способна играть роль матрицы и изменять свойства растворенных в ней солей, а также свойства белковых и углеводных компонентов биосубстратов – таких, как производные макроэргов, аденозинтрифосфата и многих молекул веществ, обладающих ферментной активностью. Кристаллизация крови и ее препаратов оказывается более сложным процессом, чем кристаллизация простых солей из раствора. По мнению А.Ф. Сонина, наблюдаемые в составных частях крови фазовые переходы имеют много общих черт с фазовыми переходами в сверхтекучем гелии. При этом роль квантово-механической волновой функции сверхтекучей фазы, не наблюдаемой в экспериментах с гелием, играет здесь амплитуда волны плотности. Многие молекулы крови имеют свойства ЖК, и в них отмечены аналогии между поведением некоторых дефектов диссипативных структур в жидких кристаллах с эффектом Джозефсена в сверхпроводниках и т.д. Просматриваются также аналогии в поведении ряда дефектов в жидких кристаллах с теоретически предсказанными свойствами магнитных монополей. Процесс формирования ТЗГ крови, ее препаратов или других БЖ оперирует уникальной информацией о ходе кристаллизации, начинающейся на наноуровне в условиях появления пересыщенного раствора и появления порядка среди частиц среды, вначале всего лишь в расположении нескольких атомов. В динамике кристаллизации БЖ важны два процесса: адсорбционный процесс, определяющий рост кристаллов и диффузионный процесс (молекулярная диффузия, режимы естественной и /или вынужденной конвекции), обеспечивающий массоперенос к растущему кристаллу, сопровождающийся рассеянием теплоты кристаллизации. Формирование характерных зональных структур означает окончание первой быстрой фазы динамичного процесса самоорганизации, характеризующееся удалением из препарата большей части жидкости. Эта фаза является наиболее чувствительной к различным факторам среды. В последующих медленно текущих фазах изменения структуры фации идут процессы освобождения из них остатков воды и газов, идет достраивание граней кристаллов солей. Эти процессы характеризуют начало фазы замедленной реструктуризации. Наряду с растрескиванием вдоль продольной оси кристаллитов, продолжается формирование простых кристаллов и кристаллитов сложного состава. Окружающая среда, воздействуя на БК или БЖ, может вызвать изменения в их форме и составе, что, в свою очередь, изменяет структуру и симметрию фации. Это уточняет разницу между кристаллизацией вне и в организме: кристаллизация вне организма – однонаправленный процесс, в организме же любой кристаллоид способен к обратному развитию – растворению. Пробоотбор, пробоподготовка. На поверхность пластины, изготовленной из стекла или иного материала, наносится капля исследуемой биологической жидкости, после чего следует процесс постепенного испарения жидкости (дегидратации) с поверхности данной капли. В ходе дегидратации, содержащиеся в жидкости вещества концентрируются по-разному из-за разной толщины капли: соли, растворённые в образце биологической жидкости (БЖ), при испарении стремятся к центру капли, белки и другие высокомолекулярные вещества остаются на периферии. В результате медленного испарения жидкости формируется тонкая плёнка, которую называют фацией. В процессе испарения воды в капле биологической жидкости происходит перераспределение растворенных веществ, в соответствии с их осмотической активностью, гидрофильностью, молекулярным весом, агрегатным состоянием и другими физико-химическими параметрами. БЖ несёт «структурную» диагностическую информацию о развитии патологического процесса. Особенности состояния организма сказываются на процессе кристаллизации жидкости, поэтому на изображении фации возникают характерные структуры. Наблюдения показали, что по имеющимся маркёрам и их расположению можно с большой уверенностью судить о состоянии организма. Обсудите ход и методику исследований биожидкостей методом биокристаллографии, проанализировав всевозможные варианты. Проведите забор исследуемых биожидкостей. Забор и подготовка образцов: 1. Кровь: · забор крови проводить из четвертого пальца левой руки. · кожу пальца обрабатывается антисептиком, · прокол делается стерильным скарификатором. · первую каплю крови снять. 2. Слюнная жидкость: · забор слюнной жидкости производится при помощи ложки Фолькмана или специальной канюли (средняя порция), · забор проводить в утренние часы, до приема пиши или после (но не ранее чем через 2 ч), после ополаскивания полости рта дистиллированной водой. · каплю секрета поместить на предметное стекло. 3. Слезная жидкость: · забор слезной жидкости провести пипеточным дозатором с помощью пластиковой насадки, имеющей округлый край и закрепленный на пипеточном дозаторе, из нижнего конъюнктивального мешка, порядка 1 мл · собирать в стерильные пробирки. Подготовить контрольный образец. На предварительно обезжиренное, промытое и просушенное предметное стекло нанести образцы биологического материала (плазмы крови или сыворотки крови, цельной крови, слюной жидкости, слезной жидкости) в объеме не более 0,2 мл и высушите методом клиновидной дегидратации.
· первый способ – облучение капиллярной крови непосредственно в фаланге пальца. Для уменьшения скорости кровотока ниже первой фаланги наложить слабый жгут и при облучении палец опустить по направлению к земле. · второй способ – кровь собирается в пробирку и используя установку, изображенную на рисунке 3, провести облучение.
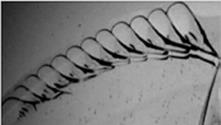
Рисунок 3. Схема установки Из облученного материала приготовьте образцы описанным выше способом. Проведите исследование фаций биожидкостей с помощью микроскопии, выделяя характерные структуры на эталонном образце, и по имеющимся маркерам и их расположению проанализируйте наличие изменений в облученных образцах в зависимости от времени облучения. Различают следующие виды маркеров фации: 1) Гребешковые структуры – линейные трещины с отходящими от них по одну сторону мелкими трещинами, напоминающие форму гребешка. Гребешковые структуры: a. всегда располагаются около границы фации; b. c. состоят из нескольких тупоугольных треугольников; d. длинные стороны треугольников приблизительно параллельны между собой; e. треугольники находятся на небольшом расстоянии друг от друга; f. фон между треугольниками относительно однороден. 2) Жгутовые трещины – радиальные трещины с приподнятыми волнистым краями. Жгуты: a. b. являются множеством коротких слегка волнистых линий, расположенных приблизительно перпендикулярно к трещине; c. обладают ярко выраженной анизотропией.
a. ярко выраженная анизотропия; b. c. наличие коротких волосков (в случае бляшек волоски располагаются под разными углами, а в случае морщин – под одинаковыми). Отличие бляшек и морщин от жгутов состоит в том, что они не находятся вдоль трещин и их отростки не расположены двумя параллельными полосами. Морщины отличаются от бляшек отсутствием однородного пятна и тем, что волоски могут располагаться под одинаковыми углами друг к другу 3) Листовидные структуры – это относительно крупные структуры, доходящие до периферии фации. Признаками листовидных структур являются: a. b. довольно симметричное расположение вдоль радиально направленных трещин; c. лепестки темнее окружающего фона; d. граничные точки листа характеризуются слабым перепадом яркости; e. граница лепестка представляет собой дугообразную линию. 4) a. граница воронки представляет собой эллипс, у которого большая полуось заметно больше малой полуоси; b. область внутри воронки однородна и светлее окружающего фона; c. на границе воронки имеется небольшой перепад яркости; d. воронки расположены между трещинами фации, не пересекая их; e. воронки наблюдаются в центральной зоне фации. 5) a. трещины серебра имеют значительно меньшую яркость по сравнению с окружающим фоном; b. трещины серебра представляют собой некоторое количество темных линий, расположенных параллельно друг другу. 6) a. трещины закрутки имеют значительно меньшую яркость по сравнению с окружающим фоном; b. их форма близка к окружности; c. фон внутри трещины закрутки относительно однороден. 7) Трёхлучевые трещины. Данные структуры имеют ряд следующих особенностей: a. b. они имеют значительно меньшую яркость по сравнению с окружающим фоном.
Подготовьте отчет по результатам вашего научного исследования.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 207; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.14.15.94 (0.119 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 , мм
, мм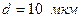
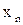 , мм
, мм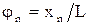 , рад
, рад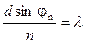 , мкм
, мкм , мкм
, мкм , мм
, мм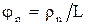 , рад
, рад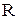 , мкм
, мкм Известно, что биологические жидкости (слюна, кровь, слезная жидкость, моча и др.) при высушивании кристаллизуются. В условиях патологии кристаллизационные свойства биологических жидкостей изменяются.
Известно, что биологические жидкости (слюна, кровь, слезная жидкость, моча и др.) при высушивании кристаллизуются. В условиях патологии кристаллизационные свойства биологических жидкостей изменяются. Метод клиновидной дегидратации, состоит в высушивании капли биологической жидкости на
Метод клиновидной дегидратации, состоит в высушивании капли биологической жидкости на 
 Облучение крови провести двумя способами
Облучение крови провести двумя способами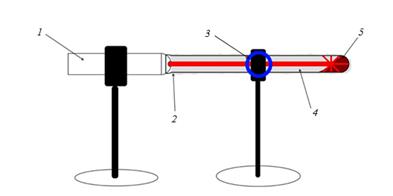
 имеют значительно меньшую яркость по сравнению с окружающим фоном;
имеют значительно меньшую яркость по сравнению с окружающим фоном; располагаются по обе стороны вдоль трещин;
располагаются по обе стороны вдоль трещин; Морщины и токсические бляшки. Токсические бляшки – однородные округлые образования, обрамленные с одной стороны множеством коротких, слегка волнистых линий (отростков). Морщины (складчатости) – локальные смещения рельефа фации с образованием параллельных складок на её поверхности Характерными особенностями данных структур являются:
Морщины и токсические бляшки. Токсические бляшки – однородные округлые образования, обрамленные с одной стороны множеством коротких, слегка волнистых линий (отростков). Морщины (складчатости) – локальные смещения рельефа фации с образованием параллельных складок на её поверхности Характерными особенностями данных структур являются: наличие однородного пятна (бляшки);
наличие однородного пятна (бляшки); их расположение на большом расстоянии от центра фации;
их расположение на большом расстоянии от центра фации;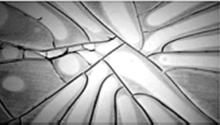 Воронкообразные структуры –вытянутые однородные светлые области приблизительно эллиптической формы. Данные структуры имеют следующие особенности:
Воронкообразные структуры –вытянутые однородные светлые области приблизительно эллиптической формы. Данные структуры имеют следующие особенности: Трещины «серебра» – ряд мелких, параллельных линейных тёмных трещин. Данные структуры имеют следующие особенности:
Трещины «серебра» – ряд мелких, параллельных линейных тёмных трещин. Данные структуры имеют следующие особенности: Трещины «закрутки» –тёмные спиралевидные трещины. Трещины закрутки имеют ряд следующих особенностей:
Трещины «закрутки» –тёмные спиралевидные трещины. Трещины закрутки имеют ряд следующих особенностей: они представляют собой три отрезка небольшой длины, начинающиеся в одной точке и образующие между собой приблизительно равные углы;
они представляют собой три отрезка небольшой длины, начинающиеся в одной точке и образующие между собой приблизительно равные углы;


