
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Лаборатория виртуальных экспериментовСодержание книги
Поиск на нашем сайте
ЛАБОРАТОРНАЯ РАБОТА №8 ФИЗИКА. ТЕРМОДИНАМИКА. ПОЛИТРОПНЫЙ ПРОЦЕСС Методические указания к виртуальной лабораторной работе
САНКТ-ПЕТЕРБУРГ 2019
ВВЕДЕНИЕ
Общая цель выполнения любой работы из лабораторного практикума, как и преподавания дисциплины в целом - обеспечить приобретение знаний и умений по физике в соответствии с Федеральным государственным образовательным стандартом (ФГОС). Лабораторный практикум является одной из форм образовательных технологий и направлен на формирование общих и профессиональных компетенций. В результате выполнения лабораторной работы студенты приобретают навыки использования современной научной аппаратуры для проведения физического эксперимента и научных исследований; осваивают методы физического исследования, которые включают планирование, постановку и обработку результатов эксперимента (компьютерную, аналитическую, графическую); учатся систематизировать информацию по теме исследований. При этом формируются способности к самостоятельной и познавательной деятельности студентов. Методические указания к лабораторной работе предназначены для самостоятельной работы студентов. Они содержат основные теоретические сведения по теме, а также порядок выполнения и оформления лабораторной работы. При выполнении лабораторной работы, студент должен понимать физический смысл данного явления или процесса, рассматриваемого в лабораторной работе. Поэтому к выполнению работы целесообразно приступать только после изучения теоретического и методического материала, соответствующего данному разделу, используя при этом как данную методическую разработку, так и рекомендуемую учебную литературу.
ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА И ЕЁ ПАРАМЕТРЫ
Термодинамическая система – совокупность макроскопических тел, выбранных к рассмотрению, которые могут обмениваться между собой и окружающей средой (т. е. с телами, не принадлежащими системе) энергией и веществом. В термодинамике для описания макроскопического состояния вещества используют такие физические величины как давление Р,объем V,температура Т,концентрация частиц п,масса тела т и т.п. Эти физические величины характеризуют свойства и состояние системы в большом масштабе и называются термодинамическими параметрами состояния.
Параметры состояния бывают двух родов: экстенсивные, пропорциональные количеству вещества; интенсивные – непропорциональные количеству вещества. Например, имеем две порции идеального газа с температурой Т объёмом V и количеством вещества n, находящихся в равновесии. Соединим их. При этом количество молей удвоится (2n). Удвоится и объем (2 V), а также увеличится внутренняя энергия (2 U). При этом у новой системы температура Т и давление Р имеют те же значения, что и в исходных порциях. Таким образом, параметры (V, U) ~ n и являются экстенсивными, а (Т и Р) Равновесное состояние – такое макросостояние системы, в котором все параметры состояния имеют определённые значения, не изменяющиеся со временем, до тех пор, пока не изменятся внешние условия. Если система находится в равновесном состоянии, то ее параметры состояния имеют определенные значения, которые зависят только от состояния и не зависят от «прошлого» системы. При термодинамическом равновесии интенсивные параметры сохраняют постоянные значения во всей системе. Термодинамический процесс – переход из одного равновесного состояния в другое. Изопроцессы – процессы изменения состояния термодинамической системы, протекающие при неизменной массе и постоянном значении одного из параметров состояния.
|
|||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 140; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.127.230 (0.009 с.) |

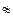 n – интенсивными.
n – интенсивными.


