
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение теплоты нейтрализации
Цель работы – определение теплоты нейтрализации сильной кислоты сильным основанием. Приборы и реактивы: калориметрическая установка, аналитические весы, мерный цилиндр на 250 Краткие теоретические положения Теплотой нейтрализации называется количество тепла, которое выделяется при взаимодействии 1 моля кислоты с 1 молем основания. Установлено, что реакция нейтрализации 1 моля сильной одноосновной кислоты (HCL,
Чтобы правильно определить тепловой эффект реакции нейтрализации, следует учесть, что при вливании раствора сильной кислоты в раствор щелочи в калориметре кроме основного процесса, сопровождающегося тепловым эффектом Таким образом, измеренная опытным путём теплота процесса
Порядок выполнения работы 1. Определение теплоёмкости калориметрической установки. Определяют теплоёмкость калориметрической установки 2. Определение суммарной теплоты процессов, протекающих в калориметре
3. Определение теплоты процесса разбавления кислоты щёлочью 4. Определение теплоты процесса разбавления щёлочи водным раствором кислоты
|
|||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 440; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.147.124 (0.004 с.) |
 , мерная пипетка на 5
, мерная пипетка на 5 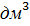 , раствор сильной кислоты (HCL,
, раствор сильной кислоты (HCL, 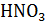 ,
, 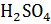 ) c = 2 моль/
) c = 2 моль/ 
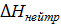 , протекает процесс разбавления кислоты водным раствором щелочи с тепловым эффектом
, протекает процесс разбавления кислоты водным раствором щелочи с тепловым эффектом  и процесс разбавления щелочи водным раствором кислоты с тепловым эффектом
и процесс разбавления щелочи водным раствором кислоты с тепловым эффектом  .
.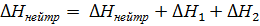
 по теплоте растворения KCL в воде.
по теплоте растворения KCL в воде. Мерным цилиндром отмеряют и заливают в калориметрический стакан 150
Мерным цилиндром отмеряют и заливают в калориметрический стакан 150  раствора кислоты вливают в 150
раствора кислоты вливают в 150  только вместо раствора щёлочи в калориметрический стакан заливается 150
только вместо раствора щёлочи в калориметрический стакан заливается 150 


