Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Первичные источники электрической энергииСтр 1 из 7Следующая ⇒
ПЕРВИЧНЫЕ ИСТОЧНИКИ ЭЛЕКТРИЧЕСКОЙ ЭНЕРГИИ
В иды первичных источников питания Любые радиотехнические устройства и системы с точки зрения обеспечения электрической энергией могут быть представлены в виде схемы, приведенной на рисунке.
Структурная схема питания электронной аппаратуры
На этом рисунке обозначено: ПИП — первичный источник питания — преобразует неэлектрические виды энергии в электрическую; ВИП — вторичный источник питания — преобразует электрическую энергию к виду удобному для потребителя (нагрузки) и собственно нагрузка — радиоэлектронная аппаратура (РЭА). Вторичные источники питания будут рассматриваться в дисциплине «Электроника и микропроцессорная техника». К первичным источникам питания обычно относят: Химические источники Термогенераторы Солнечные батареи Радиоизотопные источники Топливные элементы Ветрогенераторы Электрические машины
Химические источники
Классификация химических источников тока (ХИТ) Разовые источники тока Первую электрическую батарею создал в 1799 году итальянский физик и химик и Алессандро Вольта изобретатель источника постоянного электрического тока. Он представлял собой цинковую и медную пластины и помещённую между ними бумагу, смоченную солёной водой. Он же, позж, соединив последовательно несколько десятков таких элементов создал первую батарею, которая дала толчок исследованиям электрических явлений и устройств.
Граф Алесса́ндро Джузеппе Анто́нио Анаста́сио Во́льта (18 февраля 1745— 5 марта 1827) — итальянский физик, химик и физиолог, один из основоположников учения об электричестве и его «Вольтов столб».
Конструкция Вольтова столба
Батареи (батарейки) Батарея (фр. batterie) — два или более соединённых параллельно или последовательно электрических элементов. Обычно под этим термином подразумевается соединение электрохимических источников электроэнергии/электрического тока (гальванических элементов, аккумуляторов, топливных элементов). Батарейкой в обиходе обычно не совсем корректно называют одиночные гальванические элементы (например, типа АА), которые обычно в источниках питания устройств соединяются в батарею для получения необходимого напряжения.
Примеры батареек
Внутреннее устройство батарейки типа «Крона»
К лассификация батареек (элементов) по типу электролита
Электрический аккумулятор Электри́ческий аккумуля́тор — химический источник тока многоразового действия, который может быть вновь заряжен после разряда. Вторичный элемент, в процессе заряда функционирует как электролитическая ячейка (электролизер). В первичном элементе используется самопроизвольная химическая реакция. В электролизере электрическая энергия вызывает желаемую химическую реакцию. Перезарядка аккумулятора происходит путем пропускания тока внешнего источника. Многие реакции, используемые в гальванических (первичных) элементах непригодны для аккумуляторов даже в случае их обратимости, так как цикл разряд — заряд может изменить состояние электродов. Наибольшее распространение получили свинцовые и щелочные (железно-никелевые и кадмий-никелевые) аккумуляторы, также используются цинк-серебряные, цинк-воздушные и марганцевые. Два и более аккумулятора для повышения напряжения, тока, мощности или надежности могут быть гальванически соединены в аккумуляторную батарею.
Используется для циклического накопления энергии (через заряд-разряд) и автономного электропитания различных электротехнических устройств и оборудования, а также для обеспечения резервных источников энергии в медицине, производстве, транспорте и в других сферах. История Первый прообраз аккумулятора, который, в отличие от батареи Алессандро Вольты, можно было многократно заряжать, был создан в 1803 году Иоганном Вильгельмом Риттером.
Иога́нн Вильге́льм Ри́ттер (16 декабря 1776 — 23 января 1810) — немецкий химик, физик, философ-романтик.
Его аккумуляторная батарея представляла собой столб из пятидесяти медных кружочков, между которыми было проложено влажное сукно. После пропускания через данное устройство тока от вольтова столба оно само начинало вести себя как источник электричества. Параметры аккумулятора Ёмкость аккумулятора. За ёмкость аккумулятора чаще всего принимают количество электричества равное 1 Кл, при силе тока 1 А в течение 1 с, (при переводе времени в часы получаем 1 А*ч=3600 Кл). Как правило ёмкость аккумулятора приводится в Ампер*часах. Плотность энергии Плотность энергии — количество энергии на единицу объёма или единицу массы аккумулятора. Саморазряд Саморазряд — это потеря аккумулятором заряда после полной зарядки при отсутствии нагрузки. Саморазряд проявляется по-разному у разных типов аккумуляторов, но всегда максимален в первые часы после заряда, а после — замедляется. Температурный режим Следует беречь аккумуляторы от огня и воды, чрезмерного нагревания и охлаждения, резких перепадов температур. Не следует использовать аккумуляторы при температурах выше +50°С и ниже −25°С. При эксплуатации аккумулятора в условиях «холодной зимы» рекомендуется его снимать и хранить в тёплом помещении. Нарушение температурного режима может привести к сокращению срока службы или потере работоспособности аккумуляторов. Типы аккумуляторов Тип аккумулятора определяется используемыми материалами. В настоящее время разработаны несколько десятков видов аккумуляторов, использующих самые разные материалы и химические реакции. При ведём некоторые из них: Cn-Po — Графен-полимерный аккумулятор. La-Ft — лантан-фторидный аккумулятор Li-Ion — литий-ионный аккумулятор (3,2-4,2 V), общее обозначение для всех литиевых аккумуляторов Li-Co — литий-кобальтовый аккумулятор, (3,6 V), на базе LiCoO2, технология в процессе освоения Li-Po — литий-полимерный аккумулятор (3,7 V), полимер в качестве электролита Li-Ft — литий-фторный аккумулятор Li-Mn — литий-марганцевый аккумулятор (3,6 V) на базе LiMn2O4 LiFeP или LFP — Литий-железно-фосфатный аккумулятор (3,3 V) на базе LiFePO4 LiFeYPO4 — литий-железо-иттрий-фосфатный (Добавка иттрия для улучшения свойств) Li-Ti — литий-титанатный аккумулятор (3,2 V) на базе Li4Ti5О12 Li-Cl — литий-хлорный аккумулятор (3,99 V) Li-S — литий-серный аккумулятор (2,2 V)
LMPo — литий-металл-полимерный аккумулятор Fe-air — железо-воздушный аккумулятор Na/NiCl — никель-солевой аккумулятор (2,58 V) Na-S — натрий-серный аккумулятор, (2 V), высокотемпературный аккумулятор Ni-Cd — никель-кадмиевый аккумулятор (1,2 V) Ni-Fe — железо-никелевый аккумулятор (1,2-1,9 V) Ni-H2 — никель-водородный аккумулятор (1,5 V) Ni-MH — никель-металл-гидридный аккумулятор (1,2 V) Ni-Zn — никель-цинковый аккумулятор (1,65 V) Pb — свинцово-кислотный аккумулятор (2 V) Pb-H — свинцово-водородный аккумулятор Ag-Zn — серебряно-цинковый аккумулятор (1,85 V) Ag-Cd — серебряно-кадмиевый аккумулятор (1,6 V) Zn-Br — цинк-бромный аккумулятор (1,8 V) Zn-air — цинк-воздушный аккумулятор Zn-Cl — цинк-хлорный аккумулятор RAM (Rechargeable Alkaline Manganese) — перезаряжаемая разновидность марганцево-цинкового щелочного гальванического элемента (Ванадиевый аккумулятор (1,41 V) Алюминиево-графитный аккумулятор (2 V) Алюминиево-ионный аккумулятор (2 V) Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы:
Разновидности аккумуляторов
Автомобильный аккумулятор
Литиевые аккумуляторы Наиболее широко используемым видом литиевых аккумуляторов является литий -ионный аккумулятор. Литий-ионный аккумулятор (Li-ion) — тип электрического аккумулятора, который широко распространён в современной бытовой электронной технике и находит своё применение в качестве источника энергии в электромобилях и накопителях энергии в энергетических системах. Это самый популярный тип аккумуляторов в таких устройствах как сотовые телефоны, ноутбуки, цифровые фотоаппараты, видеокамеры и электромобили.
Литиевые аккумуляторы
История Впервые принципиальная возможность создания литиевых аккумуляторов на основе способности дисульфида титана или дисульфида молибдена включать в себя ионы лития при разряде аккумулятора и экстрагировать их при зарядке была показана в 1970 году Майклом Стэнли Уиттингемом. Существенным недостатком таких аккумуляторов являлось низкое напряжение - 2,3 В и высокая пожароопасность вследствие образования дендритов металлического лития, замыкающих электроды. Позднее Дж. Гуденафом были синтезированы другие материалы для катода литиевого аккумулятора - кобальтит лития LixCoO2(1980 год), феррофосфат лития LiFePO4 (1996 год). Преимуществом таких аккумуляторов является более высокое напряжение - около 4 В. Современный вариант литий-ионного аккумулятора с анодом из графита и катодом из кобальтита лития изобрёл в 1991 году Акира Ёсино. Первый литий-ионный аккумулятор по его патенту выпустила корпорация Sony в 1991 году. В настоящее время ведутся исследования по поиску материалов на основе кремния и фосфора, обеспечивающих повышенную ёмкость интеркалирования ионов лития и по замене ионов лития на ионы натрия. Уиттингем, Гуденаф и Ёсино получили Нобелевскую премию по химии в 2019 году с формулировкой «За создание литий-ионных батарей».
Джон Б Гуденаф, Майкл Стэнли Виттинхэм и Акира Ёсино - лауреаты Нобелевской премии по химии за изобретение литий-ионных батарей, 2019 год.
Преимущества Высокая энергетическая плотность (ёмкость). Низкий саморазряд. Высокая токоотдача. Большое число циклов заряд-разряд. Не требуют обслуживания. Недостатки Огнеопасны. Аккумуляторы Li-ion первого поколения были подвержены взрывному эффекту. Литий-ферро-фосфатные аккумуляторы полностью лишены этих недостатков. Кроме того, все современные зарядные устройства для литий-ионных аккумуляторов предотвращают перезаряд и перегрев вследствие слишком интенсивного заряда. Литиевые аккумуляторы изредка проявляют склонность к взрывному самовозгоранию. Интенсивность горения даже от миниатюрных аккумуляторов такова, что может приводить к тяжким последствиям. Авиакомпании и международные организации принимают меры к ограничению перевозок литиевых аккумуляторов и устройств с ними на авиатранспорте. Самовозгорание литиевого аккумулятора очень плохо поддаётся тушению традиционными средствами. В процессе термического разгона неисправного или повреждённого аккумулятора происходит не только выделение запасённой электрической энергии, но и ряд химических реакций, выделяющих вещества для поддержания горения, горючие газы от электролита, а также в случае не LiFePO4 электродов, выделяется кислород Вспыхнувший аккумулятор способен гореть без доступа воздуха и для его тушения непригодны средства изоляции от атмосферного кислорода. Более того, металлический литий активно реагирует с водой с образованием горючего газа водорода, потому тушение литиевых аккумуляторов водой эффективно только для тех видов аккумуляторов, где масса литиевого электрода невелика. В целом тушение загоревшегося литиевого аккумулятора неэффективно. Целью тушения может быть лишь снижение температуры аккумулятора и предотвращение распространения пламени.
Теряют работоспособность при переразряде. Если напряжение на аккумуляторе превысить всего на 4 %, он будет вдвое быстрее терять ёмкость от цикла к циклу. Глубокий разряд полностью выводит из строя литий-ионный аккумулятор. Теряют ёмкость на холоде. Как и в других типах аккумуляторов, разрядка в условиях низких температур приводит к снижению отдаваемой энергии, в особенности при температурах ниже 0 ⁰C. Так, снижение запаса отдаваемой энергии при понижении температуры от +20 ⁰C до +4 ⁰C приводит к уменьшению отдаваемой энергии на ~5-7 %, дальнейшее понижение температуры разрядки ниже 0 ⁰C приводит к потере отдаваемой энергии на десятки процентов Эффект памяти Под эффектом памяти понимается обратимая потеря ёмкости, имеющая место в некоторых типах электрических аккумуляторов при нарушении рекомендованного режима зарядки, в частности, при подзарядке не полностью разрядившегося аккумулятора. Название связано с внешним проявлением эффекта: аккумулятор как будто «помнит», что в предыдущие циклы работы его ёмкость не была использована полностью, и при разряде отдаёт ток только до «запомненной песочницы». Li-Ion аккумуляторы практически полностью избавлены от эффекта памяти. Старение. Литиевые аккумуляторы стареют, даже если не используются. Соответственно, нет смысла покупать аккумулятор «про запас» или чрезмерно увлекаться «экономией» его ресурса. Оптимальные условия хранения Li-ion-аккумуляторов достигаются при 40-процентном заряде от ёмкости аккумулятора и температуре 0…10 °C.
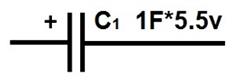
Изображение на схемах На электрических схемах ионисторы изображаются по типу электролитического конденсатора, и отличить его можно только по величине номинальных параметров.
Если, например, на схеме указана величина емкости 1 Фарада, то сразу ясно, что изображен ионистор, так как таких емких электролитических конденсаторов не бывает. Напряжение ультраконденсатора также может говорить об его отличии от электролитического конденсатора, так как обычно это незначительная величина в несколько вольт (от 1 до 5 В). Ионисторы не способны функционировать при большом напряжении. Преимущества · Если сравнивать ультраконденсаторы с аккумуляторами, то первые из них способны обеспечить значительно большее число циклов заряда и разряда. · Цикл заряда и разряда происходит за очень короткое время, что дает возможность применять их в таких ситуациях, когда нельзя установить аккумуляторы, ввиду их длительной зарядки. · Устройства такого вида имеют намного меньшую массу и габаритные размеры. · Для выполнения заряда не требуется специального зарядного устройства, что упрощает обслуживание. · Срок работы ультраконденсаторов значительно выше, по сравнению с батареями аккумуляторов и силовыми конденсаторами. · Широкий интервал эксплуатационной температуры от -40 до +70 градусов. Применение Ионисторы часто встречаются в устройстве цифрового оборудования. Они играют роль запасного источника питания микроконтроллера, микросхемы и т.д. С помощью такого источника при выключенном основном питании аппаратура способна сохранять настройки и обеспечивать питание встроенных часов. Например, в некоторых аудиоплеерах применяется миниатюрный ионистор. В момент замены батареек или аккумуляторов в плеере могут сбиться настройки частоты радиостанции, часов. Благодаря встроенному ионистору этого не происходит. Он питает электронную схему. Его емкость значительно меньше аккумулятора, но его хватает на несколько суток, чтобы сохранить работу часов и настроек. Также ультраконденсаторы используются для работы таймеров телевизора, микроволновой печи, сложного медицинского оборудования. Были случаи опытного использования ионисторов, например, для проектирования электромагнитной пушки, которую называют Гаусс - оружием. В быту ионисторы используются в схемах маломощных светодиодных фонариков. Его зарядка может выполняться от солнечных элементов. Популярным примером использования мощного ионистора можно назвать пусковое устройство для двигателя автомобиля.
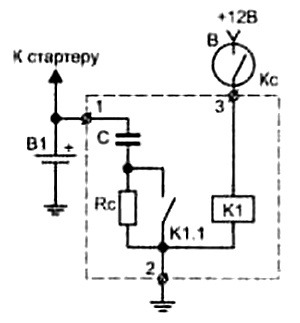
Эта схема выполняется на легковых автомобилях любой марки с напряжением сети 12 вольт.
· 1 – положительный контакт аккумуляторной батареи. · 2 – контакт массы (отрицательный полюс). · 3 – клемма замка зажигания. · В1 – аккумулятор. · Кс – замок зажигания. · К1 и К1.1 – контактор с ключом управления. · С – ионистор. · Rс – сопротивление для ограничения зарядного тока ионистора. В схеме применяется ионистор со следующими параметрами: · Максимальное напряжение 15 вольт. · Внутреннее сопротивление 0,0015 Ом. · Емкость 216 Фарад. · Рабочий ток 2000 ампер. Такого пускового устройства достаточно, чтобы запустить двигатель мощностью до 150 л. с. ионистор способен получить полный заряд за пять секунд. Такое устройство можно найти в продаже, но сделать его самостоятельно намного дешевле.
Топливные элементы Топливные элементы представляют собой очень эффективный, надежный, долговечный и экологически чистый способ получения энергии. Топливный элемент – это гальванический элемент, в котором химическая энергия топлива преобразуется электрохимическим путем в электрическую энергию. Топливо и окислитель при этом непрерывно и раздельно подводятся к ячейке, в которой они реагируют на двух электродах. Преимущества топливных элементов делают их пригодными для ряда интересных областей применения. Первоначально применявшиеся лишь в космической отрасли, в настоящее время топливные элементы все активней используются в самых разных областях — как стационарные электростанции, автономные источники тепло- и электроснабжения зданий, двигатели транспортных средств, источники питания ноутбуков и мобильных телефонов. Часть этих устройств является лабораторными прототипами, часть проходит предсерийные испытания или используется в демонстрационных целях, но многие модели выпускаются серийно и применяются в коммерческих проектах. В топливных элементах содержащаяся в топливе энергия при электрохимическом производстве энергии непосредственно преобразуется в электрическую. Исключается окольный, связанный с потерями путь через тепловую и механическую энергии. Солнечные батареи Солнечная батарея — объединение фотоэлектрических преобразователей (фотоэлементов) — полупроводниковых устройств, прямо преобразующих солнечную энергию в постоянный электрический ток, в отличие от солнечных коллекторов, производящих нагрев материала-теплоносителя.
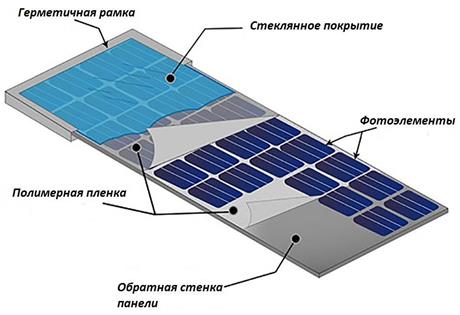
Устройство элемента солнечной батареи
Работа солнечных батарей основана на вентильном фотоэффекте в полупроводниках (фото–ЭДС на p–n переходе). Под действием света электроны переходят на более высокий энергетический уровень, поддерживая ток во внешней цепи.
Солнечная электростанция
В настоящее время наблюдается бум применений солнечных батарей в самых различных областях: электроснабжение домов, автомобилей, городов, солнечные батареи являются основным источником энергоснабжения космически станций и зондов, СБ используются даже в медицине путём вживления под кожу человека. В феврале 2017 года в нормандской деревне Tourouvre-au-Perche французским правительством была открыта дорога из солнечных батарей. Километровый участок дороги оборудован 2880 солнечными панелями. Такое дорожное покрытие обеспечит электроэнергией уличные фонари деревни. Панели каждый год будут вырабатывать 280 мегаватт час электроэнергии. Строительство отрезка дороги обошлось в 5 миллионов евро. Этот бум вызвал резким повышением к.п.д. солнечных батарей, который достиг для разных видов батарей 40 и даже 65 %! Использование солнечных батарей для энергоснабжения дома окупается в течении 5лет.
Наручные часы Citizen Eco-Drive с солнечной батареей вместо циферблата
Кроме того, потребителям в настоящее время разрешено продавать излишки электроэнергии в энергоснабжающие организации.
Солнечная батарея для снабжения дома
Области применения Радиоизотопные источники энергии применяются там, где необходимо обеспечить автономность работы оборудования, значительную надёжность, малый вес и габариты. В настоящее время основные области применения — это космос (спутники, межпланетные станции и др), глубоководные аппараты, удалённые территории (крайний север, открытое море, Антарктика). Например, изучение «глубокого космоса» без радиоизотопных генераторов невозможно, так как при значительном удалении от Солнца уровень солнечной энергии, который можно использовать посредством фотоэлементов, исчезающе мал. Например, на орбите Сатурна освещённость Солнцем в зените соответствует земным сумеркам. Кроме того, при значительном удалении от Земли для передачи радиосигналов с космического зонда требуется очень большая мощность. Существующие области применения: Энергообеспечение космических аппаратов (тепловая и электрическая энергия; список неполон): «Викинг-1 и −2» «Пионер» «Вояджер-1» «Вояджер-2» Луноходы Марсоходы Медицина: электропитание электрокардиостимуляторов и др. Энергопитание маяков и бакенов. Перспективные области применения: Роботы-андроиды: Электротеплопитание. Как основной источник энергии. Боевые лазеры космического базирования: Накачка лазеров и электротеплопитание. Боевые машины: Мощные двигатели с большим ресурсом (беспилотные разведывательные аппараты — самолёты и мини-лодки, энергопитание боевых вертолётов и самолётов, а также танков и автономных пусковых установок). Глубоководные гидроакустические станции: длительное энергопитание невозвращаемых аппаратов. ПЕРВИЧНЫЕ ИСТОЧНИКИ ЭЛЕКТРИЧЕСКОЙ ЭНЕРГИИ
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-01-14; просмотров: 254; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.252.201 (0.103 с.) |








 Пример размещения аккумулятора на шасси автомобиля
Пример размещения аккумулятора на шасси автомобиля