Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Элементы II группы главной подгруппыСтр 1 из 3Следующая ⇒
Элементы II группы главной подгруппы 1. Положение в Периодической системе химических элементов Оксиды щелочноземельных металлов Гидроксиды щелочноземельных металлов Соли щелочноземельных металлов
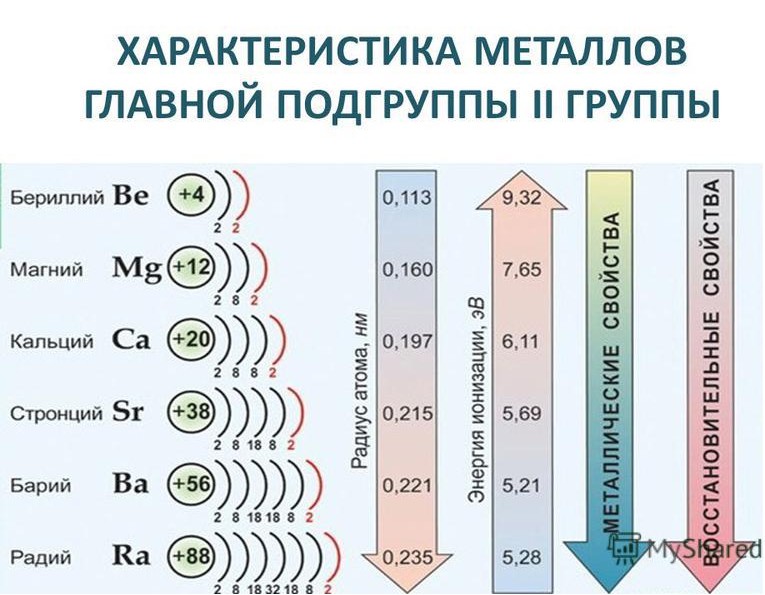
Элементы II группы главной подгруппы Положение в периодической системе химических элементов Щелочноземельные металлы расположены во второй группе главной подгруппе периодической системы химических элементов Д.И. Менделеева (или просто во 2 группе в длиннопериодной форме ПСХЭ). На практике к щелочноземельным металлам относят только кальций Ca, стронций Sr, барий Ba и радий Ra. Бериллий Be по свойствам больше похож на алюминий, магний Mg проявляет некоторые свойства щелочноземельных металлов, но в целом отличается от них. Однако, согласно номенклатуре ИЮПАК, щелочноземельными принято считать все металлы II группы главной подгруппы.
Электронное строение и закономерности изменения свойств Электронная конфигурация внешнего энергетического уровня щелочноземельных металлов: ns 2, на внешнем энергетическом уровне в основном состоянии находится 2 s -электрона. Следовательно, типичная степень окисления щелочноземельных металлов в соединениях +2. Рассмотрим некоторые закономерности изменения свойств щелочноземельных металлов. В ряду Be — Mg — Ca — Sr — Ba — Ra, в соответствии с Периодическим законом, увеличивается атомный радиус, усиливаются металлические свойства, ослабевают неметаллические свойства, уменьшается электроотрицательность.
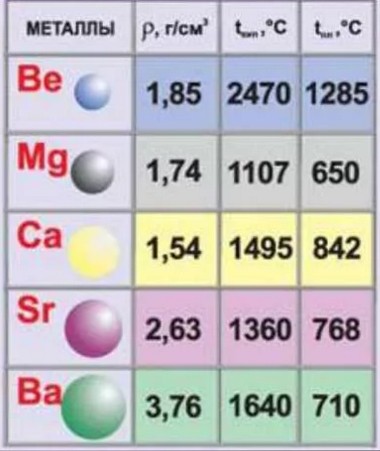
Физические свойства Все щелочноземельные металлы — вещества серого цвета и гораздо более твердые, чем щелочные металлы.
Бериллий Be устойчив на воздухе. Магний и кальций (Mg и Ca) устойчивы в сухом воздухе. Стронций Sr и барий Ba хранят под слоем керосина. Кристаллическая решетка щелочноземельных металлов в твёрдом состоянии — металлическая. Следовательно, они обладают высокой тепло- и электропроводимостью. Кипят и плавятся при высоких температурах.
Нахождение в природе Как правило, щелочноземельные металлы в природе присутствуют в виде минеральных солей: хлоридов, бромидов, йодидов, карбонатов, нитратов и др. Основные минералы, в которых присутствуют щелочноземельные металлы: Доломит — CaCO 3 · MgCO3 — карбонат кальция-магния.
Магнезит MgCO 3 – карбонат магния.
Кальцит CaCO 3 – карбонат кальция.
Гипс CaSO 4 · 2H 2 O – дигидрат сульфата кальция.
Барит BaSO 4 — сульфат бария.
Витерит BaCO 3– карбонат бария.
Способы получения Магний получают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С: MgCl 2 → Mg + Cl 2 или восстановлением прокаленного доломита в электропечах при 1200–1300°С: 2(CaO · MgO) + Si → 2Mg + Ca 2 SiO 4 Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция: CaCl 2 → Ca + Cl 2 Барий получают восстановлением оксида бария алюминием в вакууме при 1200 °C: 4BaO+ 2Al → 3Ba + Ba(AlO 2 ) 2 Качественные реакции Качественная реакция на щелочноземельные металлы — окрашивание пламени солями щелочноземельных металлов.
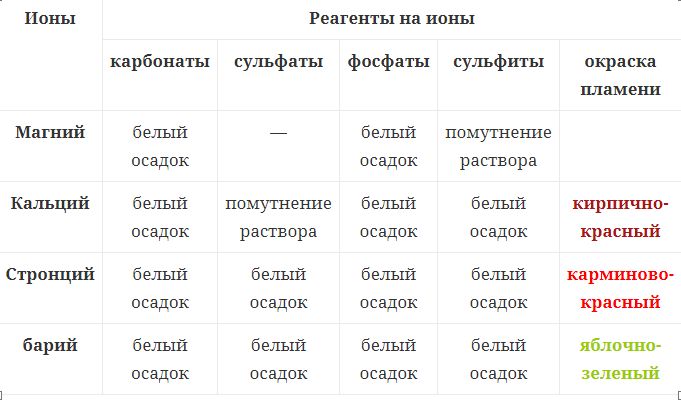
Цвет пламени: Качественная реакция на ионы магния: взаимодействие с щелочами. Ионы магния осаждаются щелочами с образованием белого осадка гидроксида магния: Mg 2+ + 2OH — → Mg(OH) 2 ↓
Качественная реакция на ионы кальция, стронция, бария: взаимодействие с карбонатами. При взаимодействии солей кальция, стронция и бария с карбонатами выпадает белый осадок карбоната кальция, стронция или бария: Ca 2+ + CO 32- → CaCO 3 ↓ Ba 2+ + CO 32- → BaCO 3 ↓
Качественная реакция на ионы стронция и бария: взаимодействие с карбонатами. При взаимодействии солей стронция и бария с сульфатами выпадает белый осадок сульфата бария и сульфата стронция: Ba 2+ + SO 42- → BaSO 4 ↓ Sr 2+ + SO 42- → SrSO 4 ↓
Также осадки белого цвета образуются при взаимодействии солей кальция, стронция и бария с сульфитами и фосфатами.
Например, при взаимодействии хлорида кальция с фосфатом натрия образуется белый осадок фосфата кальция: 3CaCl 2 + 2Na 3 PO 4 → 6NaCl + 2Ca 3 (PO 4 ) 2 ↓ Химические свойства 1. Щелочноземельные металлы — сильные восстановители. Поэтому они реагируют почти со всеми неметаллами. 1.1. Щелочноземельные металлы реагируют с галогенами с образованием галогенидов при нагревании. Например, бериллий взаимодействует с хлором с образованием хлорида бериллия: Be + Cl 2 → BeCl 2 1.2. Щелочноземельные металлы реагируют при нагревании с серой и фосфором с образованием сульфидов и фосфоридов. Например, кальций взаимодействует с серой при нагревании: Ca + S → CaS Кальций взаимодействует с фосфором с образованием фосфидов: 3Ca + 2P → Ca 3 P 2 1.3. Щелочноземельные металлы реагируют с водородом при нагревании. При этом образуются бинарные соединения — гидриды. Бериллий с водородом не взаимодействует, магний реагирует лишь при повышенном давлении. Mg + H 2 → MgH 2 1.4. С азотом магний взаимодействует при комнатной температуре с образованием нитрида: 6Mg + 2N 2 → 2Mg 3 N 2 Остальные щелочноземельные металлы реагируют с азотом при нагревании. 1.5. Щелочноземельные металлы реагируют с углеродом с образованием карбидов, преимущественно ацетиленидов. Например, кальций взаимодействует с углеродом с образованием карбида кальция: Ca + 2C → CaC 2 Бериллий реагирует с углеродом при нагревании с образованием карбида — метанида: 2Be + C → Be 2 C 1.6. Бериллий сгорает на воздухе при температуре около 900°С: 2Be + O 2 → 2BeO Магний горит на воздухе при 650°С с выделением большого количества света. При этом образуются оксиды и нитриды: 2Mg + O 2 → 2MgO 3Mg + N 2 → Mg 3 N 2
Горение кальция на воздухе Щелочноземельные металлы горят на воздухе при температуре около 500°С, в результате также образуются оксиды и нитриды. 2. Щелочноземельные металлы взаимодействуют со сложными веществами: 2.1. Щелочноземельные металлы реагируют с водой. Взаимодействие с водой приводит к образованию щелочи и водорода. Бериллий с водой не реагирует. Магний реагирует с водой при кипячении. Кальций, стронций и барий реагируют с водой при комнатной температуре. Например, кальций реагирует с водой с образованием гидроксида кальция и водорода: 2 Ca 0 + 2 H 2+ O = 2 Ca + (OH) 2 + H 20 2.2. Щелочноземельные металлы взаимодействуют с минеральными кислотами (с соляной, фосфорной, разбавленной серной кислотой и др.). При этом образуются соль и водород.
Например, магний реагирует с соляной кислотой: 2Mg + 2HCl → MgCl 2 + H 2 ↑ 2.3. При взаимодействии щелочноземельных металлов с концентрированной серной кислотой образуется сера. Например, при взаимодействии кальция с концентрированной серной кислотой образуется сульфат кальция, сера и вода: 4Ca + 5H 2 SO 4(конц.) → 4CaSO 4 + S + 5H 2 O 2.4. Щелочноземельные металлы реагируют с азотной кислотой. При взаимодействии кальция и магния с концентрированной или разбавленной азотной кислотой образуется оксид азота (I): 4Ca + 10HNO 3 (конц) → N 2 O + 4 С a(NO 3 ) 2 + 5H 2 O При взаимодействии щелочноземельных металлов с очень разбавленной азотной кислотой образуется нитрат аммония: 4Ba + 10HNO 3 → 4Ba(NO 3 ) 2 + NH 4 NO 3 + 3H 2 O 2.5. Щелочноземельные металлы могут восстанавливать некоторые неметаллы (кремний, бор, углерод) из оксидов. Например, при взаимодействии кальция с оксидом кремния (IV) образуются кремний и оксид кальция: 2Ca + SiO 2 → 2CaO + Si Магний горит в атмосфере углекислого газа. При этом образуется сажа и оксид магния: 2Mg + CO 2 → 2MgO + C 2.6. В расплаве щелочноземельные металлы могут вытеснять менее активные металлы из солей и оксидов. Обратите внимание! В растворе щелочноземельные металлы будут взаимодействовать с водой, а не с солями других металлов. Например, кальций вытесняет медь из расплава хлорида меди (II): Ca + CuCl 2 → CaCl 2 + Cu
Способы получения 1. Оксиды щелочноземельных металловможно получить из простых веществ — окислением металлов кислородом: 2Ca + O 2 → 2CaO 2. Оксиды щелочноземельных металлов можно получить термическим разложением некоторых кислородсодержащих солей — карбонатов, нитратов. Например, карбонат кальция разлагается на оксид кальция, оксид азота (IV) и кислород: 2Ca(NO 3 ) 2 → 2CaO + 4NO 2 + O 2 MgCO 3 → MgO + CO 2 СаСО 3 → СаО + СО 2 3. Оксиды магния и бериллия можно получить термическим разложением гидроксидов: Mg(OH) 2 → MgO + H 2 O Химические свойства Оксиды кальция, стронция, бария и магния— типичные основные оксиды. Вступают в реакции с кислотными и амфотерными оксидами, кислотами, водой. Оксид бериллия — амфотерный. 1. Оксиды кальция, стронция, бария и магния взаимодействуют с кислотными и амфотерными оксидами: Например, оксид магния взаимодействует с углекислым газом с образованием карбоната магния:
MgO + CO 2 → MgCO 3 2. Оксиды щелочноземельных металлов взаимодействуют с кислотами с образованием средних и кислых солей (с многоосновными кислотами). Например, оксид кальция взаимодействует с соляной кислотой с образованием хлорида кальция и воды: CaO + 2HCl → CaCl 2 + H 2 O 3. Оксиды кальция, стронция и бария активно взаимодействуют с водой с образованием щелочей. Например, оксид кальция взаимодействует с водой с образованием гидроксида кальция: CaO + H 2 O → 2Ca(OH) 2 Оксид магния реагирует с водой при нагревании: MgO + H 2 O → Mg(OH) 2 Оксид бериллия не взаимодействует с водой. 4. Оксид бериллия взаимодействует с щелочами и основными оксидами. При взаимодействии оксида бериллия с щелочами в расплаве или с основными оксидами образуются соли-бериллаты. Например, оксид натрия реагирует с оксидом бериллия с образованием бериллата натрия: Na 2 O + BeO → Na 2 BeO 2 Например, гидроксид натрия реагирует с оксидом бериллия в расплаве с образованием бериллата натрия: 2NaOH + BeO → Na 2 BeO 2 + H 2 O При взаимодействии оксида бериллия с щелочами в растворе образуются комплексные соли. Например, оксид бериллия реагирует с гидроксидом калия с растворе с образованием тетрагидроксобериллата калия: 2NaOH + BeO + H 2 O → Na 2 [Be(OH) 4 ]
Способы получения 1. Гидроксиды кальция, стронция и бария получают при взаимодействии соответствующих оксидов с водой. Например, оксид кальция (негашеная известь) при взаимодействии с водой образует гидроксид кальция (гашеная известь): CaO + H 2 O → Ca(OH) 2 Оксид магния взаимодействует с водой только при нагревании: MgO + H 2 O → Mg(OH) 2 2. Гидроксиды кальция, стронция и бария получают при взаимодействии соответствующих металлов с водой. Например, кальций реагирует с водой с образованием гидроксида кальция и водорода: 2Ca + 2H 2 O → 2Ca(OH) 2 + H 2 Магний взаимодействует с водой только при кипячении: 2Mg + 2H 2 O → 2Mg(OH) 2 + H 2 3. Гидроксиды кальция и магния можно получить при взаимодействии солей кальция и магния с щелочами. Например, нитрат кальция с гидроксидом калия образует нитрат калия и гидроксид кальция: Ca(NO 3 ) 2 + 2KOH → Ca(OH) 2 ↓ + 2KNO 3 Химические свойства 1. Гидроксиды кальция, стронция и бария реагируют с всеми кислотами (и сильными, и слабыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов. Гидроксид магния взаимодействует только с сильными кислотами. Например, гидроксид кальция с соляной кислотой реагирует с образованием хлорида кальция: Ca(OH) 2 + 2HCl → CaCl 2 + 2H 2 O 2. Гидроксиды щелочных металлов реагируют с кислотными оксидами. При этом образуются средние или кислые соли, в зависимости от соотношения реагентов. Например, гидроксид бария с углекислым газом реагирует с образованием карбонатов или гидрокарбонатов: Ba(OH) 2(избыток) + CO 2 → BaCO 3 + H 2 O Ba(OH) 2 + 2CO 2(избыток) → Ba(HCO 3 ) 2 3. Гидроксиды кальция, стронция и бария реагируют с амфотерными оксидами и гидроксидами. При этом в расплаве образуются средние соли, а в растворе комплексные соли.
Например, гидроксид бария с оксидом алюминия реагирует в расплаве с образованием алюминатов: Ba(OH) 2 + Al 2 O 3 → Ba(AlO 2 ) 2 + H 2 O в растворе образуется комплексная соль — тетрагидроксоалюминат: Ba(OH) 2 + Al 2 O 3 + 3H 2 O → Ba[Al(OH) 4 ] 2 4. Гидроксиды кальция, стронция и бария взаимодействуют с кислыми солями. При этом образуются средние соли, или менее кислые соли. Например: гидроксид кальция реагирует с гидрокарбонатом кальция с образованием карбоната кальция: Ca(OH) 2 + Ca(HCO 3 ) 2 → 2CaCO 3 + 2H 2 O 5. Гидроксиды кальция, стронция и бария взаимодействуют с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода). Взаимодействие щелочей с неметаллами подробно рассмотрено в статье про щелочные металлы. 6. Гидроксиды кальция, стронция и бариявзаимодействуют с амфотерными металлами, кроме железа и хрома. При этом в расплаве образуются соль и водород: Ca(OH) 2 + Zn → CaZnO 2 + H 2 В растворе образуются комплексная соль и водород: Ca(OH) 2 + 2Al + 6Н 2 О = Ca[Al(OH) 4 ] 2 + 3Н 2 7. Гидроксиды кальция, стронция и бариявступают в обменные реакции с растворимыми солями. Как правило, с этими гидроксидами реагируют растворимые соли тяжелых металлов (в ряду активности расположены правее алюминия), а также растворимые карбонаты, сульфиты, силикаты, и, для гидроксидов стронция и бария — растворимые сульфаты. Например, хлорид железа (II) реагирует с гидроксидом бария с образованием хлорида бария и осадка гидроксида железа (II): Ba(OH) 2 + FeCl 2 = BaCl 2 + Fe(OH) 2 ↓ Также с гидроксидами кальция, стронция и бариявзаимодействуют соли аммония. Например, при взаимодействии бромида аммония и гидроксида кальция образуются бромид кальция, аммиак и вода: 2NH 4 Cl + Ca(OH) 2 = 2NH 3 + 2H 2 O + CaCl 2 8. Гидроксид кальция разлагается при нагревании до 580оС, гидроксиды магния и бериллия разлагаются при нагревании: Mg(OH) 2 → MgO + H 2 O 9. Гидроксиды кальция, стронция и бария проявляют свойства сильных оснований. В воде практически полностью диссоциируют, образуя щелочную среду и меняя окраску индикаторов. Ba(OH) 2 ↔ Ba 2+ + 2OH — Гидроксид магния — нерастворимое основание. Гидроксид бериллия проявляет амфотерные свойства. 10. Гидроксид и бериллия взаимодействует с щелочами. В расплаве образуются соли бериллаты, а в растворе щелочей — комплексные соли. Например, гидроксид бериллия реагирует с расплавом гидроксида натрия: Be(OH) 2 + 2NaOH → Na 2 BeO 2 + 2H 2 O При взаимодействии гидроксида бериллия с избытком раствора щелочи образуется комплексная соль: Be(OH) 2 + 2NaOH → Na 2 [Be(OH) 4 ]
Жесткость воды Элементы II группы главной подгруппы 1. Положение в Периодической системе химических элементов Оксиды щелочноземельных металлов Гидроксиды щелочноземельных металлов Соли щелочноземельных металлов
|
|||||||||
|
Последнее изменение этой страницы: 2020-11-28; просмотров: 245; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.12.172 (0.139 с.) |