
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Расчет рабочего цикла двигателя
Процесс впуска Давление впуска в начале сжатия определяется по формуле:
Pа=(1-δn) Pn (Н/м2).
Где: δn – относительная потеря давления из-за сопротивления впуску Pn – давление наддува Pa=(1–0.10)*1.4=0.95*1.4=1.33 Н/м2 Определяем величину нагрева воздуха в турбокомпрессоре:
Где: n – показатель политропы сжатия компрессора To – температура окружающей среды Рn – давление наддува Ро - атмосферное давление
Определяем температуру в начале сжатия по формуле:
Ta=(To+γrTr)/1+γr Найдем температуру свежего заряда с учетом подогревания его от стенок:
To=To+ΔT+ΔT1
T1o=293+6+81=380 К Подставив значение в формулу получим:
Температура наддува воздуха равна:
Tн=То-ΔТ
Tн=380–10=370 К
Определяем коэффициент наполнения:
Процесс сжатия Основные параметры состояния газа в начале сжатия Ра и Та определены. Процесс сжатия протекает по политропе, и для простоты расчета цикла полагают, что политропа имеет средний постоянный показатель. Найдем параметры состояния газа по окончании процесса сжатия Рс и Тс. Давление в конце сжатия:
Где: Ра-давление начала сжатия ε-степень сжатия n1-показатель политропы сжатия Рс= 1,26*13,31,36 =38 кгс/см2 Температура в конце сжатия определяется по формуле:
Где: Та-температура в начале сжатия. Тс=380*13,31,36-1=380*2,5=890 К
Процесс сгорания Самовоспламенение и сгорание топлива сложный процесс химического соединения его горючих элементов с кислородом воздуха, сопровождаемый выделением теплоты. При расчете процесса сгорания рассчитывают давление в конце сгорания Рz и температуру в конце сгорания Тz. Давление в конце сгорания рассчитывают по формуле:
Рz=λ*Pc, кгс/см2
Где: λ – степень повышения давления, берется по справочным данным и колеблется в пределах от 1,4 до 2,2. Произведем расчет давления конца сгорания: Рz=1.6*38=60.8 кгс/см2 Температуру конца сгорания определяют путем решения уравнения сгорания:
Где: β – коэффициент молекулярного изменения λ – степень повышения давления при сгорании ξ – коэффициент использования теплоты при сгорании Qн – низкая теплота сгорания топлива М1 – количество газа в начале горения
Рассчитаем все составляющие уравнения. Расчеты будем вести в системе единиц измерения СИ. Найдем количество газов в начале сгорания М1, по формуле:
М1=0,5α (1+γr), КМоль/кг
Где: α – коэффициент избытка воздуха и для данного дизеля колеблется в пределах от 1,5 до 1,7. Произведем расчет количества газов в начале сгорания: М1=0,5*1,5 (1+0,04)=0,78 КМоль/кг Найдем количества продуктов сгорания М2 по формуле: М2= М1+0,03 КМоль/кг Произведем расчет количества продуктов сгорания: М2=0.78+0.03=0.81 КМоль/кг Найдем коэффициент молекулярного изменения β по формуле: β= М2/ М1
Произведем расчет коэффициента молекулярного изменения: β= Найдем степень повышения давления по формуле:
Произведем расчет степени повышения давления:
По справочным данным коэффициент использования теплоты при сгорании ζ колеблется в пределах от 0,8 до 0,85, а низкая теплота сгорания топлива Qн равна 42000 кДж/кг. Среднюю молярную изохорную теплоемкость свежего заряда
Рассчитаем
Средняя молярная изобарная теплоемкость продуктов сгорания
Примем температуру конца сжатия Тz считается неизвестной. Тогда выразим через Тz величину
Подставив это выражение в выше указанное уравнение сгорания получим полное квадратное уравнение относительно Тz. Решив его получим температуру конца сгорания Тz: 29,252 Тz+0,0309 Тz2=31508,136+43076,923 0,0309 Тz2-29,252 Тz-74585,059=0 Д=855,6795+4*0,0309*74585,059=10074,39279 Тz= Процесс расширения При расширении газа совершается полезная работа. Процесс происходит по политропе с показаниями n2, который для тихоходных двигателей равен 1,24–1,30, а для быстроходных 1,20–1,25. Давление газа в конце расширения рассчитывается по формуле:
Произведем расчет давления газа в конце расширения:
Температура газа в конце расширения рассчитывается по формуле:
Произведем расчет температуры газа в конце расширения:
Выпуск Давление газов в цилиндре за период выпуска не остается постоянным и зависит от проходного сечения выпускного канала, сопротивления выпускного трубопровода. Колебание давления газов при выпуске не поддаются точному теоретическому подсчету, поэтому используют среднее постоянное давление газов в период выпуска. Вывод: расчетные числовые значения давлений и температур не выходят за пределы полученных опытным путем для рабочего цикла ДВС.
|
||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 61; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.204.208 (0.014 с.) |
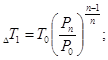
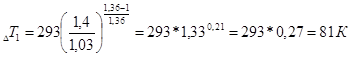
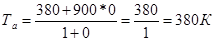
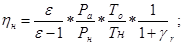
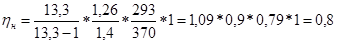

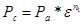
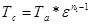
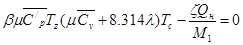
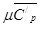 -средняя малярная изобарная теплоемкость продуктов сгорания
-средняя малярная изобарная теплоемкость продуктов сгорания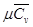 -средняя малярная изохорная теплоемкость свежего заряда
-средняя малярная изохорная теплоемкость свежего заряда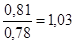
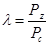
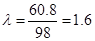
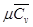 рассчитывается по следующей эмпирической формуле:
рассчитывается по следующей эмпирической формуле: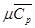 рассчитывается по следующей эмпирической формуле:
рассчитывается по следующей эмпирической формуле: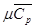 =
= 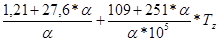 кДж/(кМоль*К)
кДж/(кМоль*К)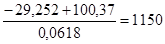
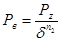 , кгс/см2
, кгс/см2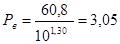 Кгс/см2
Кгс/см2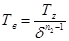 , К
, К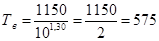 К
К


