Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Раздел 1 источники тепловой энергииСодержание книги
Поиск на нашем сайте
Тема 1.1 Топливо и его сжигание ТОПЛИВО – это группа веществ, которая при нагревании в присутствии кислорода активно окисляется (сгорает) с выделением значительного количества тепла. Топливо – это основной источник тепловой энергии для металлургических печей.
Таблица 1-Классификация топлива
Топливо обычно имеет органическое происхождение, поэтому основными его составляющими являются углерод и водород, которые находятся в топливе в виде различных соединений. В состав топлива обычно входят кислород, азот, сера. Кроме того, в топливе всегда участвуют зола (А) и вода (W).
Химический состав топлива: C H O N S A W.
C - наиболее важная составляющая часть топлива. Основное количество тепла выделяется при сгорании углерода: C + O2 = CO2↑. Углерод в топливе содержится в количестве 80 – 90 %. H – важная часть топлива, но присутствует в меньшем количестве. Теплота сгорания его больше (выше) чем у углерода. О – содержится в твердом и жидком топливе в связанном состоянии (0,5 – 2%) N – содержится в топливе в незначительном количестве. При горении он не окисляется, а переходит в дымовые газы в виде свободного азота. S – в топливе находится в виде органических соединений (сульфидов, сульфатов). При горении серы выделяется значительное тепло. Содержание серы в топливе нежелательно вследствие загрязнения атмосферы и изделий сернистыми продуктами. А – твердый, негорючий остаток, получаемый после полного сжигания топлива. Является баластом, снижает его ценность и качество. W – является баластом топлива, снижающим качество топлива, поэтому в ряде случаев топливо сушат. Различают внешнюю влагу, которую удаляют при сушке без подогрева (воздушная сушка), и внутреннюю влагу (гигроскопическая), удаляемую при нагреве до 100°. Незначительное количество влаги в топливе полезно – это ускоряет процесс горения. Технический анализ При приеме топлива обычно производится его технический анализ на содержание влаги, золы и летучих соединений, а также оценка внешнего вида твердого остатка после проводимой в процессе анализа сухой перегонки топлива. Сухой перегонкой называется нагрев топлива без доступа воздуха, в результате которого топливо разлагается на летучие и твердый остаток – кокс. Химический анализ Химический анализ топлива можно выполнять как по элементарному составу (1),так и путем определения содержания в топливе определенных химических соединений (2). (1) – для твердого и жидкого топлива. (2) – для газообразного топлива. Метод Элементарным анализом находят содержание основных элементов (C, H, N, S; W, A) в процентах, причём кислород определяют по разности вычитанием из 100% всех основных компонентов: O = 100 – (C +H + N + S + W + A). На практике обычно пользуются другим выражением: C + H +О + N + S + W + A = 100%. C + H + O + N – органическая масса топлива «О». C + H + O + N + S – горючая масса топлива «Г». C + H + O + N + S + A – сухая масса топлива «С». C + H + O + N + S + A + W – рабочая масса топлива «Р». Для пересчета состава топлива из одной массы в другую будем пользоваться таблицей 2. Таблица 2
Задача. Определить состав рабочего топлива по заданному его элементарному составу. Дано: Со = 80%; Оо = 9%; Но = 8%; No = 3%; Sc = 1,5%; Ac = 10%; WP = 2%. Найти: рабочую массу топлива (р.м.т.). Решение: Так как нужно определить состав рабочего топлива → определим содержание S и A в р.т.:
Проверка: С + H + O + N + S + A + W =100%; 69,384 + 6,9384 + 7,8057 + 2,6019 + 1,47 + 9,8 + 2 = 100(%). Ответ: рабочая масса топлива =100%.
Задача 2. Дано: Сг = 89%; Ог = 2%; Нг = 4%; Nг = 2%; Sг = 3%; Ac = 10%; WP = 12%. Найти: р.м.т. Решение: Так как нужно определить состав р.т. → определим содержание S и A в р.т:
Проверка: С + H + O + N + S + A + W =100%; 70,488 + 3,168 + 1,584 + 1,584 + 2,376 + 8,8 + 12 = 100%. Ответ: рабочая масса топлива =100%.
Метод Второй метод анализа предназначен для газообразного топлива. Газообразное топливо состоит из смеси газообразных соединений: CO2; H2; CH4; C2H4; CmHn; H2S; CO; H2O; N2 и других.
Содержание перечисленных составляющих в объемных долях процента определяются специальным газовым анализом:
N2 = 100 – (CO2 + CO + H2 + CmHn + …).
Для пересчета рабочего топлива следует содержание влаги (г/см3) пересчитать на объем при нормальных условиях, приходящихся на 100 м3 сухого газа по формуле:
Если состав сухого газа:
COc2 + COc + Hc2 + CHc4 + CmHnc + Nc2 + Oc2 = 100% ,
то состав влажного газа (р.м.т.) в объемных процентах определяется по формулам:
Задача 1. Дано: Найти: р.м.т. Решение:
Проверка:
81,45 + 1,81 + 2,715 + 2,2625 + 2,2625 + 9,554 = 100,054» 100%. Ответ: рабочая масса топлива 100%.
Задача 2. Дано: Найти: р.м.т. Решение:
Проверка:
77,3177 + 2,72886 + 3,63848 + 2,27405 + 5,00291 + 9,04176 = 100,004» 100%. Ответ: рабочая масса топлива 100%. Тема 1.2 Методы определения теплоты сгорания
Теплота сгорания топлива – это количество тепла, выделяющееся при сжигании одной единицы топлива. [кДж/кг] – твердое, жидкое топливо; [кДж/м3] – газообразное топливо. Различают высшую и низшую теплоты сгорания топлива:
Для нагрева 1кг воды требуется 2516 кДж. Разность между
Если W1 и H выражены в процентах, то уравнение принимает вид:
При расчете теплоты сгорания топлива наилучшие результаты дает формула Д.И.Менделеева, принятая для всех видов твердого и жидкого топлива:
Теплоту сгорания газа можно определить по следующей формуле:
Для сравнения различных видов топлива введено понятие условного топлива. Условное топливо – топливо, теплота сгорания которого 29,3МДж/кг (это теплота сгорания донецкого каменного угля). Тепловой эквивалент топлива – это величина, полученная в результате деления низшей теплоты сгорания топлива на теплоту сгорания условного топлива.
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 139; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.006 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||


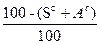
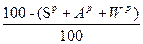
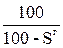

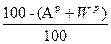
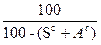



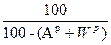
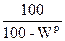
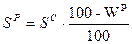 Þ
Þ 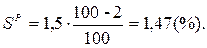
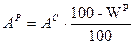 Þ
Þ 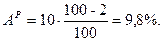

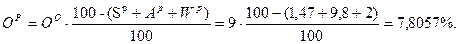


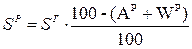 Þ
Þ 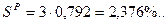
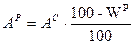 Þ
Þ 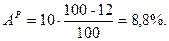


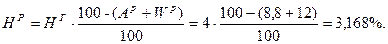
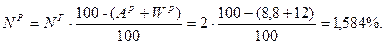
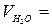 0, 1242 ∙W, (м3).
0, 1242 ∙W, (м3).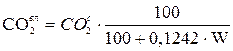 ;
;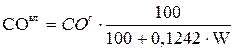 ;
;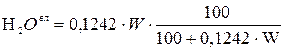 .
.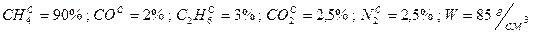 .
.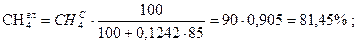


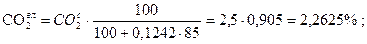
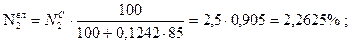

 .
.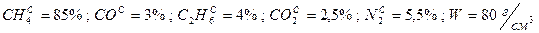 .
.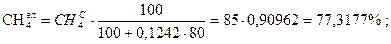
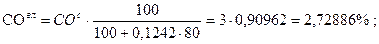


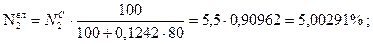
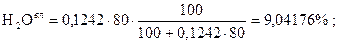
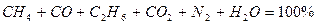
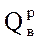 ,
, 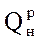 .
.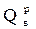 и
и  сгорания на 1кг рабочего топлива составляет:
сгорания на 1кг рабочего топлива составляет: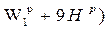 .
.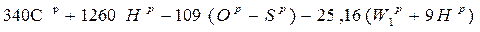
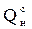 =
=