
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основы молекулярно-кинетической теории.Стр 1 из 3Следующая ⇒
ГАЗОВЫЕ ЗАКОНЫ Методические указания И особенности решения задач При решении задач на эту тему рекомендуется: – установить, какие тела входят в рассматриваемую термодинамическую систему, а также выяснить, что является причиной изменения внутренней энергии тел системы; – в случае адиабатически изолированной замкнутой системы следует установить, у каких тел системы внутренняя энергия увеличивается, а у каких уменьшается; – выяснить, происходят ли в системе тел фазовые переходы (испарение или конденсация, плавление или кристаллизация). При этом полезно использовать график зависимости изменения температуры тел от количества теплоты, полученной или отданной при теплообмене – составить уравнение теплового баланса – при рассмотрении процессов, в которых происходит теплообмен с окружающей средой и совершается механическая работа, Q – количество теплоты, сообщенное системе, DU – изменение ее внутренней энергии, А – работа, совершаемая системой. Задачи для самостоятельного решения 1.1. При нагревании на 7 К внутренняя энергия одноатомного идеального газа увеличилась на 348,6 Дж. Определить количество вещества. Ответ: 4.
1.2. Внутренняя энергия одноатомного идеального газа, находящегося в баллоне объемом 0,02 м3, равна 600 Дж. Определить в килопаскалях давление газа. Ответ: 20.
1.3. На сколько кельвинов следует нагреть 6 моль идеального газа, чтобы он совершил работу, равную 124,5 Дж? Давление газа постоянно. Ответ: 2,5.
1.4. При изобарическом нагревании от 300 К до 350 К газ совершил работу 100 Дж. Какую работу совершил газ при дальнейшем изобарическом нагревании на 25 К? Давление и масса газа постоянны. Ответ: 50.
1.5. Идеальный газ нагрели на 20 К при постоянном давлении и газ совершил работу 249 Дж. Сколько молей газа нагревали? Ответ: 1,5. ОСНОВЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ. ГАЗОВЫЕ ЗАКОНЫ Методические указания и Особенности решения задач
При решении задач на эту тему рекомендуется: – использовать уравнение Менделеева-Клапейрона, если состояние газа не меняется. Если при этом давление Р и объем газа V не заданы, то их следует выразить через величины, заданные в условии задачи; – если в задаче рассматривается несколько состояний газа, то параметры этих состояний обозначают следующим образом: 1-е состояние – m 1, P 1, V 1, T 1; 2-е состояние – m 2, P 2, V 2, T 2 и т.д., а затем используют для каждого из состояний уравнение Менделеева-Клапейрона (если масса газа m изменяется) или уравнение Клапейрона – если один из параметров газа остается постоянным и масса газа не меняется, то используют один из законов идеального газа: Бойля-Мариотта (T =const), Гей-Люссака (при Р =const) и Шарля (при V =const); – при решении задач, в которых рассматриваются процессы, связанные с изменением состояний нескольких газов все выше названные действия следует проделать для каждого газа отдельно; – решить полученные уравнения (дополненные в случае необходимости другими соотношениями, которые следуют из условия задачи) и найти искомые величины. Задачи для самостоятельного решения 1.1. В равных объемах при одинаковой температуре давление гелия 5 Па, кислорода 13 Па. Какое давление смеси, если гелий перекачать в объем, занимаемый кислородом? Ответ: 18
1.2. В 0,036 м3 содержится 5,1 киломоль углерода. Найти его плотность, если молярная масса углерода равна 12 г/моль. Ответ: 1700.
1.3. Во сколько раз возрастет плотность идеального газа при увеличении давления от 100 кПа до 140 кПа в ходе изотермического процесса? Ответ: 1,4. 1.4. Во сколько раз возрастет число молекул идеального газа в единице объема, если в ходе изотермического сжатия давление увеличивается в 2,5 раза? Ответ: 2,5.
1.5. При изотермическом сжатии давление газа возросло в 8 раз. Чему равен начальный объем газа, если в конце процесса газ занимал 0,24 м3? Ответ: 1,92. КОЛЕБАНИЯ И ВОЛНЫ
|
|||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 270; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.182.179 (0.004 с.) |
 ;
; при этом следует помнить, что в эту сумму слагаемые, соответствующие теплоте плавления твердых тел или теплоте парообразования жидкостей, входят со знаком «+», а слагаемые, соответствующие теплоте кристаллизации твердых тел или теплоте конденсации пара, – со знаком «-».
при этом следует помнить, что в эту сумму слагаемые, соответствующие теплоте плавления твердых тел или теплоте парообразования жидкостей, входят со знаком «+», а слагаемые, соответствующие теплоте кристаллизации твердых тел или теплоте конденсации пара, – со знаком «-».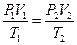 (если масса газа не изменяется);
(если масса газа не изменяется);


