
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Обробка експериментальних даних
5.1. Результати вимірів записуються у табл. 1.1. Т а б л и ц я 1.1.
5.2. Кількість теплоти, яка підводиться до повітря у процесі, Вт Qe = U ×I × x де х= 0,9 – коефіцієнт втрати теплоти у навколишнє середовище. 5.3. Масова витрата повітря, кг/с
де А = 2,2×10-4 – витратна характеристика повітропроводу; r = 1000 кг/м3 – густина води у дифманометрі, кг/м3. 5.4. Масова ізобарна середня теплоємність, Дж/кг×К
5.5. Масова ізохорна середня теплоємність визначається з рівняння Майєра, Дж/(кг×К) сvm = cpm - R де R = 287 Дж/(кг×К) - газова стала повітря. 5.6. Показник адіабати k = cpm / с vm. 5.7. Об’ємна ізобарна середня теплоємність, Дж/(м3×К) с’pm = cpm ×rв, де r в = 1,293 кг/м3 – густина повітря, кг/м3. 5.8. Мольна ізобарна середня теплоємність, Дж/(кмоль×К) mcрm = c ¢ pm × 22,4 де 22,4 м3/кмоль – об’єм одного кмоля повітря при нормальних умовах. 5.9. Об’ємна ізохорна середня та мольна ізохорна середня теплоємності
5.10. Розраховані значення теплоємностей заносять у табл. 1.2. Т а б л и ц я 1.2.
5.11. Робота ізобарного процесу, Дж/с L = m×R(tk – t п ) 5.12. Зміна внутрішньої енергії, Дж/с DU =Qe – L 5.13. Зміна ентальпії, Дж/с DІ = cpm×m×(tk – t п ) 5.14. Зміна ентропії, Дж/(с×К) DS = cpm×m×lnTk/T п 5.15. Визначається похибка досліду, для чого проводиться порівняння експериментальної теплоємності повітря з табличним значенням теплоємності. Табличне значення теплоємності розраховується за інтерполяційною формулою
де
` t = 0,5(t п + t к) – середньоарифметична температура досліду. Відносна похибка досліду
5.16. Результати розрахунків параметрів ізобарного процесу та відносної похибки заносяться у табл. 1.3.
Т а б л и ц я 1.3.
5.17. Висновки по роботі – пишуться на основі порівняння табличної та експериментальної теплоємності.
ФОРМА ПОДАННЯ ЗВІТУ Звіт по лабораторній роботі подається на подвійному аркуші учнівського зошиту. На першій сторінці оформлюється титульний лист. На інших сторінках розміщається: 1. Мета та задача роботи 2. Схема установки та короткий опис її роботи 3. Таблиця 1.1 – вимірювання дослідних даних 4. Таблиця 1.2 – розрахункових значень теплоємності 5. Таблиця 1.3 – розрахункових значень параметрів ізобарного процесу та похибки досліду 6. Висновки по роботі Звіт складається та пред’являється студентом до захисту індивідуально.
КОНТРОЛЬНІ ПИТАННЯ ДЛЯ САМОПЕРЕВІРКИ 7.1. Ціль та задачі роботи. 7.2. Дати визначення масової, мольної та об’ємної теплоємності. 7.3. Взаємозв’язок між видами теплоємності. 7.4. Середня та істина теплоємності. 7.5. Ізобарна та ізохорна теплоємності. 7.6. Рівняння Майєра. 7.7. Формула для визначення середньої масової ізобарної теплоємності. 7.8. Схема лабораторної установки та її робота. 7.9. Визначення витрати повітря. 7.10. Порядок проведення роботи. 7.11. Обробка експериментальних даних. 7.12. Розрахунок параметрів ізобарного процесу. 7.13. Звужуючий пристрій та проточний калориметр.
Л І Т Е Р А Т У Р А 8.1. Кириллин В.А., Сычев В.В., Шейндлин А.Е. Техническая термодинамика. - М.: Наука, 1979. - 512 с. 8.2. Нащекин В.В. Техническая термодинамика и теплопередача. - М.: Высшая школа, 1960. - 469 с. 8.3. Кириллин В.А., Шейндлин А.Е. Основы экспериментальной термодинамики. - М.: Наука, 1967. 8.4. Преображенский В.П. Теплотехнические измерения и приборы. - М.: Энергия, 1976. - 704 с. 8.5. Андрианова Т.Н., Дзампов Б.В., Зубарев В.Н., Ремизов С.А. Сборник задач по технической термодинамике. - М.: Энергоиздат, 1981. - 240 с. 8.6. Рабинович О.М. Сборник задач по технической термодинамике. - М.: Машиностроение, 1973. - 344 с. Лабораторна робота № 2 ПОБУДОВА ПРОЦЕСІВ ВОДЯНОЇ ПАРИ В І-S ДІАГРАМІ
МЕТА І ЗАДАЧА РОБОТИ Мета роботи – отримання практичних навичок роботи з і-s діаграмою. Задача роботи – побудова і розрахунок термодинамічних процесів водяної пари в і-s діаграмі.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 118; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.26.176 (0.011 с.) |




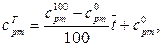
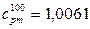 кДж/(кг×К) – табличне значення теплоємності при 100 оС.
кДж/(кг×К) – табличне значення теплоємності при 100 оС. кДж/(кг×К) – табличне значення теплоємності при 0 оС.
кДж/(кг×К) – табличне значення теплоємності при 0 оС. .
.


