
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тепловой эффект реакции взрыва. Закон Гесса
В инженерной практике определение теплового эффекта реакции взрывчатого превращения производят в соответствии с первым началом (законом) термодинамики и важнейшим законом термохимии - законом Гесса. Согласно первому началу термодинамики вся теплота, сообщенная системе, расходуется на изменение внутренней энергии системы, а также на совершение работы системой: Q=DU+А или dQ=dU+dА где U – внутренняя энергия; А – работа. Для случая изобарного процесса (при постоянстве давления Р=const) это уравнение, определяющее тепловой эффект реакции взрыва QP, примет вид: dQP=dU+PdV=d(U+PV) или dQP=dН где величина Н=U+PV называется энтальпией. Энтальпия является функцией состояния системы и определяется ее параметрами. В случае изохорного процесса (при постоянстве объёма V=const) тепловой эффект реакции взрыва равен dQv=dU или Qv=DU(298)=DН(298)-Sn·R·298 где Sn – сумма стехиометрических коэффициентов при газовых компонентах в уравнении реакции взрыва; R=8,31 Дж/(моль·К) – универсальная газовая постоянная. Для реакций, протекающих в изотермических условиях (при постоянстве температуры Т=const), тепловой эффект вычисляют в соответствии с законом Гесса DrH0298=[ånкон(DfH0298)кон-ånисх(DfH0298)исх] где: DfН0298 – стандартные энтальпии образования исходных и конечных веществ (индекс f означает формирование, а r - реакцию), т.е. энтальпии реакции образования 1 моль этих веществ из простых веществ, взятые в форме, устойчивой при нормальных условиях (Р0=101,3 кПа; Т0=298К). Размерность их следующая: кДж/моль или ккал/моль (в более поздней литературе). Эти величины приводятся в справочниках физико-химических величин (см. приложение); n – стехиометрические коэффициенты в реакции. В настоящее время помимо термодинамической системы знаков существует термохимическая система знаков теплоты и работы. Согласно последней тепловой эффект Q противоположен по знаку изменению энтальпий реакции DrH0298: Q= -DrH0298, кДж/моль или Q= -DrH0298·n, кДж где n – число молей вещества. Таким образом, если величина DrH0298<0, то реакция протекает с тепловыделением (+Q, -DH), и, наоборот, в случае, когда DrH0298>0, реакция протекает с теплопоглощением (-Q, +DH). Как следует из закона Гесса, суммарный тепловой эффект некоторой последовательности химических реакций не зависит от пути превращения исходных веществ в конечные продукты, а определяется только начальным и конечным состоянием системы:
Qр=åQпв–Qвв, (1.24) где Qр - теплота взрывчатого превращения; Qвв, åQпв - теплота образования ВВ и сумма теплот образования продуктов взрыва соответственно. В общем виде Закон Гесса можно сформулировать следующим образом: тепловой эффект кругового процесса равен нулю. При вычислении теплоты образования ВВ обычно рассматривают такие три составляющие системы, рис.14, как взрывчатое вещество (1), продукты взрыва (2) и свободные молекулы химических элементов (3).
Рис.14 Схематическое изображение закона Гесса.
При переходе (1)-->(2) выделится тепло, равное теплоте полного сгорания – Qвв. В случае перехода (2)-->(3) произойдет поглощение тепла, равное сумме теплот образования ПВ – åQпв. Так как переход (3)-->(1) соответствует процессу образования молекул ВВ, то теплота этого процесса равна теплоте взрывчатого превращения - Qр. Таким образом, в качестве теплоты взрывчатого превращения (Qр=Qвзр) рассматривают количество тепла, выделяемое при взрывчатом превращении одного моля вещества. Теплотой образования вещества (Qобр=-DfH0298) называют количество тепла, которое выделяется или поглощается при образовании одного моля вещества из молекул газов соответствующих элементов (Н2, О2, N2 и т.д.) и простых веществ (С, металл и т.д.). При этом реакции образования могут быть как реальными
так и виртуальными (пример - реакция образования тротила):
В общем виде виртуальная реакция образования ВВ брутто-формулы СaНbОcNd записывается следующим образом: a·СТВ+(b/2)·Н2+(c/2)·О2+ (d/2)·N2 ---> СaНbОcNd+Qобр Теплоту образования ВВ Qвв в прямом эксперименте определить невозможно. Величину Qвв рассчитывают с учетом экспериментально найденной стандартной теплоты сгорания данного вещества. Стандартная теплота сгорания вещества - это количество тепла, выделяющееся при сгорании одного моля вещества в атмосфере избытка кислорода при условии, что углерод и водород образуют при этом высшие оксиды (СО2, Н2О). Для ВВ формулы СaНbОcNd реакция сгорания в избытке кислорода может быть представлена следующим образом:
СaНbОcNd+[a+(b/4)+(c/2)]O2 ---> aCO2 +(b/2)H2O( l )+(d/2)N2+Qсгор. Для бризантных ВВ допустимы небольшие ошибки при оценке Qобр, так как окончательная приемка ВВ производится по натурным испытаниям зарядов: бризантность, разрушение преград, метательные действия, работоспособность и т.д. В таблице приложения П-1 приведены стандартные энтальпии образования DfН0298 некоторых индивидуальных ВВ, горючих, окислителей и продуктов некоторых реакций взрыва, а в таблицах П-2 и П-3 - контрольные задания.
Примеры расчета тепловых эффектов реакций Взрывчатых превращений Пример 1. Рассчитать тепловой эффект реакции взрывчатого превращения 320 г дымного пороха следующего состава: 75% KNO3, 15% С и 10% S. Решение. Реакция горения дымного пороха, состоящего из указанных компонентов, имеет вид: 2,38KNO3(s)+4C(s)+S(s)=1,19K2O(s)+SO2(g)+3,95CO(g)+0,05C(s)+1,19N2(g), где 2,38= 1= Дальнейший расчет удобнее производить при помощи таблицы.
Примечание: индексы (s) и (g) у веществ обозначают их агрегатное состояние (твердое и газообразное). Следует учитывать, что величины DfН0298 для простых веществ равны нулю (например, для С, S и N2 в данном примере).
Найдём по закону Гесса тепловой эффект реакции для 1 моль ВВ: DrH0298=ånкон(DfH0298)кон-ånисх(DfH0298)исх=[-361,5·1,19+(-296,9·1)+ +(-110,5·3,95)+0·0,05+0·1,19]-[(-492,5·2,38)+0·4+0·1]=8,59 кДж/моль. Для расчета теплового эффекта рассматриваемой реакции горения 320г дымного пороха необходимо определить количество моль вещества, содержащееся в указанной массе. Для этого выведем брутто-формулу (или условную формулу) данного ВВ (2,38KNO3(s)+4C(s)+S(s)): Брутто-формула имеет следующий вид: CaSbNcOdКе, где а, b, c, d и е – количества углерода (С), серы (S), азота (N), кислорода (О) и калия (К), соответственно. а=4·1=4; b=2,38·1=2,38; c=2,38·1=2,38; d=2,38·3=7,14 и е=2,38·1=2,38. Таким образом, получим: C4S2,38N2,38O7,14К2,38. Следовательно, в 320 г ВВ состава C4S2,38N2,38O7,14К2,38 содержится следующее количество моль вещества n= +16·7,14+39·2,38=365 г/моль – мольная масса указанного ВВ; mВВ=320 г – масса данного ВВ (см. условие). Тогда Q= - Пример 2. Рассчитать тепловой эффект реакции взрывчатого превращения 1 кг нитроглицерина: С3Н5(ONO2)3(l)®3CO2+2,5H2O+1,5N2+0,25O2. Решение. Расчет произведём при помощи таблицы:
Примечание: индекс (l) у вещества обозначает агрегатное состояние (жидкое).
Согласно закону Гесса найдём тепловой эффект реакции для 1 моль ВВ: DrH0298=ånкон(DfH0298)кон-ånисх(DfH0298)исх=[-393,5·3+(-241,8·2,5)+ +0·1,5+0·0,25]-[(-364,8·1)]=-1420,2 кДж/моль.
В 1 кг ВВ состава С3Н5(ONO2)3 содержится следующее количество моль вещества n= Тогда Q= - Пример 3. Рассчитать стандартную энтальпию образования ацетиленида серебра DfH0298(Ag2C2) по реакции Ag2C2=2Ag+2C, если тепловой эффект данной реакции составляет Q=364,53 кДж/моль.
Решение. Обозначим стандартную энтальпию образования ацетиленида серебра через х (искомая величина). Расчет произведём при помощи таблицы:
Тогда можно составить уравнение: DrH0298=ånкон(DfH0298)кон-ånисх(DfH0298)исх=(0·2+0·2)-(х·1) По условию задано, что Q=364,53 кДж/моль, т.е. DrH0298=-Q=-364,53 кДж/моль и уравнение примет вид: (0·2+0·2)-(х·1)=-364.53, откуда х=DfH0298(Ag2C2)=364,53 кДж/моль.
Кислородный баланс ВВ С химической точки зрения взрыв – это необратимая химическая реакция превращения исходного ВВ в газообразные продукты. Направление реакции и состав конечных продуктов определяют основные параметры взрыва: теплоту, температуру, давление и др. Входящие в состав продуктов взрыва (ПВ) окислы азота и окись углерода, как известно, обладают высокой токсичностью. Они становятся особенно опасными в подземных выработках, когда их количество превышает допустимые пределы. Борьба с ядовитыми газами в горных выработках ведется в течение многих десятков лет, а в настоящее время в связи с расширением ассортимента применяемых ВВ и развитием горных работ становится весьма важной и актуальной. Неизбежные ограничения, например, по условиям вентиляции в подземных выработках обязывают вводить определенные нормы для ВВ в отношении количества образуемых при взрыве ядовитых газов. Идеальными компонентами взрывчатого превращения являются наиболее термодинамически устойчивые соединения. Однако в случаях промышленного использования ВВ наблюдаются отклонения от идеального состава ПВ по нескольким причинам. Например, на состав ПВ с отрицательным кислородным балансом сильное влияние оказывает плотность заряда ВВ, скорость закалки ПВ (скорость теплообмена с окружающей средой), условия разлета ПВ, т.е. время протекания реакции в зоне химического пика и особенности характера взаимодействия между компонентами ПВ, а также химический состав и концентрация добавок. Кроме этого, свойства горных пород при ведении взрывных работ оказывают весьма заметное влияние на образование, состав и концентрацию ядовитых газов. Причиной отклонения от идеального состава ПВ является каталитическое действие горных пород – при взрыве одного ВВ в различных горных породах, были обнаружены значительные отклонения количественного состава ядовитых газов. Другими словами, горные породы вступают в химическое взаимодействие с ПВ, оказывая каталитическое действие на сценарии вторичных реакций в самих ПВ.
Эксперименты исследования современного периода свидетельствуют о том, что влияние породы, окружающей заряд ВВ, значительно сильнее, чем влияние состава ВВ на количество ядовитых газов в ПВ. Колебания суммарного количества ядовитых газов при взрыве различных ВВ в одной горной породе достигали 200%, а при взрыве одного ВВ в различных породах – до 1000%. При взрывании зарядов ВВ в горном массиве возникают радиальные и тангенциальные трещины, механизм образования которых подробно описан в литературе. ПВ под действием высокого давления проникают не только в свежеобразованные трещины, но и в трещины естественного происхождения, вызывая их развитие. Процесс разрушения, при котором происходит образование трещин, сопровождается разделением разноименных электрических зарядов на свежеобразованных поверхностях, при этом, в области разрыва возникают электрические поля высокой напряженности, что приводит к резко неравновесному состоянию поверхности, высокой поверхностной проводимости и химической активности. На стойкость молекул и ход химических реакций в целом оказывает решающее влияние плотность поверхностных зарядов. Под действием давления газов вероятность соударения молекул ПВ с поверхностными зарядами трещины резко возрастает, т. е. существует большая вероятность их сближения на расстояния, сравнимые с межъядерными расстояниями в молекуле. В результате этого возможна диссоциация исходных молекул и образование новых, в том числе и таких токсичных, как окислы азота, углерода и др. Для оценки энергетических параметров ВВ необходимо находить соотношение между горючими компонентами и окислителем в молекуле. Это соотношение характеризуется величиной кислородного баланса – КБ, выраженного в процентах. Кислородным балансом называется выраженное в процентах отношение массы свободного кислорода, остающегося после окисления всего углерода, содержащегося в ВВ, в углекислый газ СО2, всего водорода в H2O, всех металлов в высшие оксиды к массе взятого ВВ. Азот при этом должен оставаться свободным в виде N2. Таким образом, из определения следует, что КБ может быть положительным, отрицательным и нулевым. Положительный КБ - наличие кислорода в составе ВВ превышает количество, необходимое для окисления горючих элементов (при взрывчатом превращении ВВ образуются ядовитые окислы азота, вследствие чего такие ВВ не допускаются для взрывных работ над землей). Вещества с положительным КБ (селитра, нитроглицерин), т.е. окислители, для увеличения мощности ВВ необходимо смешивать с соединениями, имеющими отрицательный кислородный баланс, или с горючими, в которых не содержится кислорода. Нулевой КБ – в составе ВВ кислород содержится в количестве, необходимом для полного окисления всех горючих элементов.
Отрицательный КБ – наличие кислорода недостаточно для окисления всех горючих элементов и компонентов в продуктах взрывчатого превращения. При отрицательном кислородном балансе в результате взрыва могут образоваться ядовитые газы (СО), сажа (С), а при положительном - ядовитые оксиды азота. Поэтому в промышленности стремятся использовать ВВ такого состава, чтобы их кислородный баланс приближался к нулю. Кислород ВВ в этом случае расходуется таким образом, что в первую очередь он идёт на окисление металлов, водорода, серы в диоксид, углерода первостепенно в оксид, далее в диоксид. По составу ВВ делятся на индивидуальные химические вещества и механические смеси компонентов, которые вступают между собой в реакцию. Кислородный баланс индивидуальных взрывчатых веществ можно вычислить по их химическим формулам. Если индивидуальное ВВ содержит атомы кислорода, водорода и азота и его химический состав описывается формулой CaHbNcOd, то его кислородный баланс вычисляется по формуле:
где 2a - число атомов кислорода в СО2, b/2 - число атомов кислорода в H2O, а знаменатель - это масса моля ВВ, г/моль. Для смесевых ВВ вычисление КБ производится, исходя из процентного содержания компонентов смеси и по ее условной химической формуле, или по величине кислородного баланса каждого компонента, приводимого в справочниках. В том случае, если помимо атомов водорода, кислорода, углерода и азота в состав ВВ входит алюминий и его химический состав выражается условной формулой CaHbNcOdAll, кислородный баланс ВВ вычисляют по формуле:
в которой 3/2 l - число атомов кислорода в Al2O3. Кислородный баланс смесевых ВВ на практике чаще вычисляют, относя к одному килограмму смеси. В этом случае расчетная формула имеет вид:
В инженерной практике применяют также следующие расчетные формулы при определении КБ. Так для индивидуальных ВВ можно использовать следующее выражение:
где А Г– грамм-атомный вес излишка или недостатка кислорода в составе ВВ; М – грамм-молекулярный вес данного ВВ; 16 – грамм-атомный вес кислорода; КГ – необходимое число атомов кислорода для полного окисления атомов углерода в СО2 и атомов водорода в воду; KB – число атомов кислорода в составе взрывчатого вещества; АГ=(КВ–КГ)·16. KГ =2·Сn+0,5·Hm.
Нулевому КБ соответствует кислородный коэффициент aК, равный 1: aК=d/(2a+0,5b)=1. Относительно 1 кг смеси ВВ расчет КБ можно производить по формуле:
Если в смеси ВВ содержится алюминий, то уравнения для КБ и aК будут иметь следующий вид:
где е – количество грамм-атомов алюминия. В таблице П-4 приложения приведены значения КБ некоторых ВВ и их компонентов.
2.7.1 Примеры определения КБ ВВ
Пример 1. Вычислить кислородный баланс нитроглицерина C3H5(ONO2)3. Решение. В молекуле нитроглицерина число атомов: кислорода d = 9, углерода a = 3, азота c = 3 и водорода b = 5. Подставляя эти данные, получим:
Нитроглицерин имеет слегка положительный кислородный баланс. Пример 2. Вычислить кислородный баланс тринитротолуола (тротила) C7H5(NO2)3. Решение. В молекуле тринитротолуола число атомов: кислорода d = 6, углерода a = 7, азота c = 3 и водорода b = 5. Подставляя эти данные, получим:
Как следует из этого расчета, тринитротолуол имеет резко отрицательный кислородный баланс. Пример 3. Вычислить кислородный баланс нитрата аммония (аммиачной селитры) NH4NO3. Решение. В молекуле NH4NO3 число атомов: кислорода d = 3, углерода a = 0, азота c = 2 и водорода b = 4. В итоге получим:
Положительный КБ. Пример 4. Вычислить кислородный баланс аммонала, смесевого ВВ, состоящего из аммиачной селитры (80% по массе), тротила C7H5(NO2)3 (15%) и алюминия (5%). Расчет выполнить, исходя из массы ВВ, равной 1 кг. Решение. Первый способ – по условной химической формуле смеси. В 1000 г ВВ заданного состава содержится 800 г NH4NO3 (масса одного моля М = 80), 150 г тротила (М = 227) и 50 г алюминия. Число молей этих компонентов в 1 кг их смеси заданного состава составляет: nNH4NO3 = C4,62 H43,3N21,28O33,96Al1,85, а кислородный баланс ВВ равен
Второй способ решения этой задачи – по величине кислородного баланса (приложение) и доле по массе (wi) каждого компонента смесевого ВВ. Формула для расчета кислородного баланса в этом случае имеет вид: КБ = S(КБi × wI) Кислородный баланс NH4NO3 равен +20% (см. пример 3), для тротила КБ = – 74% (пример 2), для алюминия КБ = - Пример 5. Какое количество тротила (КБ = -74%) следует добавить к 1 кг нитрата аммония (КБ = +20%), чтобы кислородный баланс этой смеси был равен нулю? Решение. Обозначив искомую массу тротила за x, получим КБ = S(КБi × wI) =
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 973; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.210.17 (0.068 с.) |



 ; 4=
; 4=  ;
; (М – мольные массы, г/моль; m – массы в соответствии с процентным содержанием, г; 320 г – общая масса ВВ).
(М – мольные массы, г/моль; m – массы в соответствии с процентным содержанием, г; 320 г – общая масса ВВ). , где МВВ=12·4+32·2,38+14·2,38+
, где МВВ=12·4+32·2,38+14·2,38+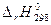 ·n= -8,59 кДж/моль·0,877 моль= -7,53 кДж.
·n= -8,59 кДж/моль·0,877 моль= -7,53 кДж. , где МВВ=227 г/моль – мольная масса указанного ВВ; mВВ=103 г – масса данного ВВ (см. условие).
, где МВВ=227 г/моль – мольная масса указанного ВВ; mВВ=103 г – масса данного ВВ (см. условие). ,
, ,
, .
.
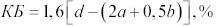

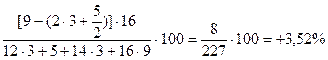 .
. .
. .
. , nC7H5(NO2)3 =
, nC7H5(NO2)3 =  , nAl =
, nAl =  = 1,85 или в ней содержится 10NH4NO3 + 0,66 C7H5(NO2)3 + 1,85Al. Для вывода условной химической формулы, которая должна иметь общий вид CaHbNcOdAll, вычисляем число молей: атомов углерода a = 0,66×7 = 4,62; атомов водорода b = 10×4 + 0,66×5 = 43,3; атомов азота с = 10×2 + 0,66×3 = 21,98; атомов кислорода d = 10×3 + 0,66×6 = 33,96; атомов алюминия l = 1,85. Условная химическая формула ВВ, таким образом, имеет вид:
= 1,85 или в ней содержится 10NH4NO3 + 0,66 C7H5(NO2)3 + 1,85Al. Для вывода условной химической формулы, которая должна иметь общий вид CaHbNcOdAll, вычисляем число молей: атомов углерода a = 0,66×7 = 4,62; атомов водорода b = 10×4 + 0,66×5 = 43,3; атомов азота с = 10×2 + 0,66×3 = 21,98; атомов кислорода d = 10×3 + 0,66×6 = 33,96; атомов алюминия l = 1,85. Условная химическая формула ВВ, таким образом, имеет вид: = + 0,47%.
= + 0,47%. =-88,9%. Для смеси заданного состава КБ = 0,8×20 + 0,15×(-74) + 0,05×(-88,9) = + 0,46%.
=-88,9%. Для смеси заданного состава КБ = 0,8×20 + 0,15×(-74) + 0,05×(-88,9) = + 0,46%. , откуда x =
, откуда x =  = 270,3 г.
= 270,3 г.


