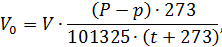Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Послідовність виконання роботи та розрахунківСодержание книги
Поиск на нашем сайте
Для отримання оксиду сірки (VІ) S02 з балону 1, а повітря з компресора 7 подають у змішувач 3. Після змішування синтез-газ подається в трубчасту піч 4, де в об’ємі каталізатору при температурі 450-600 °С відбувається процес окислення S02 в S03. Після виходу з печі 4 газ охолоджується, проходить через поглинальні склянки 6 (для поглинання S02 і S03) та направляється в атмосферу. Колбу 8 заповнюють до гумової пробки дистильованою водою, забарвленою метиловим оранжевим. Трубка 9 опускається до дна колби 8. Трубку 9 приєднують до крана відбору проби 5, трубку 10 опускають в мірну колбу 14. Відкривають затискачі (спочатку 11, потім 12). Коли мірна колба 14 заповниться до позначки, закривають затискачі 11 і 12. При цьому необхідно пам’ятати, що в колбі 8 має обов’язково залишитися певна кількість води (біля 200 см3), щоб шар води, забарвлений в червоний колір під впливом поглинутих S02 і S03, не попав у мірну колбу. Після цього колбу 14 від’єднують від колби 8 та струшують у перевернутому положенні до повного поглинання туману. Потім, перевернувши, колбу 8 з’єднують за допомогою трубки 10 з ротаметром і заміряють розрідження. Відмічають температуру, при якій проводилося визначення розрідження в колбі. Після цього вміст колби 8 переносять у конічну колбу, ретельно промивають трубки і горловину колби 8. Промивні води додають до рідини, яка аналізується.
Розрахунок ведуть таким чином: Об’єм води, що витекла у мірну колбу 14, зводять до нормальних умов:
де V0 - об'єм при нормальних умовах, см3; V - об'єм води, що витік у колбу 13, см3; Р та р - різниця барометричного та залишкового тисків у колбі 8, Па; 101325 - нормальний тиск, Па; t - температура, при якій аналізувався газ, °С. Маса GS02 + S03 (в г) у перерахунку на S03 буде становити: GS02 + S03 = 0,040 · 0,1a · K1, де 0,040 - мг-екв S03; а - об'єм 0,1 н розчину NaОН, який пішов на титрування, см3. Маса S02 дорівнює, г: GS02 = 0,032 · 0,1% · K2, де 0,032 - мг-екв S02; в - об’єм 0,1н розчину І2, який пішов на титрування, см3. Знайдену масу S02 перераховують на S03:
Тоді маса S03 буде дорівнювати GS02 + S03 - G'S03 = GS03. Газ містить, см3:
Об’єм газової суміші, взятий для аналізу, см3: Vзаг = V0+А+В, тоді склад газу буде, %:
5. Техніка безпеки 1. Перед проведенням експерименту установку слід перевірити на герметичність. 2. Температура в контактному апараті для запобігання спіканню каталізатора не повинна перевищувати 600 °С. 3. При виявленні запаху S02 негайно повідомити про це викладача або майстра по наладці установки. 4. Робота повинна виконуватися тільки при ввімкненій вентиляції у витяжній шафі. 6. Контрольні питання 1. Хімізм процесу контактного окислення S02 в S03. 2. Параметри технологічного процесу окислення S02 в S03. 3. Апаратурне оформлення процесу. 4. Сутність методики проведення роботи по визначенню оксидів сірки в газі. 7.Література 1. Х.Мухленов И.П., Кузнецов Д.А., Авербук А.Я. и др. Общая химическая технология, - М.: Высшая школа, 1983. 2. Амелин А.Г. Технология серной кислоты. - М.: Химия, 1983. 3. Руководство к практическим занятиям по технологии неорганических веществ: Учебное пособие для вузов / Под ред. М.Е. Позина. - Л.: Госхимиздат, 1967.
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 97; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.136.22.184 (0.007 с.) |

 Отримані розчини Н2 S03 та Н2S04 титрують 0,1н розчином лугу в присутності 2-3 крапель фенолфталеїну. Далі додають у той самий розчин 2-3 см3 0,5 % розчину крохмалю та титрують 0,1н розчином І2 до появи синього забарвлення.
Отримані розчини Н2 S03 та Н2S04 титрують 0,1н розчином лугу в присутності 2-3 крапель фенолфталеїну. Далі додають у той самий розчин 2-3 см3 0,5 % розчину крохмалю та титрують 0,1н розчином І2 до появи синього забарвлення.