
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Домашняя работа «анализ двойных диаграмм»Содержание книги
Поиск на нашем сайте
2.1. МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО ВЫПОЛНЕНИЮ ДОМАШНЕЙ РАБОТЫ «АНАЛИЗ ДВОЙНЫХ ДИАГРАММ» К выполнению домашнего задания предъявляются следующие требования: · домашнее задание выполняется на формате А4 в печатном виде; · оформление титульного листа в приложении П1; · на первой странице указываются номер задания и через тире буквенный индекс варианта, помещается текст содержания задания с указанием названия диаграммы, химического состава заданного сплава и температуры; · на второй странице слева вычерчивается в масштабе диаграмма так, чтобы справа было место для изображения кривой охлаждения. Для построения кривой охлаждения заданного в варианте сплава необходимо на оси концентраций найти точку, соответствующую составу сплава. Из этой точки восстановить ординату заданного сплава так, чтобы она охватывала диапазон температур от оси концентраций до области жидкого состояния. Ордината сплава должна отчетливо выделяться на диаграмме. Точки пересечения ординаты с линиями диаграммы являются критическими точками заданного сплава (температурами начала или окончания фазовых превращений). Правее диаграммы необходимо вычертить оси «Температура – Время» для построения кривой охлаждения. На ось ординат следует также нанести критические точки заданного сплава в градусах Цельсия; · на последующих страницах необходимо произвести общее описание заданной диаграммы, описание процесса кристаллизации, указанного в варианте сплава, и определить состав и количество фаз на 1 килограмм сплава. Пример выполнения домашнего задания приведен в приложении П2.
2.2. ЦелИ и задчи изучения диаграмм состояния Диаграмма состояния представляет собой графическое изображение зависимости температур фазовых превращений в сплавах от их состава. Цель изучения диаграмм состояния сплавов: · научиться по диаграмме состояния устанавливать, какие процессы происходят в сплавах при их охлаждении, какие при этом образуются фазы и структуры сплавов разного состава; · научиться анализировать процессы фазовых превращений в зависимости от изменения температуры сплава; · выявлять взаимосвязь механических и технологических свойств сплавов от соответствующего фазового и структурного состояния. По диаграммам состояния можно устанавливать не только температуры фазовых превращений в сплавах любого состава, но и качество и количество фаз в разных областях диаграммы состояния. Однако этим не исчерпывается практическая значимость диаграмм состояния сплавов. В частности, разбирая процессы, происходящие при охлаждении сплава, по диаграмме состояния можно выявить, в какой форме проявляются образующиеся фазы при охлаждении сплава. Фазой называется однородная часть системы, образованная компонентами сплава, которая во всех своих точках имеет одинаковые составы, строение и свойства. Жидкая фаза представляет собой раствор расплавленных компонентов. Твердые фазы являются зернами, имеющими определенную форму, размер, состав, структуру и свойства. Это могут быть твердые растворы, химические соединения, зерна чистых компонентов, не образующих с другими компонентами ни твёрдых растворов, ни химических соединений. Форма проявления фаз называется структурой сплава. Возможность по диаграмме состояния прогнозировать структуру, образующуюся из сплавов разного состава, имеет очень большое практическое значение, так как в двухфазных сплавах не фазы, а именно структуры сплавов определяют их механические свойства. Так, например, стали и белые чугуны состоят из одних и тех же фаз, но свойства этих сплавов сильно различаются именно потому, что структуры этих сплавов разные. Имеются тысячи разработанных диаграмм состояния сплавов. Все их выучить механически невозможно. Поэтому специалист должен уметь мысленно представить те процессы, которые происходят в сплавах и образуют их структуру и свойства, чтобы оптимально воздействовать на технологический процесс. Для этого необходимо: 1) ясное понимание особенностей строения основных фаз в сплавах, которыми являются твердые растворы, химические соединения, чистые компоненты; 2) знание, как эти фазы обозначаются; 3) знание признаков этих фаз; 4) умение по диаграмме состояния определить состав и количество фаз; 5) умение логически мыслить. Для выработки навыка разбора процессов, происходящих при охлаждении конкретного сплава, необходимо обязательно выполнение следующих действий: строить кривую охлаждения разбираемого сплава; против участков кривой охлаждения схематично изображать состояние фаз (структуру) сплава; письменно объяснять процесс, происходящий в сплаве при рассматриваемых температурных условиях.
2.3. ПРАВИЛО ФАЗ При рассмотрении процессов превращения в диаграммах равновесного состояния сплавов широко применяется так называемое «правило фаз», дающее возможность проверить правильность построения диаграмм и теоретически обосновать направление протекания процессов превращения для установления равновесного состояния системы, которое определяется следующими переменными факторами: температурой, давлением и составом фаз системы (концентрацией). Число переменных величин (концентрация фаз, температура, давление), которые могут изменяться независимо друг от друга, называется числом степеней свободы или вариантностью системы. Число степеней свободы зависит от количества компонентов, числа фаз в системе и переменных внешних условий – температуры и давления. Так как давление в практических условиях изменяется в небольших пределах, не оказывая существенного влияния на процессы превращения, то основным переменным фактором является только температура и тогда уравнение «правила фаз» имеет вид
Если число степеней свободы системы равно нулю (С = 0), то такое равновесие называют нонвариантным (безвариантным). Это означает, что сплав с данным числом фаз может существовать только при определенных условиях: при постоянной температуре и определенной концентрации всех находящихся в равновесии фаз. Если С = 1, то такая система называется моновариантной (одновариантной), т. е. чтобы не нарушилось равновесное состояние фаз, можно изменить либо концентрацию фаз, либо температуру. Когда С = 2, система бивариантна (двухвариантна). Наличие одной или двух степеней свободы позволяет изменять одну или две переменных без изменения числа фаз.
2.4. Правило отрезков При анализе строения и свойств сплавов рассматривается состав фаз и их количественное соотношение. Для определения количества фаз и их концентрации в любой точке двухфазной области диаграммы состояния сплавов служит «правило отрезков (рычага)». На рис. 2.1 приведена диаграмма состояния сплавов с неограниченной растворимостью в твердом состоянии. При температуре t1 сплав состоит из α -твёрдого раствора и жидкой фазы. Для определения массового или объемного соотношения фаз и их состава для сплава I при температуре t1 проводим через данный температурный уровень горизонтальную линию (коноду) до пересечения с ближайшими линиями диаграммы АВС и АDС, ограничивающими двухфазную область. Проекции точек пересечения В, D, спроектированные на ось концентрации В’, D’ показывают состав (концентрацию) фаз: жидкая содержит 20 % В, твердая – 72 % В.
Рис. 2.1. Применение «правила отрезков» для определения концентрации фаз
Отрезки, лежащие на температурной горизонтали (коноде) между точками концентрации фаз ( В, D ) и средней точкой, соответствующей концентрации исходного сплава (Е), обратно пропорциональны количеству этих фаз:
Иными словами, количество фазы, например жидкости, характеризуется величиной противолежащего отрезка ЕD, а количество кристаллов С помощью правила отрезков можно определить не только фазовый состав сплава, но и количественное соотношение структурных составляющих, например избыточных кристаллов и эвтектики. Для определения количественного соотношения фаз:
Для определения веса фаз на 1 килограмм сплава:
2.5. Общий Обзор диаграмм состояния Как известно, вид диаграммы состояния зависит от характера взаимодействия компонентов в жидком и твердом состояниях, возможности образования устойчивых и неустойчивых химических соединений, протекания тех или иных нонвариантных превращений. Различные варианты простейших (или типовых) диаграмм состояний как диаграмм равновесия систем безымянных компонентов А и В приведены ниже. 1. Диаграмма состояния для сплавов, образующих смеси из чистых компонентов. Общий вид диаграммы для случая, когда оба компонента сплава в жидком состоянии неограниченно растворимы, а в твердом – не растворяются, не образуют химических соединений и не имеют полиморфных превращений, представлен на рис. 2.2а. Фазы: жидкость – Ж, чистые компоненты – А и В. Линия АСВ– линия ликвидус; линия ДСЕ – линия солидус. На линии АС начинают выделяться кристаллы А; на линии СВ – кристаллы В; на линии ДСЕ из жидкости концентрации С одновременно выделяются кристаллы А и В. Эвтектическая смесь двух видов кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой. 2. Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии. На рис. 2.2б приведена диаграмма состояния для сплавов с неограниченной растворимостью компонентов друг в друге в жидком и твердом состоянии, имеющих одинаковые типы решеток, небольшую разницу атомных радиусов (до 10–12 %) и сходное строение наружных электронных оболочек, т. е. близость химической природы металлов. Линия АМВ– линия ликвидус; линия АNВ – линия солидус; фаза α представляет собой неограниченный твёрдый раствор замещения компонентов А и В, зерна этой фазы имеют единую кристаллическую решетку, но у сплавов разного состава число атомов компонентов А и В в элементарных ячейках решетки различно. 3. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии, с эвтектикой. На рис. 2.2в приведена диаграмма состояния для сплавов с ограниченной растворимостью компонентов друг в друге в твердом состоянии, с эвтектическим превращением. Ограниченные твердые растворы на основе компонентов А и В образуются, когда последние заметно отличаются строением и размером атомов, кристаллической структурой и физико-механическими свойствами. Ограниченные твердые растворы могут образовываться по типу замещения и внедрения. Линия АСВ – линия ликвидус; линия АDCEВ – линия солидус; фаза α является твердым раствором компонента В в кристаллической решетке компонента А; фаза β представляет собой твёрдый раствор компонента А в кристаллической решетке компонента В. Кривые DM и EN – линии ограниченной растворимости в твердом состоянии (сольвус), отражающие характер изменения растворимости компонентов друг в друге в зависимости от температуры. Растворимость компонента В в компоненте А уменьшается с понижением температуры (линия DM). Растворимость компонента А в компоненте В не зависит от температуры (линия EN). DCE – линия эвтектического превращения ЖВ → (αD+βE). Смесь получившихся в результате данной реакции ограниченных твёрдых растворов αD и βE называется эвтектической (эвтектикой). Сплавы, располо- женные между точкой максимальной растворимости М и эвтектической точкой С, называют доэвтектическими, а сплавы, расположенные между С и N, – заэвтектическими. 4. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии, с перитектикой. На рис. 2.2г показана диаграмма состояния для сплавов с ограниченной растворимостью в твердом состояния с перитектическим превращением. Диаграммы такого типа образуют металлы с небольшой разницей в строении атомов и их размеров, но заметно отличающиеся друг от друга температурами плавления. Линия АСВ – линия ликвидус; линия АDEВ – линия солидус; линия
|
||
|
Последнее изменение этой страницы: 2016-12-28; просмотров: 517; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.156 (0.009 с.) |

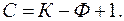 (2.1)
(2.1)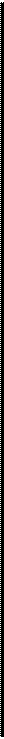 где С ≥ 0 – число степеней свободы (вариантность системы), К – число компонентов в системе, Ф – количество фаз, находящихся в равновесии при рассматриваемых условиях.
где С ≥ 0 – число степеней свободы (вариантность системы), К – число компонентов в системе, Ф – количество фаз, находящихся в равновесии при рассматриваемых условиях.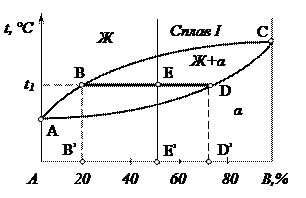
 . (2.2)
. (2.2)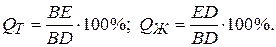 (2.3)
(2.3)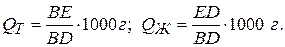 (2.4)
(2.4)


