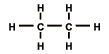Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Парафиновые углеводороды метанового рядаСодержание книги
Поиск на нашем сайте
ОГЛАВЛЕНИЕ
Введение.......................................................................................................... 3 1. Состав и свойства нефти............................................................................. 4 1.1 Парафиновые углеводороды метанового ряда....................................... 7 1.2 Нафтеновые углеводороды этиленового ряда......................................... 8 1.3 Ароматические углеводороды бензольного ряда................................... 9 2. Состав и свойства природного газа......................................................... 10 2.1 Газовый конденсат.................................................................................. 12 3. Состав и свойства газовых гидратов........................................................ 14 3.1 Образование газовых гидратов.............................................................. 14 3.2 Строение гидратов.................................................................................. 17 4. Состав и свойства воды............................................................................. 21 4.1 Химический состав воды......................................................................... 21 4.2 Физико - химические свойства воды...................................................... 22 5. Состав и свойства пластовых вод............................................................. 23 Список использованных источников и литературы.................................... 27
ВВЕДЕНИЕ
Флюиды (от латинского fluidus – текучий) – любые вещества, поведение которых при деформации может быть описано законами механики жидкостей. Термин введен в науку в 17 веке для обозначения гипотетических жидкостей, с помощью которых объясняли некоторые физические явления и образование горных пород. С развитием науки понятие «флюиды» изменилось. Реологическими и геологическими исследованиями доказано, что все реальные тела под действием длительных тангенциальных нагрузок ведут себя как жидкости. В геологических процессах, длительность которых измеряется миллионами лет, в качестве флюидов могут выступать не только газы,водные растворы, нефть, ил, магма, но и глины, соли, ангидриты, известняки и другие твердые вещества. Основными компонентами промышленной органической химии являются углеводороды. Углеводородное сырье становится основой для получения производных составляющих углеводородов. Углеводородным сырьем считают углеводороды природного происхождения и продукты, прошедшие процесс переработки. При типировании к углеводородному сырью относят следующие вещества: · Нефть · Природный газ · Газовый конденсат В данной работе мы рассмотрим только химико–физические свойства, по большей части химические свойства углеводородного сырья, воды, пластовых вод и газогидратов.
Состав и свойства нефти
Нефть представляет собой комбинацию углеводородов в различных пропорциях, является полезным ископаемым. Физическими признаками являются жидкое состояние, маслянистость, специфичный запах, горючесть. Относится к ископаемым, находящимся в осадочных породах. Цвет нефти может различаться от грязно-коричневого до чисто черного, при этом встречаются месторождения с бесцветной или ярко-зеленой жидкостью. Нефть представляет собой весьма сложное минеральное вещество. Она не образует самостоятельного пласта, а заполняет пустоты в породах, принимает форму залегания вмещающих ее пород. Как правило, нефти небольшой относительной плотности обладают более светлой окраской, а большой - имеют темный и даже черный цвет и более вязки. Запах может варьироваться от приятного до насыщенно-тяжелого. Физические показатели нефти определяются наличием в ее составе примесей азота, серы или кислорода, остающихся в масле и нефтяном остатке. С конца ХХ века и до настоящего момента нефть считается ключевым полезным ископаеым, имеющим определяющую роль в экономике и производстве. Впервые была изучена пенсильванская нефть Северо-Американского нефтеносного бассейна, в которой немецкий ученый К. Шорлеммар (1834— 1892) обнаружил предельные углеводороды метанового ряда. Исчерпывающее объяснение строения углеводородов дал А.М. Бутлеров (1861), а основоположником науки о нефти принято считать Д.И. Менделеева. В большинстве случаев содержание углерода в нефти различных месторождений составляет 84-87%, а содержание водорода - 12-14%. На долю этих двух элементов приходится 97-99% всего состава нефти. Наиболее часто встречающаяся примесь - сера (до 7%), хотя во многих нефтях серы практически нет. Сера содержится в нефтях в чистом виде (самородная), в виде сероводорода или меркаптанов. Она усиливает коррозию металлов. Азота в нефтях не больше 1,7%, он совершенно безвреден в силу своей инертности. Кислород встречается в нефти не в чистом виде, а в различных соединениях (кислоты, фенолы, эфиры и т.д.) Его в нефти не более 3,6%. Каких-либо закономерностей в соотношении углерода и водорода не установлено. Из металлов в нефти присутствуют железо, магний, алюминий, медь, натрий, олово, кобальт, хром, германий, ванадий, никель, ртуть и другие. Содержание металлов столь мало, что они обнаруживаются лишь в золе, остающейся после сжигания нефти. По содержанию серы нефти подразделяют на малосернистые с содержанием серы до 0,5% и на высокосернистые с содержанием серы более 0,5%. Присутствие серы в нефтях нежелательно, так как она разъедает нефтеперегонную аппаратуру, нефтепроводы и придает нефти неприятный запах. В составе нефти всегда присутствуют в относительно большем или меньшем количестве асфальтены и смолы. Асфальтены - это высокомолекулярные органические соединения, содержащие коме углерода и водорода серу и кислород. По внешнему виду представляют собой бурые или черные аморфные порошки. Смолы - это полужидкие, иногда почти твердые, тягучие темно-желтые или темно-коричневые вещества с относительной плотностью несколько выше единицы; по своим химическим свойствам очень напоминают асфальт. По содержанию асфальтенов и смол нефти подразделяют на малосмолистые с содержанием смол менее 8%; смолистые с содержанием смол 8-28%; сильно смолистые с содержанием смол более 28%. Основные физические свойства нефти - относительная плотность, вязкость, температура кипения, теплота сгорания, растворимость, электрические и оптические свойства. Нефти подразделяют на легкие и тяжелые. Нефти с относительной плотностью менее 0,9 считаются легкими, с плотностью 0,9 и более - тяжелыми. Различие плотности нефтей объясняется, прежде всего их химической природой, а также зависит от количества растворенного в них газа: чем больше количество газа в нефти, тем меньше ее плотность. Вязкость, или внутреннее трение, - это свойство жидкости оказывать сопротивление перемещению ее частиц относительно друг друга под влиянием приложенной силы. существенное влияние на вязкость оказывают температура, давление и факторы химического характера. Вязкость жидкостей с повышением температуры уменьшается, а с повышением давления возрастает. Наибольшей вязкостью обладают ароматические углеводороды, далее следуют нафтены, затем парафины. Нефть не имеет определенной температуры кипения, поэтому для нее различают начальную и конечную температуру кипения. Чем меньше плотность нефти, тем при более низкой температуре она закипает. Теплота сгорания нефтей колеблется в пределах 10300-10800 ккал. Чем меньше плотность нефти, тем выше ее теплота сгорания. Нефть и ее дистилляты растворяются в воде в ничтожно малом количестве. Например, вода растворяет 0,027% керосина, т. е. 1 м3 воды может растворить только 270 грамм керосина. Нефть и нефтепродукты хорошо растворяются в органических растворителях: бензоле. хлороформе, сероуглероде, эфире. На этом свойстве основано определение нефтенасыщенности пород путем получения из них нефтяных вытяжек. Нефть и ее производные по отношению к электрическому току являются изоляторами. Сопротивление, которое она оказывает прохождению электрического тока, весьма велико и на изменении этого свойства нефтей основано применение электрокаротажа скважин. В зависимости от преобладания в нефти одного из трех представителей групп углеводородов в количестве более 50% нефти именуются метановыми, нафтеновыми, ароматическими. Если к доминирующему присоединяется другой углеводород в количестве не менее 25 %, то им дают комбинированное название, например метанонафтеновые. Парафиновые углеводороды метанового ряда отличаются наибольшим содержанием водорода. Нафтеновые углеводороды этиленового ряда содержат меньше водорода. Ароматические углеводороды бензольного ряда - еще меньше водорода. Чистые классы нефтей парафиновых, нафтеновых и ароматических в природе не встречаются. В большинстве случаев нефти представляют собой смешанные типы с преобладанием того или иного класса.
Газовый конденсат
Газовый конденсат - сложное природное органическое вещество-смесь, состоящее преимущественно из легких (нефтяных) углеводородных соединений, растворённых в газе или переходящих в жидкую фазу при определённых пластовых термобарических условиях. Газовый конденсат получается из природного газа при разработке газоносных месторождений. В пластовых условиях при высоком давлении (от 10 до 60 МПа) и температуре в парообразном состоянии находятся некоторые бензино-керосиновые фракции и, что случается реже, более высокомолекулярные жидкие компоненты нефти. При разработке месторождений давление падает в несколько раз - до 4-8 МПа, и из газа выделяется сырой нестабильный конденсат, содержащий, в отличие от стабильного, не только углеводороды С5 и выше, но и растворённые газы метан-бутановой фракции. Содержание жидких компонентов в одном кубометре газа для различных месторождений составляет от 10 до 700 см³. Как правило, это прозрачная жидкость, но в зависимости от глубины, с которой она была извлечена, цвет может меняться от соломенного до желтовато-коричневого из-за примесей нефти. Газовый конденсат иногда называют белой нефтью — он может использоваться в качестве топлива. При уменьшении давления, по мере расходования газа, газовый конденсат выделяется в геологическом пласте и пропадает для потребителя. Поэтому при эксплуатации месторождений с большим содержанием газового конденсата из добытого на поверхность земли газа выделяют углеводороды С3 и выше, а фракцию C1—С2 для поддержания давления в пласте закачивают обратно. Главные направления в переработке газового конденсата — топливное и нефтехимическое. Из газового конденсата получаются высококачественные бензины, реактивное, дизельное и котельное топливо. Нефтехимическая переработка конденсата сводится к получению ароматических углеводородов, олефинов и других мономеров (маленьких молекул), используемых для производства пластмасс, синтетических каучуков, волокон и смол.
Образование газовых гидратов
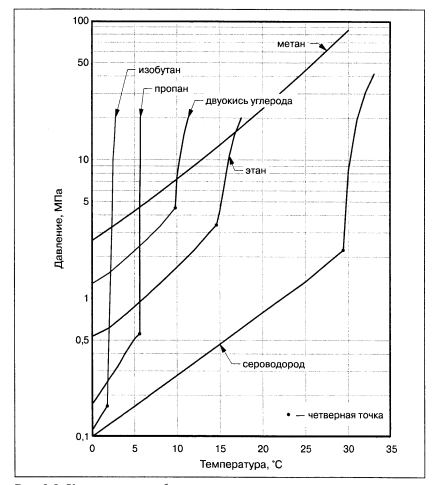
Газовые гидраты подразделяются на техногенные (искусственные) и природные (естественные). Все известные газы при определенных давлениях и температурах образуют кристаллогидраты, структура которых зависит от состава газа, давления и температуры. Гидраты могут стабильно существовать в широком диапазоне давлений и температур. Например, гидрат метана существует при давлениях от 2*10-8 до 2*103 MPa и температурах от 70 до 350 K. Некоторые свойства гидратов уникальны. Например, один объем воды при переходе в гидратное состояние связывает 207 объемов метана. При этом ее удельный объем возрастает на 26% (при замерзании воды ее удельный объем возрастает на 9%). 1 м3 гидрата метана при P=26 атм и Т=0°С содержит 164 объема газа. При этом на долю газа приходится 0.2 м3, на воду 0,8 м3. Удельный объем метана в гидрате соответствует давлению порядка 1400 атм. Разложение гидрата в замкнутом объеме сопровождается значительным повышением давления. На рисунке 3.1.1 дана диаграмма условий существования гидрата некоторых компонентов природного газа в координатах давление-температура.
Рисунок 3.1.1 - Кривые газо-гидрато-образования для некоторых компонентов природного газа.
Для образования газогидрата необходимы следующие три условия: 1. Благоприятные термобарические условия. Образованию газогидратов благоприятствует сочетание низкой температуры и высокого давления. 2. Наличие гидратообразующего вещества. К гидратообразующим веществам относятся метан, этан, пропан, двуокись углерода и др. 3. Достаточное количество воды. Воды не должно быть ни слишком мало, ни слишком много. Для предотвращения газогидратообразования достаточно исключить одно из трёх условий. Природные газовые гидраты представляют собой метастабильный минерал, образование и разложение которого зависит от температуры, давления, химического состава газа и воды, свойств пористой среды и др. Морфология газогидратов весьма разнообразна. В настоящее время выделяют три основных типа кристаллов: · массивные кристаллы. Формируются за счёт сорбции газа и воды на всей поверхности непрерывно растущего кристалла; · вискерные кристаллы. Возникают при туннельной сорбции молекул к основанию растущего кристалла; · гель-кристаллы. Образуются в объёме воды из растворённого в ней газа при достижении условий гидратообразования. В пластах горных пород гидраты могут быть как распределены в виде микроскопических включений, так и образовывать крупные частицы, вплоть до протяжённых пластов многометровой толщины. Благодаря своей клатратной структуре единичный объём газового гидрата может содержать до 160—180 объёмов чистого газа. Плотность гидрата ниже плотности воды и льда (для гидрата метана около 900 кг/м³). Ускоренному образованию газовых гидратов способствуют следующие явления: · Турбулентность. Образование газовых гидратов активно протекает на участках с высокими скоростями потока среды. При перемешивании газа в трубопроводе, технологическом резервуаре, теплообменнике и т.п. интенсивность газогидратообразования возрастает. · Центры кристаллизации. Центр кристаллизации представляет собой точку, в которой имеются благоприятные условия для фазового превращения, в данном случае – образования твердой фазы из жидкой. · Свободная вода. Наличие свободной воды не является обязательным условием для гидратообразования, однако интенсивность этого процесса в присутствии свободной воды значительно возрастает. Кроме того, поверхность раздела фаз вода-газ является удобным центром кристаллизации для образования газогидратов.
Строение гидратов
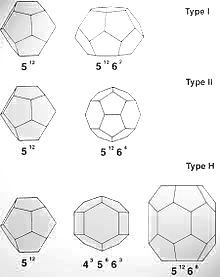
В структуре газогидратов молекулы воды образуют ажурный каркас (то есть решётку хозяина), в котором имеются полости. Установлено, что полости каркаса обычно являются 12- («малые» полости), 14-, 16- и 20-гранниками («большие» полости), немного деформированными относительно идеальной формы. Эти полости могут занимать молекулы газа («молекулы—гости»). Молекулы газа связаны с каркасом воды ван-дер-ваальсовскими связями. В общем виде состав газовых гидратов описывается формулой M·n·H2O, где М — молекула газа-гидрато-образователя, n — число молекул воды, приходящихся на одну включённую молекулу газа, причём n — переменное число, зависящее от типа гидрато-образователя, давления и температуры. Полости, комбинируясь между собой, образуют сплошную структуру различных типов. По принятой классификации они называются КС, ТС, ГС - соответственно кубическая, тетрагональная и гексагональная структура. В природе наиболее часто встречаются гидраты типов КС-I (англ. sI), КС-II (англ. sII), в то время как остальные являются метастабильными.
Таблица 3.2.1 - Некоторые структуры клатратных каркасов газовых гидратов.
Рисунок 3.2.1 - Кристаллические модификации газогидратов. При повышении температуры и уменьшении давления гидрат разлагается на газ и воду с поглощением большого количества теплоты. Разложение гидрата в замкнутом объёме либо в пористой среде (естественные условия) приводит к значительному повышению давления. Кристаллогидраты обладают высоким электрическим сопротивлением, хорошо проводят звук, и практически непроницаемы для свободных молекул воды и газа. Для них характерна аномально низкая теплопроводность (для гидрата метана при 273 К в пять раз ниже, чем у льда). Для описания термодинамических свойств гидратов в настоящее время широко используется теория Ван-дер-Ваальса - Платтеу. Основные положения данной теории: · решётка хозяина не деформируется в зависимости от степени заполнения молекулами-гостями либо от их вида; · в каждой молекулярной полости может находиться не более одной молекулы-гостя; · взаимодействие молекул-гостей пренебрежимо мало; · к описанию применима статистическая физика. Несмотря на успешное описание термодинамических характеристик, теория Ван-дер-Ваальса - Платтеу противоречит данным некоторых экспериментов. В частности, показано, что молекулы-гости способны определять как симметрию кристаллической решётки гидрата, так и последовательность фазовых переходов гидрата. Помимо того, обнаружено сильное воздействие гостей на молекулы-хозяева, вызывающее повышение наиболее вероятных частот собственных колебаний. Большинство природных газов (CH4, C2H6, C3H8, CO2, N2, H2S, изобутан и т. п.) образуют гидраты, которые существуют при определённых термобарических условиях. Область их существования приурочена к морским донным осадкам и к областям многолетнемёрзлых пород. Преобладающими природными газовыми гидратами являются гидраты метана и диоксида углерода. При добыче газа гидраты могут образовываться в стволах скважин, промышленных коммуникациях и магистральных газопроводах. Отлагаясь на стенках труб, гидраты резко уменьшают их пропускную способность. Для борьбы с образованием гидратов на газовых промыслах вводят в скважины и трубопроводы различные ингибиторы(метиловый спирт, гликоли, 30%-ный раствор CaCl2), а также поддерживают температуру потока газа выше температуры гидратообразования с помощью подогревателей, теплоизоляцией трубопроводов и подбором режима эксплуатации, обеспечивающего максимальную температуру газового потока. Для предупреждения гидратообразования в магистральных газопроводах наиболее эффективна газоосушка — очистка газа от паров воды.
Состав и свойства воды
Около 71 % поверхности Земли покрыто водой (океаны, моря, озёра, реки, льды) — 361,13 млн км2. На Земле примерно 96,5 % воды приходится на океаны, 1,7 % мировых запасов составляют грунтовые воды, ещё 1,7 % — ледники и ледяные шапки Антарктиды и Гренландии, небольшая часть находится в реках, озёрах и болотах, и 0,001 % в облаках (образуются из взвешенных в воздухе частиц льда и жидкой воды). Бо́льшая часть земной воды — солёная, непригодная для сельского хозяйства и питья. Доля пресной составляет около 2,5 %, причём 98,8 % этой воды находится в ледниках и грунтовых водах. Менее 0,3 % всей пресной воды содержится в реках, озёрах и атмосфере, и ещё меньшее количество (0,003 %) находится в живых организмах. Исключительно важна роль воды в возникновении и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды. Вода является важнейшим веществом для всех живых существ на планете Земля.
Химический состав воды
Вода (оксид водорода) — бинарное неорганическое соединение с химической формулой Н2O. Молекула воды состоит из двух атомов водорода и одного — кислорода, которые соединены между собой ковалентной связью. При нормальных условиях представляет собой прозрачную жидкость, не имеет цвета (в малом объёме), запаха и вкуса. В твёрдом состоянии называется льдом (кристаллы льда могут образовывать снег или иней), а в газообразном — водяным паром. Вода также может существовать в виде жидких кристаллов (на гидрофильных поверхностях). Составляет приблизительно около 0,05 массы Земли. Состав воды можно выяснить с помощью реакции разложения электрическим током. Образуется два объема водорода на один объем кислорода (объем газа пропорционален количеству вещества): 2H2O = 2H2↑ + O2↑ Вода состоит из молекул. Каждая молекула содержит два атома водорода, соединенные ковалентными связями с одним атомом кислорода. Угол между связями около 105º.
ОГЛАВЛЕНИЕ
Введение.......................................................................................................... 3 1. Состав и свойства нефти............................................................................. 4 1.1 Парафиновые углеводороды метанового ряда....................................... 7 1.2 Нафтеновые углеводороды этиленового ряда......................................... 8 1.3 Ароматические углеводороды бензольного ряда................................... 9 2. Состав и свойства природного газа......................................................... 10 2.1 Газовый конденсат.................................................................................. 12 3. Состав и свойства газовых гидратов........................................................ 14 3.1 Образование газовых гидратов.............................................................. 14 3.2 Строение гидратов.................................................................................. 17 4. Состав и свойства воды............................................................................. 21 4.1 Химический состав воды......................................................................... 21 4.2 Физико - химические свойства воды...................................................... 22 5. Состав и свойства пластовых вод............................................................. 23 Список использованных источников и литературы.................................... 27
ВВЕДЕНИЕ
Флюиды (от латинского fluidus – текучий) – любые вещества, поведение которых при деформации может быть описано законами механики жидкостей. Термин введен в науку в 17 веке для обозначения гипотетических жидкостей, с помощью которых объясняли некоторые физические явления и образование горных пород. С развитием науки понятие «флюиды» изменилось. Реологическими и геологическими исследованиями доказано, что все реальные тела под действием длительных тангенциальных нагрузок ведут себя как жидкости. В геологических процессах, длительность которых измеряется миллионами лет, в качестве флюидов могут выступать не только газы,водные растворы, нефть, ил, магма, но и глины, соли, ангидриты, известняки и другие твердые вещества. Основными компонентами промышленной органической химии являются углеводороды. Углеводородное сырье становится основой для получения производных составляющих углеводородов. Углеводородным сырьем считают углеводороды природного происхождения и продукты, прошедшие процесс переработки. При типировании к углеводородному сырью относят следующие вещества: · Нефть · Природный газ · Газовый конденсат В данной работе мы рассмотрим только химико–физические свойства, по большей части химические свойства углеводородного сырья, воды, пластовых вод и газогидратов.
Состав и свойства нефти
Нефть представляет собой комбинацию углеводородов в различных пропорциях, является полезным ископаемым. Физическими признаками являются жидкое состояние, маслянистость, специфичный запах, горючесть. Относится к ископаемым, находящимся в осадочных породах. Цвет нефти может различаться от грязно-коричневого до чисто черного, при этом встречаются месторождения с бесцветной или ярко-зеленой жидкостью. Нефть представляет собой весьма сложное минеральное вещество. Она не образует самостоятельного пласта, а заполняет пустоты в породах, принимает форму залегания вмещающих ее пород. Как правило, нефти небольшой относительной плотности обладают более светлой окраской, а большой - имеют темный и даже черный цвет и более вязки. Запах может варьироваться от приятного до насыщенно-тяжелого. Физические показатели нефти определяются наличием в ее составе примесей азота, серы или кислорода, остающихся в масле и нефтяном остатке. С конца ХХ века и до настоящего момента нефть считается ключевым полезным ископаеым, имеющим определяющую роль в экономике и производстве. Впервые была изучена пенсильванская нефть Северо-Американского нефтеносного бассейна, в которой немецкий ученый К. Шорлеммар (1834— 1892) обнаружил предельные углеводороды метанового ряда. Исчерпывающее объяснение строения углеводородов дал А.М. Бутлеров (1861), а основоположником науки о нефти принято считать Д.И. Менделеева. В большинстве случаев содержание углерода в нефти различных месторождений составляет 84-87%, а содержание водорода - 12-14%. На долю этих двух элементов приходится 97-99% всего состава нефти. Наиболее часто встречающаяся примесь - сера (до 7%), хотя во многих нефтях серы практически нет. Сера содержится в нефтях в чистом виде (самородная), в виде сероводорода или меркаптанов. Она усиливает коррозию металлов. Азота в нефтях не больше 1,7%, он совершенно безвреден в силу своей инертности. Кислород встречается в нефти не в чистом виде, а в различных соединениях (кислоты, фенолы, эфиры и т.д.) Его в нефти не более 3,6%. Каких-либо закономерностей в соотношении углерода и водорода не установлено. Из металлов в нефти присутствуют железо, магний, алюминий, медь, натрий, олово, кобальт, хром, германий, ванадий, никель, ртуть и другие. Содержание металлов столь мало, что они обнаруживаются лишь в золе, остающейся после сжигания нефти. По содержанию серы нефти подразделяют на малосернистые с содержанием серы до 0,5% и на высокосернистые с содержанием серы более 0,5%. Присутствие серы в нефтях нежелательно, так как она разъедает нефтеперегонную аппаратуру, нефтепроводы и придает нефти неприятный запах. В составе нефти всегда присутствуют в относительно большем или меньшем количестве асфальтены и смолы. Асфальтены - это высокомолекулярные органические соединения, содержащие коме углерода и водорода серу и кислород. По внешнему виду представляют собой бурые или черные аморфные порошки. Смолы - это полужидкие, иногда почти твердые, тягучие темно-желтые или темно-коричневые вещества с относительной плотностью несколько выше единицы; по своим химическим свойствам очень напоминают асфальт. По содержанию асфальтенов и смол нефти подразделяют на малосмолистые с содержанием смол менее 8%; смолистые с содержанием смол 8-28%; сильно смолистые с содержанием смол более 28%. Основные физические свойства нефти - относительная плотность, вязкость, температура кипения, теплота сгорания, растворимость, электрические и оптические свойства. Нефти подразделяют на легкие и тяжелые. Нефти с относительной плотностью менее 0,9 считаются легкими, с плотностью 0,9 и более - тяжелыми. Различие плотности нефтей объясняется, прежде всего их химической природой, а также зависит от количества растворенного в них газа: чем больше количество газа в нефти, тем меньше ее плотность. Вязкость, или внутреннее трение, - это свойство жидкости оказывать сопротивление перемещению ее частиц относительно друг друга под влиянием приложенной силы. существенное влияние на вязкость оказывают температура, давление и факторы химического характера. Вязкость жидкостей с повышением температуры уменьшается, а с повышением давления возрастает. Наибольшей вязкостью обладают ароматические углеводороды, далее следуют нафтены, затем парафины. Нефть не имеет определенной температуры кипения, поэтому для нее различают начальную и конечную температуру кипения. Чем меньше плотность нефти, тем при более низкой температуре она закипает. Теплота сгорания нефтей колеблется в пределах 10300-10800 ккал. Чем меньше плотность нефти, тем выше ее теплота сгорания. Нефть и ее дистилляты растворяются в воде в ничтожно малом количестве. Например, вода растворяет 0,027% керосина, т. е. 1 м3 воды может растворить только 270 грамм керосина. Нефть и нефтепродукты хорошо растворяются в органических растворителях: бензоле. хлороформе, сероуглероде, эфире. На этом свойстве основано определение нефтенасыщенности пород путем получения из них нефтяных вытяжек. Нефть и ее производные по отношению к электрическому току являются изоляторами. Сопротивление, которое она оказывает прохождению электрического тока, весьма велико и на изменении этого свойства нефтей основано применение электрокаротажа скважин. В зависимости от преобладания в нефти одного из трех представителей групп углеводородов в количестве более 50% нефти именуются метановыми, нафтеновыми, ароматическими. Если к доминирующему присоединяется другой углеводород в количестве не менее 25 %, то им дают комбинированное название, например метанонафтеновые. Парафиновые углеводороды метанового ряда отличаются наибольшим содержанием водорода. Нафтеновые углеводороды этиленового ряда содержат меньше водорода. Ароматические углеводороды бензольного ряда - еще меньше водорода. Чистые классы нефтей парафиновых, нафтеновых и ароматических в природе не встречаются. В большинстве случаев нефти представляют собой смешанные типы с преобладанием того или иного класса.
Парафиновые углеводороды метанового ряда
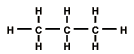
Наиболее распространены в природных условиях углеводороды метанового ряда: метан СН4, этан С2Н6, пропан С3Н8 и др. Эти углеводороды называют также предельными или насыщенными, что подчеркивает их небольшую химическую активность, а также плохую способность вступать в соединение с атомами других веществ.
Рисунок 1.1.1 Метан, этан, пропан.
Метановые — наиболее простые по строению, получившие свое название от самого простейшего из всех углеводородов — метана. Структурная формула метана напоминает простейшее из живых существ — амебу. Только у метана вместо ядра — атом углерода, а протоплазму образуют 4 атома водорода. Каждый следующий углеводород имеет на 1 атом углерода больше, т. е. структурная формула алканов имеет вид: СnН2n+2. Как бы не вытягивалась цепочка углеводородов, она всегда будет окружена водородной оболочкой. В нефти встречаются почти все члены этого ряда: СН4 — С4Н10 — газы; С5Н12 — С17Н36 — жидкости; начиная с С18Н38 — могут находиться в нефти в виде кристаллов и входят в состав парафинов. Отсюда еще одно название углеводородов — парафиновые. Названия первых 10 членов по порядку: метан, этан, пропан, бутан, пентан, гексан, гептан, октан, нонан, декан. Начиная с четвертого углеводорода — бутана, все имеют несколько разновидностей — изомеров. Молекулы их построены по-разному, хотя химическая формула одинакова. Если основной член ряда имеет вид простой цепочки, то у изомеров цепь ветвится. Различаясь по структуре, по прочности связей, изомеры отличаются и свойствами. Углеводороды от метана до бутана (С4Н10) включительно при атмосферном давлении находятся в газообразном состоянии. Из них состоит нефтяной газ. Углеводородные соединения, содержащие от 5 до 17 атомов углерода в молекуле (С5Н12—C17H36) — жидкие вещества. Эти соединения входят в состав нефти. Углеводороды, в молекулах которых имеется свыше 17 атомов углерода, относятся к твердым веществам. Это парафины и церезины, содержащиеся в тех или иных количествах во всех нефтях. По содержанию парафинов нефти подразделяют на беспарафиновые - с содержанием парафина до 1%; слабо парафиновые - с содержанием парафина 1-2%; парафиновые - с содержанием парафина свыше 2%.
|
|||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-25; просмотров: 1313; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.2 (0.014 с.) |