
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение фактора эквивалентностиСодержание книги Поиск на нашем сайте
Фактор эквивалентности определяется: 1) природой вещества, 2) конкретной химической реакцией.
а) в обменных реакциях; КИСЛОТЫ Величина z фактора эквивалентности кислот определяется числом атомов водорода, которые могут быть замещены в молекуле кислоты на атомы металла. Пример 1. Определить факторы эквивалентности для кислот: а) НСl, б) Н2SO4, в) Н3РО4; г) Н4[Fe(CN)6]. Решение. а) z =1, фактор эквивалентности – 1; б) z =2; Фактор эквивалентности - в) z =3; фактор эквивалентности - г) z =4; фактор эквивалентности - В случае многоосновных кислот фактор эквивалентности зависит от конкретной реакции: а) H2SO4 + 2KOH → K2SO4 + 2H2O. в этой реакции в молекуле серной кислоты замещается два атома водорода, следовательно, z =2, фактор эквивалентности - б) Н2SO4 + KOH → KHSO4 + H2O. В этом случае в молекуле серной кислоты замещается один атом водорода, z =1, фактор эквивалентности – 1. Для фосфорной кислоты, в зависимости от реакции, значения факторов эквивалентности могут быть: 1, ОСНОВАНИЯ Величина z основания определяется числом гидроксидных групп, которые могут быть замещены на кислотный остаток. Пример 2. Определить факторы эквивалентности оснований: а) КОН; б) Cu(OH)2; в) La(OH)3. Решение. а) z =1, фактор эквивалентности – 1; б) z =2, фактор эквивалентности – в) z =3, фактор эквивалентности – Фактор эквивалентности многокислотных оснований может изменяться в зависимости от количества замещенных групп (также как и у кислот). Например, для гидроксида латана возможны значения фактора эквивалентности – 1, СОЛИ Значения факторов эквивалентности солей определяются по катиону. Величина z в случае солей равна q·n, где q – заряд катиона металла, n – число катионов в формуле соли. Пример 3. Определить фактор эквивалентности солей: а) KNO3; б) Na3PO4; в) Cr2(SO4)3; г) Al(NO3)3. Решение. а) z = q· n = 1, фактор эквивалентности – 1; б) z = 1·3 = 1, фактор эквивалентности – в) z = 3·2 = 1, фактор эквивалентности – г) z = 3·1 = 1, фактор эквивалентности – Значение факторов эквивалентности для солей зависит также и от реакции, аналогично зависимости его для кислот и оснований.
б) в окислительно-восстановительных реакциях для определения факторов эквивалентности используют схему электронного баланса. Число z для вещества в этом случае равно числу принятых или отданных электронов молекулой вещества. К2Cr2O7 + HCl → CrCl3 + Cl2 + KCl + H2O
реакции 2Cl-- 2∙1
для обратной 2Cr+3-2∙3 реакции Cl2-2
Молярная концентрация эквивалента (нормальная концентрация или нормальность) С(
Пример: 1,0 Н – однонормальный раствор, т. е. С(
Молярная концентрация эквивалента всегда больше молярной концентрации в z раз.
4) Титр раствора Т(х) – величина, измеряемая массой растворенного вещества в 1 мл раствора или величина, измеряемая отношением массы вещества к объему раствора.
5) Моляльная концентрация вещества (моляльность) Сm(х) или в(х) – величина, измеряемая отношением количества вещества к массе растворителя.
6) Молярная доля вещества в растворе N(х) или Х(х) – величина, измеряемая отношением числа молей вещества в растворе к сумме числа молей вещества в растворе и числа молей растворителя.
Методы определения СОСТАВА раствора
1) Метод денсиметрии – измерение плотности раствора ареометром. Ареометр представляет поплавок с дробью или ртутью и узким отростком – трубкой, в которой находится шкала с делениями. Он погружается в различных жидкостях на различную глубину. При этом он вытесняет объемы этих жидкостей одной и той же массы, равной массе ареометра, а следовательно, обратно пропорциональные их плотности. То деление шкалы, до которого ареометр погружается в жидкость, показывает плотность этой жидкости.
2) Титрование.
|
|||||||
|
Последнее изменение этой страницы: 2019-05-20; просмотров: 3577; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.009 с.) |

 ;
; ;
; .
.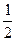 ;
;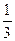 .
. ,
,  .
. ;
;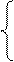 для прямой 2Сr+6+2∙3
для прямой 2Сr+6+2∙3 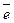 →2Cr3+
→2Cr3+
 (K2Cr2O7)=
(K2Cr2O7)=  (
( .
. .
. .
. .
.
 .
.


