
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Контроль и корректирование цинк-фосфатного раствора.Содержание книги
Поиск на нашем сайте
1.1. При контроле определяют общую и свободную кислотности, массовые концентрации азотистокислого натрия и цинка. 1.2. Свободную кислотность определяют титрованием 10 см3 раствора раствором гидроокиси натрия молярной концентрацией 0,1 моль/дм3 с индикатором метиловым оранжевым. Общую кислотность определяют титрованием 1.0 см3 раствора раствором гидроокиси натрия молярной концентрацией 0,1 моль/дм3 с индикатором фенолфталеином. Количество сантиметров кубических щелочи, израсходованное на титрование, выражают в условных единицах-«точках». 1.3. Для определения массовой концентрации цинка 10 см3 раствора помещают в коническую колбу вместимостью 150-200 см3, добавляют 50-60 см3 дистиллированной воды, нейтрализуют несколькими каплями 25%-ного водного раствора аммиака, добавляют индикатор метиловый красный, 10-15 см3 буферной смеси (рН 10-11), 3-4 капли индикатора хрома темно-синего. и титруют раствором трилона Б молярной концентрацией 0,05 моль/дм3 до изменения цвета от вишневого до синего. Массовую концентрацию цинка (Сzn2+), кг/м3, вычисляют по формуле: где 0,00327 - масса цинка, эквивалентная 1 см3 раствора трилона Б молярной концентрацией 0,05 моль/дм3, г; V 1 - объем трилонаБ, израсходованный на титрование, см3; V 2 - объем раствора, см3. 1.3а. Для определения суммарной массовой концентрации цинка и никеля 10 см3 отфильтрованного и охлажденного фосфатирующего раствора помещают в коническую колбу вместимостью 250 см3, добавляют 50 см3 дистиллированной воды, 10-15 см3 раствора гидроокиси натрия молярной концентрацией 0,1 моль/дм3, 20 см3 буферного раствора с рН=10,0-10,2, 25 см3 раствора трилона Б молярной концентрацией 0,01 моль/дм3, 20-30 капель индикатора хромогена черного ЕТ-00, затем кипятят в течение 5 мин до изменения цвета от синего до зеленого. Раствор охлаждают до температуры (25±10)°С и титруют раствором сернокислого магния молярной концентрацией 0,0l моль/дм3 до изменения цвета от зеленого до красного. Разность объемов раствора трилона Б молярной концентрацией 0,01 моль/дм3, добавленного в раствор, и раствора сернокислого магния молярной концентрацией 0,01 моль/дм3, израсходованного на титрование, условно выражает суммарную массовую концентрацию цинка (Zn2+) и никеля (Ni2+) в растворе. 1 см3 раствора трилона Б молярной концентрацией 0,01 моль/дм3 соответствует массовой концентрации 0,0628 кг/м3 цинка и никеля в растворе.
(Введен дополнительно, Изм. № 1). 1.4. Для определения массовой концентрации азотистокислого натрия 100 см3 охлажденного и отфильтрованного раствора помещают в коническую колбу вместимостью 250 см3, добавляют 10-20 капель 50%-ного раствора серной кислоты и титруют раствором марганцовокислого калия молярной концентрацией 0,02 моль/дм3 до появления розового цвета, устойчивого в течение 15-20 с. Массовую концентрацию азотистокислого натрия (СNaNO2), кг/м3, вычисляют по формуле: где 0,00345 - масса азотистокислого натрия, эквивалентная 1 см3 раствора марганцовокислого калия молярной концентрацией 0,02 моль/дм3, г; V1 - объем марганцовокислого калия, израсходованный на титрование, см3, «точки»; V2 - объем раствора, см3. Допускается массовую концентрацию азотистокислого натрия определять титрованием определенного количества марганцовокислого калия (V1), рабочим раствором (V2) до исчезновения розовой окраски. (Измененная редакция, Изм. № 2). 1.5. Корректирование фосфатирующего раствора КФ-1 проводят только концентратом КФ-1 из расчета, что 0,203 кг на 100 дм3 раствора повышает общую кислотность на «точку». (Измененная редакция, Изм. № 1, 3). 1.6. Корректирование фосфатирующего раствора типа КФ-3 из-за снижения кислотности в процессе работы проводят концентратом КФ-1 из расчета, что 0,296 кг на 100 дм3 раствора повышает общую кислотность на «точку». (Измененная редакция, Изм. № 1). 1.6а. Корректирующий концентрат вводят непрерывно через дозирующий насос с подачей (Q), дм3/ч, определяемой по формуле: где S - площадь изделий, обрабатываемых за 1 ч, м2; Р - удельный расход корректирующего фосфатирующего концентрата, определяемый из табл. 1, дм3/м2. Таблица 1
(Введен дополнительно. Изм. № 1). 1.7. При восполнении потерь фосфатирующего раствора типа КФ-3; связанных с уносом изделиями, с очисткой от шлама, добавляют воду и концентрат КФ-3 из расчета, что 0,296 кг на 100 дм3 раствора повышает общую кислотность на «точку».
1.8. Подачу 10%-ного раствора азотистокислого натрия при фосфатировании раствором КФ-1 методом погружения (V) вычисляют по формуле: где CNaNO2 - массовая концентрация азотистокислого натрия, кг/м3; 0,21 - коэффициент, характеризующий количество азотистокислого натрия, разлагающегося за 1 с; V-вместимость ванны фосфатирования, м3; 0,16 - коэффициент, рассчитанный по окислительно-восстановительной реакции, протекающей между азотистокислым натрием и Fe2+; GFe2+ - масса железа, растворяющаяся при фосфатировании, равная 1,5-10-3, кг/м2; S - площадь поверхности изделий, обрабатываемых за 1 ч, м2; 0,1 - массовая концентрация азотистокислого натрия в растворе для корректирования, кг/дм3. 1.9. Подачу 10%-ного раствора азотистокислого натрия при фосфатировании раствором КФ-1 методом распыления (V), л/ч; вычисляют по формуле: где CNaNO2 - массовая концентрация азотистокислого натрия, кг/м3; V - вместимость ванны фосфатирования м3; 0,5 - коэффициент, характеризующий количество азотистокислого натрия, разлагающегося за 1 ч; 0,785 - коэффициент, рассчитанный по окислительно-восстановительной реакции, протекающей между азотистокислым натрием и Fe2+; GFe2+ - масса железа, растворяющаяся при фосфатировании, равная 2×10-3, кг/м2; S - площадь поверхности изделий, обрабатываемых за 1 ч, м2; 0,1 - массовая концентрация азотистокислого натрия в растворе для корректирования, кг/дм3. 1.10. Массовую концентрацию виннокислого калия-натрия в растворе для корректирования ( где СNaNO2 - массовая концентрация азотистокислого натрия в растворе, кг/м3; К - содержание азотистокислого виннокислого натрия и калия-натрия в растворе, вычисляемого по формуле: где Р -расход виннокислого калия-натрия, равный (1,0-1,2) 10-3, кг/м2; СNaNO2 - массовая концентрация азотистокислого натрия, кг/м3; V - вместимость ванны, фосфатирования, м3; 0,5 - коэффициент, характеризующий количество азотистокислого натрия, разлагающегося за 1 ч; 0,785 - коэффициент, рассчитанный по окислительно-восстановительной реакции, протекающей между азотистокислым натрием и Fe2+; GFe2+ - поверхностная площадь растворившегося железа равна 2-10-3, кг/м2; S - площадь поверхности изделий, обрабатываемых за один час, м2/ч.
|
||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-17; просмотров: 636; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.190.176.244 (0.008 с.) |

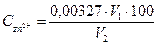 ,
, ,
, ,
, ,
, ,
, ) кг/м3, вычисляют по формуле:
) кг/м3, вычисляют по формуле: ,
, ,
,


