
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Виды стационарных состояний.Содержание книги
Поиск на нашем сайте
1. Основное стационарное состояние (S0, Т0). Частица не подвергается внешним воздействиям. 2. Возбуждённое стационарное состояние (S*, Т*).
Синглетное состояние (S): все электроны спарены, т.е. имеют попарно антипараллельные спины: Триплетное состояние (Т): имеется два неспаренных электрона – с параллельными и однонаправленными спинами:
Основное состояние большинства органических молекул – синглетное. При возбуждении также осуществляется переход на синглетный возбуждённый уровень. Заселение триплетного возбуждённого уровня происходит путём растраты части энергии синглетного возбуждённого уровня в тепло, следовательно, триплетный уровень всегда расположен ниже соответствующего синглетного.
Любые переходы между S и Т уровнями связаны с переменой направления (обращением) спина. А это процесс возможный, но очень маловероятный (запрещён по спину). Поэтому концентрация триплетно возбуждённых молекул всегда меньше концентрации синглетно возбуждённых молекул, а время жизни (продолжительность существования), наоборот:
Способы расходования молекулой энергии возбуждения.
Переходы с верхних уровней на нижние могут быть безизлучательные и излучательные. Способы безизлучательного перехода: 1. Растрата энергии в виде тепла: А* → А0 + тепло. Так растрачивается энергия высших возбуждённых уровней. 2. Вступление возбуждённой молекулы в химическую реакцию – фотобиологический процесс: А* → продукты. 3. Передача энергии возбуждения окружающим молекулам: А* + В → А + В*.
Излучательный переход – это переход с высвечиванием квантов излучения – люминесценция: А* → А0 +
Виды люминесценции: 1. Спонтанная (самопроизвольная) 2. Вынужденная (индуцированная)
В зависимости от способа предварительного возбуждения молекулы: 1. Фотолюминесценция (светом) 2. Электролюминесценция (электрическим полем или током) 3. Хемилюминесценция (в результате химической реакции)
По механизму излучения: 1. Флуоресценция 2. Фосфоресценция
Флуоресценция – испускание кванта излучения при переходе с первого синглетного возбуждённого уровня на основной (чрезвычайно малая длительность 10-9 – 10-6 с):
Фосфоресценция (послесвечение) – испускание фотона при переходе с триплетного возбуждённого уровня на основной (затухает 10-3 – 10 с):
Диаграмма состояний – схема, на которой представлены основные типы переходов между энергетическими уровнями.

a, a1 – переходы с поглощением энергии b, e – растрата энергии в тепло c – флуоресценция f – фосфоресценция d, g – все виды безизлучательных переходов
Спектры поглощения и люминесценции.
У каждого вещества – характерная система энергетических уровней, поэтому излучения разных длин волн испускаются и поглощаются по-разному. Следовательно, спектральный состав испускаемого и поглощаемого излучения – важнейшая характеристика вещества.
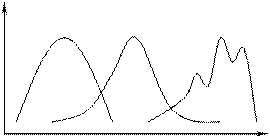
Спектр поглощения – зависимость оптической плотности образца от длины волны падающего света: Спектр люминесценции – зависимость интенсивности люминесценции от длины волны люминесценции: Так как часть энергии высших возбуждённых уровней растрачивается в виде тепла, кванты люминесценции меньше поглощённых квантов. Соответственно, длина волны люминесценции больше длины волны поглощённого излучения. Так как триплетный уровень расположен ниже синглетного, кванты фосфоресценции меньше квантов флуоресценции, а длина волны фосфоресценции больше длины волны флуоресценции. Поэтому для спонтанной люминесценции справедливо правило Стокса: спектры флуоресценции и фосфоресценции сдвинуты в сторону больших длин волн относительно спектра поглощения того же вещества.
Интенсивность люминесценции зависит также от длины волны падающего (возбуждающего люминесценцию) света. Отношение интенсивности люминесценции Спектр возбуждения люминесценции – зависимость относительной интенсивности люминесценции от длины волны возбуждающего света:
|
||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 461; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.105.40 (0.009 с.) |





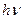


 , и
, и  .
.
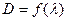 .
.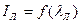 .
.
 к интенсивности падающего света
к интенсивности падающего света  - относительная интенсивность люминесценции.
- относительная интенсивность люминесценции.



