
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Квантово-механическая модель атома водородаСодержание книги
Поиск на нашем сайте
Двойственная природа электрона. В 1905 г. А. Эйнштейн предсказал, что любое излучение представляет собой поток квантов энергии, называемых фотонами. Из теории Эйнштейна следует, что свет имеет двойственную (корпускулярно-волновую) природу. В 1924 г. Луи де Бройль (Франция) выдвинул предположение, что электрон также характеризуется корпускулярно-влновым дуализмом. Позднее это было подтверждено на опытах по дифракции на кристаллах. Де Бройль предложил уравнение, связывающее длину волны λ электрона или любой другой частицы с массой m и скоростью ν, Волны частиц материи де Бройль назвал материальными волнами. Они свойственны всем частицам или телам. Однако, как следует уравнения (1.5), для макротел длина волны настолько мала, что в настоящее время не может быть обнаружена. Так, для тела с массой 1000 кг, двигающегося со скоростью 108 км/ч (30 м/с) λ = 2,21·10-38 м. В 1927 г. В. Гейзенберг (Германия) постулировал принцип неопределенности, согласно которому положение и импульс движения субатомной частицы (микрочастицы) принципиально невозможно определить в любой момент времени с абсолютной точностью. В каждый момент времени можно определить только лишь одно из этих свойств. Э. Шредингер (Австрия) в 1926 г. вывел математическое описание поведения электрона в атоме. Работы Планка, Эйнштейна, Бора, де Бройля, Гейзенберга, а также Шредингера, предложившего волновое уравнение, заложили основу квантовой механики, изучающей движение и взаимодействие микрочастиц. Орбиталь. В соответствие с квантово-механическими представлениями невозможно точно определить энергию и положение электрона, поэтому в квантово-механической модели атома используют вероятностный подход для характеристики положения электрона. Вероятность нахождения электрона в определенной области пространства описывается волновой функцией ψ, которая характеризует амплитуду волны, как функцию координат электрона. В наиболее простом случае эта функция зависит от трех пространственных координат и называется орбиталью. В соответствии с определением ψ, орбиталью называется область пространства, в котором наиболее вероятно нахождение электрона. Необходимо заметить, что понятие орбиталь существенно отличается от понятия орбита, которая в теории Бора означала путь электрона вокруг ядра атома. Величина области пространства, которую занимает орбиталь, обычно такова, чтобы вероятность нахождения электрона внутри нее составляла не менее 95 %. Так как электрон несет отрицательный заряд, то его орбиталь представляет собой определенное распределение заряда, которое получило название электронного облака. Квантовые числа. Для характеристики поведения электрона в атоме введены квантовые числа: главное, орбитальное, магнитное и спиновое. Главное квантовое число n определяет энергию и размеры электронных орбиталей. Главное квантовое число принимает значения 1,2,3,4,5,… и характеризует оболочку или энергетический уровень. Чем больше n, тем выше энергия. Оболочки (уровни) имеют буквенные обозначения: К (n = 1), L (n = 2), M (n = 3), N (n = 4), Q (n = 5), переходы электронов с одной оболочки (уровня) на другую сопровождаются выделение квантов энергии, которые могут проявиться в виде спектров (см. рис. 1.1). Орбитальное квантовое число l определяет форму атомной орбитали. Электронные оболочки расщеплены на подоболочки, поэтому орбитальное квантовое число также характеризует энергетические подуровни в электронной оболочке атома. Орбитальные квантовые числа принимают целочисловое значение от 0 до (n-1). Подоболочки также обозначаются буквами: Подоболочка (подуровень)…………………s p d f Орбитальное квантовое число, l ……………0 1 2 3 Электроны с орбитальным квантовым числом 0, называются s - электронами. Орбитали и соответственно электронные облака имеют сферическую форму (рис. 1.2). Электроны с орбитальным квантовым числом 1называются p - электронами. Орбитали и соответственно электронные облака имеют форму, напоминающую гантель (рис. 1.2). Электроны с орбитальным квантовым числом 2 называют d – электронами. Орбитали имеют форму четырехлепестковой розетки (рис. 1.2). Электроны с орбитальным квантовым числом 3 получили название f – электронов. Форма их орбиталей еще сложнее, чем форма d – орбиталей. В первой оболочке (n=1) может быть одна (s–), во второй (n=2) две (s- и p-), в третьей (n=3) – три (s-, p-, d-), в четвертой (n=4) – четыре (s-, p-, d-, f-)-подоболочки. Магнитное квантовое число m l характеризует положение орбитали в пространстве (см. рис. 1.2).
Соответственно в подоболочке s (l = 0) имеется одна орбиталь (m l = 0), в подоболочке р (l = 1) – три орбитали (m l = -1, 0, +1), в подоболочке d (l = 2) пять орбиталей (m l = -2, -1, 0, +1, +2). Атомная орбиталь. Каждая электронная орбиталь в атоме (атомная орбиталь, АО) может характеризоваться тремя квантовыми числами n, l и ml. Условно атомную орбиталь обозначают в виде клеточки Соответственно для s-подоболочки имеется одна АО Спиновое квантовое число
|
||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 148; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.11 (0.007 с.) |

 . (1.5)
. (1.5)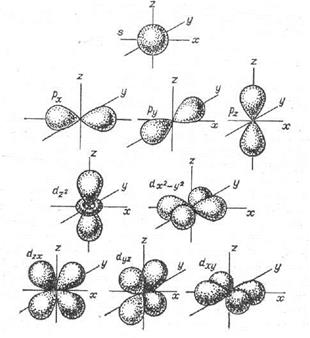 Рис. 1.2. Фрмы электронных облаков различных атомных орбиталей
Рис. 1.2. Фрмы электронных облаков различных атомных орбиталей
 .
.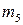 . Каждый электрон характеризуется собственным механическим моментом движения, который получил название спина. Соответствующие спину квантовое число имеет только 2 значения: +1/2 и -1/2. Положительные и отрицательные значения спина связаны с его направлением. Электроны с разными спинами обычно обозначаются противопложно напрвленными стрелками
. Каждый электрон характеризуется собственным механическим моментом движения, который получил название спина. Соответствующие спину квантовое число имеет только 2 значения: +1/2 и -1/2. Положительные и отрицательные значения спина связаны с его направлением. Электроны с разными спинами обычно обозначаются противопложно напрвленными стрелками 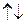 .
.


