
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
ЭДС окислительно-восстановительных реакций
Энергия Гиббса и ЭДС реакции связаны уравнением:
Знак «–» перед
Зная окислительно-восстановительные потенциалы, можем определить ЭДС:
Окислительно-восстановительная реакция возможна, когда электродвижущая сила реакции является положительной величиной: в этом случае изменение свободной энергии Окислительно-восстановительные реакции идут в сторону образования более слабых окислителей и восстановителей. Из всех возможных при данных условиях окислительно-восстановительных реакций в первую очередь протекает та, которая имеет наибольшую разность окислительно-восстановительных потенциалов. Кинетика электродных процессов. Равновесные потенциалы могут быть определены в условиях отсутствия в цепи тока. При прохождении электрического тока потенциалы электродов изменяются. Изменение потенциала электрода при прохождении электрического тока, называется поляризацией:
Поляризация может наблюдаться как на катоде, так и на аноде, поэтому различают катодную и анодную поляризации Изменение потенциала при прохождении тока также называется перенапряжением. Поляризация электрода в отрицательную сторону связана с протеканием процесса восстановления (катодная поляризация), а в положительную сторону – с протеканием процесса окисления (анодная). Для электролиза аналогично: при прохождении электрического тока изменяются потенциалы электродов электролизера, то есть возникает электродная поляризация. Вследствие катодной поляризации потенциал катода становится более отрицательным, а из-за анодной поляризации потенциал анода становится более положительным. Поэтому разность потенциалов при прохождении электрического тока
Поляризация электрода – необходимое условие протекания электродного процесса. Чем сильнее поляризован электрод, тем больше скорость соответствующей полуреакции. Если речь идет о катодном выделении водорода, то поляризацию называют перенапряжением водорода. Перенапряжение выделения водорода на различных металлах различно.
|
|||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 53; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.183.172 (0.004 с.) |
 , где
, где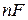 – количество электричества, прошедшее через элемент;
– количество электричества, прошедшее через элемент; – уменьшение свойств энергии Гиббса;
– уменьшение свойств энергии Гиббса; – количество электронов перемещающихся от восстановителя к окислителю;
– количество электронов перемещающихся от восстановителя к окислителю; – постоянная Фарадея;
– постоянная Фарадея;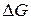 свидетельствует о возможности протекания реакции.
свидетельствует о возможности протекания реакции.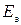 – ЭДС.
– ЭДС.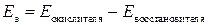 .
. , где
, где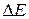 – поляризация;
– поляризация;  – потенциал электрода при прохождении электрического тока;
– потенциал электрода при прохождении электрического тока; 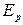 – равновесный потенциал.
– равновесный потенциал. и
и 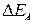 .
. при электролизе больше, чем разность равновесных потенциалов электродов
при электролизе больше, чем разность равновесных потенциалов электродов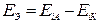 .
.


