Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Зависимость скорости химической реакции от концентрации реагирующих веществ
Необходимым условием того, чтобы между частицами (молекулами, ионами) исходных веществ произошло химическое взаимодействие, является их столкновение (соударение). Точнее говоря, частицы должны сблизиться друг с другом настолько, чтобы атомы одной из них испытывали бы действие электрических полей, создаваемых атомами другой. Только при этом станут возможны те переходы электронов и перегруппировки атомов, в результате которых образуются молекулы новых веществ – продуктов реакции. Поэтому скорость веществ пропорциональна числу соударений, которые претерпевают молекулы реагирующих веществ. Число соударений тем больше, чем выше концентрация каждого из исходных веществ. Зависимость скорости химической реакции от концентрации определяется законом действия масс: при постоянной температуре скорость химической реакции пропорциональна произведению концентраций реагирующих веществ, причем каждая концентрация входит в произведение в степени, равной коэффициенту, стоящему перед формулой данного вещества в уравнении реакции. Например, для реакции aA+bB=cC Обозначив концентрации веществ A и B через [A] и [B], можно записать кинетическое уравнение:
где a и b – коэффициенты в уравнении реакции, k – коэффициент пропорциональности, называемый константой скорости данной реакции. Величина константы скорости k зависит от природы реагирующих веществ, от температуры, от присутствия катализаторов, но не зависит от концентрации веществ. Аналогично для реакции: 2A+B=C или A+A+B=C можно записать как:
В качестве примера приложения закона действия масс можно привести уравнение зависимости скорости реакции окисления оксида азота (II): 2NO+ от концентрации NO и
Гетерогенные реакции протекают на границе раздела фаз (например, твердой и жидкой, жидкой и газообразной), которая и служит реакционным пространством. Если площадь поверхности равна S то общая скорость гетерогенной реакции описывается уравнением:
где с – концентрация реагента (газообразного или жидкого). Скорость гетерогенной химической реакции измеряется в [моль ∙ с-1]. Если в химической реакции непосредственно участвует твердое вещество, то в кинетическое уравнение не входит его концентрация, т.к. она постоянна. Роль твердого тела в кинетике отражается путем введения площади его поверхности (S).
Например,
кинетическое уравнение для этой реакции:
Особенности гетерогенных реакций: 1) Влияние площади реакционной поверхности на скорость реакции. 2) Скорость гетерогенной химической реакции зависит от скорости подвода реагента в зону химической реакции.
|
|||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 51; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.11.28 (0.004 с.) |
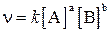 ,
,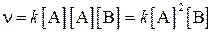
 =2
=2 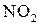

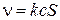 ,
,