

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Анаболическое значение катаболизма глюкозы.
Содержание книги
- Тема 2. 9. Применение ферментов в медицине
- Модуль 3 матричные биосинтезы
- Тема 3. 2. Биосинтез днк (репликация)
- III. Исключение праймеров. Завершение формирования отстающей цепи ДНК
- Тема 3. 4. Биосинтез рнк (транскрипция). Посттранскрипционные модификации рнк
- Тема 3. 5. Трансляция как механизм перевода генетической информации в фенотипические
- Тема 3. 6. Ингибиторы матричных биосинтезов: лекарственные препараты, яды и бактериальные токсины
- Тема 3. 7. Механизмы адаптивной регуляции активности генов у прокариотов и эукариотов
- Тема 3. 8. Механизмы, обеспечивающие разнообразие белков у эукариотов
- Тема 3. 9. Механизмы генетической изменчивости: эволюционная изменчивость, полиморфизм белков. Наследственные болезни
- Тема 3. 10. Использование рекомбинантных днк
- Использование техники рекомбинанатных днк для диагностики и лечения заболеваний
- Инактивация аденилатциклазы и протеинкиназы А
- Последовательность событий передачи сигнала первичных мессенджеров с помощью инозитолфосфатной системы
- Первый этап тканевого дыхания - дегидрирование различных субстратов, образующихся в реакциях катаболизма.
- Тема 5. 4. Сопряжение тканевого дыхания и синтеза атф
- В реакциях цпэ часть энергии не превращается в энергию макроэргических связей атф, А рассеивается в виде теплоты.
- Окислительное декарбоксилирование пирувата
- Кроме того, адф аллостерически активирует некоторые ферменты опк
- Тема 5. 12. Гипоэнергетические состояния
- Желудочный сок не содержит ферментов, расщепляющих пищевые углеводы. Амилаза слюны инактивируется в желудке, так как оптимальное
- Тема 6. 3. Синтез гликогена (гликогеногенез), мобилизация гликогена (гликогенолиз). Регуляция процессов
- Активация гликогенфосфорилазы адреналином посредством аденилатциклазной системы
- В аэробном и анаэробном гликолизе можно выделить два этапа.
- Тема 6. 6. Биологическое значение катаболизма глюкозы. Регуляция процесса
- Анаболическое значение катаболизма глюкозы.
- Тема 6. 7. Пентозофосфатный путь превращения
- А - окислительный этап; б - неокслительный этап в обратном направлении
- Тема 6. 9. Регуляция гликолиза и глюконеогенеза
- Регуляция активности пируваткиназы в печени осуществляется путем фосфорилирования (дефосфорилирования) в зависимости от ритма питания
- Структурная организация межклеточного матрикса (суставной хрящ, базальные мембраны, субэпителиальные слои)
- Гликозилирование лизина под действием гликозилтрансфераз прекращается по мере формирования трехспиральной структуры.
- Патологий, связанных с уменьшением эластичности сосудов. При недостаточной активности металлопротеиназ развивается фиброз тканей и неадекватный иммунный ответ.
- Хондроитинсульфат; 2 - кератансульфат; 3 - коровый белок; гк - гиалуроновая кислота
- Тема 7. 5. Структурная организация межклеточного матрикса (суставной хрящ, базальные мембраны, субэпителиальные слои)
- Регуляция процесса. Амф, гмф, имф, ди- и трифосфаты адениловых и гуаниловых нуклеотидов ингибируют ключевые реакции своего синтезааллостерически по механизму отрицательной обратной связи.
- Частым нарушением катаболизма пуринов является гиперурикемия, которая возникает, когда в плазме крови Концентрация мочевой кислоты превышает норму.
- Синтез цтф из утф осуществляет цтф-синтетаза, используя амидную группу глн и энергию атф для аминирования пиримидинового кольца.
- Тема 10. 3. Биосинтез дезоксирибонуклеотидов.
- Тема 10. 4. Механизмы действия противовирусных и противоопухолевых препаратов на ферменты синтеза рибо- и дезоксирибонуклеотидов
- И рецепторов. Особенно много сфинголипидов в нервной ткани, где они формируют миелиновые оболочки нейронов.
- Тема 8. 3. Хиломикроны - транспортная форма экзогенных жиров
- Модульная единица 2 биосинтез высших жирных кислот и жиров
- Реакции восстановления обеспечивают синтез насыщенного алифатического радикала жирных кислот
- Запасание жиров в жировой ткани - так называемое депонирование жиров - происходит в абсорбтивный период, когда увеличивается соотношение инсулин - глюкагон.
- Первичное ожирение развивается в результате алиментарного дисбаланса - избыточной калорийности питания по сравнению с расходами энергии.
- Модульная единица 3 жиры, жирные кислоты и кетоновые тела как источники энергии. Эйкозаноиды, Строение, синтез и биологические функции
- Скелетные мышцы и почки используют кетоновые тела даже при их низкой концентрации в крови.
- Выведение кетоновых тел, в том числе и ацетона, с мочой (кетонурия), потом выдыхаемым воздухом является способом выведения избытка кетоновых тел из организма и уменьшения таким образом ацидоза.
- Ацетильный остаток переносится с молекулы аспирина на oh-группу фермента и необратимо ингибирует его
Процесс катаболизма глюкозы, кроме энергетического значения, имеет также и анаболическое значение. Метаболиты гликолиза используются для синтеза ряда соединений. Так, фруктозо-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата - структурного компонента нуклеотидов; 3-фосфоглицерат может включаться в синтез аминокислот, таких как серин, глицин, цистеин. В печени и жировой ткани ацетил-КоА, образующийся из пирувата, используется как субстрат при синтезе жирных кислот, холестерола, а дигидроксиацетонфосфат как субстрат для синтеза глицерол-3-фосфата, необходимого для синтеза триацилглицеролов (ТАГ).
В гликолитическом пути может протекать дополнительная реакция, катализируемая бисфосфоглицератмутазой, превращающая 1,3-бисфосфо- глицерат в 2,3-бисфосфоглицерат (2,3-БФГ), который может при участии 2,3-бисфосфоглицератфосфатазы возвращаться в гликолиз в виде 3-фосфоглицерата (рис. 6.16).
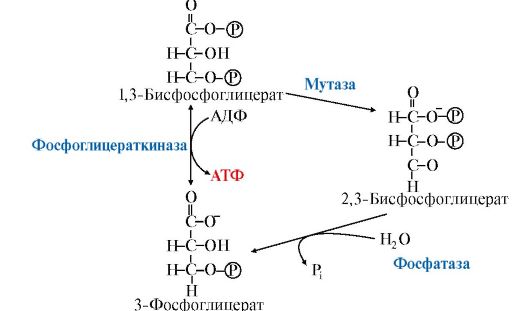 Рис. 6.16. Образование и катаболизм 2,3-бисфосфоглицерата Рис. 6.16. Образование и катаболизм 2,3-бисфосфоглицерата
В большинстве тканей 2,3-БФГ образуется в небольших количествах. В эритроцитах его содержание значительно, так как он выполняет роль аллостерического регулятора функции гемоглобина. 2,3-БФГ, связываясь с гемоглобином, понижает его сродство к кислороду, способствует его диссоциации и переходу в ткани (см. модуль 1).
Регуляция катаболизма глюкозы в скелетных мышцах. Основное значение гликолиза - синтез АТФ, поэтому его скорость должна коррелировать с затратами энергии в организме.
Большинство реакций гликолиза обратимы за исключением трех, катализируемых гексокиназой, фосфофруктокиназой и пируваткиназой.Регуляторные факторы, изменяющие скорость гликолиза, а значит, и образование АТФ, направлены на необратимые реакции. Показателем потребления АТФ является накопление АДФ и АМФ - продуктов распада АТФ.
Даже небольшой расход АТФ ведет к заметному увеличению АДФ и АМФ. Отношение уровня АТФ к АДФ и АМФ характеризует энергетический статус клетки, а его составляющие служат аллостерическими регуляторами скорости как общего пути катаболизма, так и гликолиза (рис. 6.17).
Существенное значение для регуляции гликолиза имеет изменение активности фосфофруктокиназы, поскольку этот фермент катализирует наиболее медленную реакцию процесса. Фосфофруктокиназа активируется АМФ, но ингибируется АТФ. АМФ, связываясь с аллостерическим центром фосфофруктокиназы, увеличивает сродство фермента к фруктозо-6-фосфату и повышает скорость его фосфорилирования.
Повышение уровня АТФ относительно АДФ снижает скорость этой реакции, поскольку АТФ в этих условиях действует как ингибитор: связывается с аллостерическим центром фермента, вызывает конформационные изменения и уменьшает его сродство к субстрату - фруктозо-6-фосфату.
Снижение активности фосфофруктокиназы при высоком уровне АТФ ведет к накоплению как фруктозо-6-фосфата, так и глюкозо-6-фосфата, а последний ингибирует гексокиназу. Гексокиназа во многих тканях (за исключением печени и β-клеток поджелудочной железы) ингибируется глюкозо-6-фосфатом.
При высоком уровне АТФ снижается скорость цикла лимонной кислоты и дыхательной цепи. В этих условиях процесс гликолиза также замедляется. Следует напомнить, что регуляция ферментов ОПК и дыхательной цепи связана с изменением концентрации таких ключевых продуктов, как NADH, АТФ и некоторых метаболитов. Так, увеличение концентрации NADH, в том случае, если снижается скорость его окисления в дыхательной цепи, ингибирует некоторые аллостерические ферменты цитратного цикла (см. модуль 5).
Физиологическая роль гликолиза в печени и жировой ткани несколько иная, чем в других тканях. В печени и жировой ткани гликолиз в период пищеварения функционирует в основном как источник субстратов для синтеза жиров. Регуляция гликолиза в печени имеет свои особенности и будет рассмотрена позже.
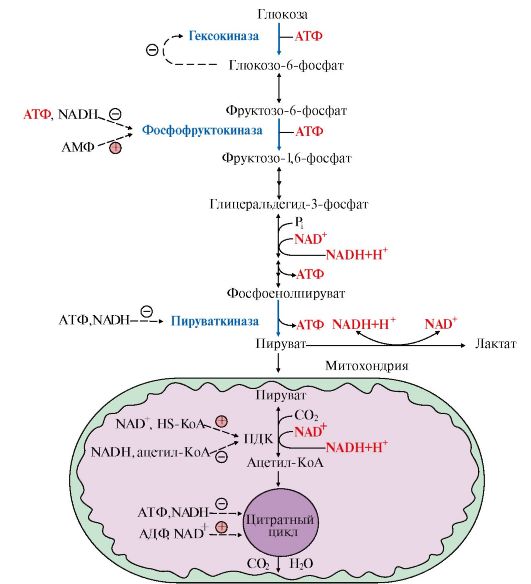 Рис. 6.17. Регуляция катаболизма глюкозы в скелетных мышцах Рис. 6.17. Регуляция катаболизма глюкозы в скелетных мышцах
|