Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Консультации других специалистов
При сложностях дифференциальной диагностики желательна консультация у генетика. Консультация у психолога для улучшения психосоциальной адаптации больных. Оценка эффективности лечения Лечение считают эффективным при достаточной феминизации фигуры, увеличении матки по данным эхографического исследования до возрастного норматива, восстановлении и стабилизации МПКТ, полной социальной адаптации. Дальнейшее ведение (наблюдение) Наблюдение за больными осуществляют до возраста физиологической менопаузы с ежегодным контролем уровня гормонов в сыворотке крови (уровень эстрадиола не менее 150 пмоль/л), состоянием органов-мишеней (эхографическое исследование молочных желёз, денситометрия). В первый год терапии исследование гормонального профиля крови и эхографию осуществляют каждые 3 мес, на второй год - 1 раз в 6 мес, далее - ежегодно. Глава 9. Синдром тестикулярной феминизации Определение СТФ, или синдром нечувствительности к андрогенам (androgen insensitivity syndrome - AIS), представляет собой полную или частичную нечувствительность тканей органов-мишеней к андрогенам, обусловленную нарушением связывающей способности рецептора андрогенов или пострецепторным дефектом. Данное заболевание входит в понятие XY-реверсии пола и относится к ложному мужскому гермафродитизму - состоянию, при котором у генетически мужской особи наблюдается женский фенотип, мужской гонадный и гормональный пол. Код по МКБ-10 Е34.5 Синдром андрогенной резистентности. Эпидемиология Частота встречаемости СТФ 1 на 20 000-70 000 ново- рождённых, это составляет 15-20% всех больных с ложным мужским гермафродитизмом и 5% по отношению ко всем формам нарушения половой дифференцировки. СТФ занимает по частоте третье место среди причин первичной аменореи у лиц с женским фенотипом после дисгенезии гонад и врождённой аплазии матки и влагалища (синдром РокитанскогоКюстера). Скрининг Принимая во внимание повышенный риск опухолевого перерождения половых желёз, а также серьёзные психологические проблемы, возникающие у больных с СТФ, живущих в женском паспортном поле, желательно введение определения полового хроматина как скрининговой методики лабораторного подтверждения пола всем новорождённым. Учитывая патогномоничность паховых грыж при данной патологии, необходимо проведение кариотипирования всем девочкам, имевшим в анамнезе операции по поводу паховых грыж.
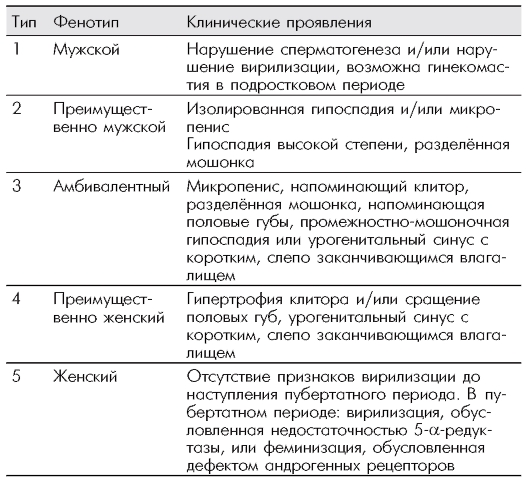
Классификация Существует два основных клинических варианта синдрома: ■ I - полная форма - синдром Морриса (пСТФ) при полном блоке рецепторного аппарата и полной нечувствительности тканей к влиянию андрогенов, при котором наружные половые органы имеют женский тип строения; ■ II - неполная форма (нСТФ) в случаях исходно неполного блока рецепторного аппарата или при спонтанной активации части рецепторов в пубертатном периоде, при которой наружные половые органы имеют разную степень маскулинизации. Принимая во внимание большую вариабельность фенотипов при СТФ - от фенотипической женщины с отсутствием полового оволосения до фенотипического мужчины, страдающего первичным бесплодием; некоторыми авторами были предложены варианты классификации фенотипов в зависимости от степени маскулинизации (андрогенизации) или феминизации наружных половых органов. Соответственно степени андрогенизации наружных половых органов Г.Х.Г. Синнескер и соавт. (1996; 1985; 1997) предложили свою классификацию фенотипов при ложном мужском гермафродитизме, в том числе и при СТФ (табл. 9.1). Таблица 9.1. Классификация фенотипов при ложном мужском гермафродитизме, включая синдром тестикулярной феминизации
Этиология и патогенез В основе заболевания лежат мутации гена рецептора андрогенов (AP), обусловливающие резистентность к тестостерону и дегидротестостерону. Одновременно выявляется снижение инсулиноподобных факторов роста I и II в фибробластах кожи половых органов, так как система инсулиноподобных факторов роста служит медиатором влияния андрогенов на рост тканей в андроген-зависимых клетках. Степень дефекта рецептора проявляется от полной утраты его активности до изменения качества связи с гормоном или нарушения связывания комплекса «стероидный гормон-рецептор» с ДНК. Если мутация гена АР не критическая, то она не приводит к полной потери функции рецептора, и формируется неполная форма СТФ (нСТФ). Полная форма СТФ ассоциирована с разными типами мутаций гена АР (структурные мутации, нонсенс-мутации, сплайсинг-мутации, миссенс-мутации), а неполная форма - только с миссенс-мутациями гена.
СТФ наследуется по Х-сцепленному рецессивному типу, при этом около 60% пациентов имеют семейный анамнез, и в одной семье можно наблюдать различные фенотипические проявления болезни. В процессе эмбриогенеза гонады при СТФ дифференцируются как полноценные функционирующие яички. Однако из-за дефекта гена АР у больных отсутствует чувствительность к андрогенам, ответственным за формирование мужского фенотипа (мужской уретры, простаты, полового члена и мошонки). При этом чувствительность к эстрогенам сохранена, и закономерно формируется женский фенотип при отсутствии, как правило, производных мюллеровых протоков (маточных труб, матки и верхней трети влагалища), так как продукция АМГ клетками Сертоли не страдает, в некоторых случаях рудименты маточных труб могут сохраняться. Патоморфология При морфологическом исследовании половые железы представлены семенниками, лишёнными сперматогенеза. Иногда отмечается уменьшенный диаметр семенных канальцев. Если у детей допубертатного возраста присутствуют только диффузные изменения в виде гиперплазии клеток Сертоли, то в постпубертатном периоде отмечается прогрессирующий гиалиноз канальцев, узловые и диффузные поражения семявыносящих протоков, в последующем возможно почти полное замещение тестикулярной ткани гамартоматозными (аденомоподобными) узлами. За счёт гиалинизации и агрегации недоразвитых тубулярных структур в гонадах могут определяться так называемые «белые тела», затрудняющие идентефикацию половой дифференцировки железы. Клетки Лейдига развиты, но неполноценные, достаточно часто имеется очаговая гиперплазия клеток Лейдига. В связи с изменённой структурой яичек частота их опухолевого перерождения повышена. Риск развития неоплазий у пациентов с СТФ в возрасте до 25-30 лет невелик, примерно 4%, но позже он увеличивается и достигает 33% к 50 годам. Чаще всего встречаемые опухоли яичек при СТФ - лейдигомы и сертолиомы (24%), аденоматоз встречается в 12%, реже диагностируют дисгерминомы и карциномы, иногда встречается опухоль, эквивалентная цистаденофиброме. Клиническая картина Клинически полная форма СТФ относится к «типу 5» соответственно классификации Г.Х.Г. Синнескер и характеризуется женским типом строения наружных половых органов, отсутствием матки, маточных труб и простаты, соматических аномалий развития, лобкового и аксиллярного оволосения, наличием слепо замкнутого влагалища и хорошо развитыми молочными железами (гинекомастия). Неполный вариант (к гинекологам, как правило, обращаются больные с 4-ым типом СТФ соответственно классификации Г.Х.Г. Синнескер) заболевания имеет сходство с полной формой СТФ за исключением признаков маскулинизации (вирилизации) наружных половых органов и наличия полового оволосения. Рост больных с СТФ, как правило, выше среднего, костный возраст соответствует календарному, конечности могут быть относительно длинными. Высокорослость некоторых больных - следствие недостаточности общего пула половых гормонов (в ус-
ловиях резистентности к андрогенам), обусловливающей позднее закрытие «зон роста» в пубертатном периоде, это характерно для большинства форм допубертатного гипогонадизма. Индекс таза к 18-19 годам жизни у больных с СТФ не достигает нормативных значений, принятых для женщин, а тазово-плечевой коэффициент имеет промежуточное, между мужскими и женскими нормативами, значение, это свидетельствует об интерсексуальном типе телосложения. Несмотря на хорошее внешнее развитие, в молочных железах пациенток с СТФ при нормально сформированных протоках часто наблюдают мелкие кисты и гиперплазию железистой ткани в сочетании с диффузным фиброзом стромы. Характерная особенность - бледная окраска недостаточно развитых сосков молочных желёз. Несмотря на соответствие календарного и биологического возраста, более чем у половины пациенток с данной патологией выявляют снижение МПКТ, в основном у больных с полной формой СТФ. При этом на фоне выявленной остеопении не наблюдают отклонения от нормы маркёров костного метаболизма и общей частоты переломов. Влагалище у больных с СТФ заканчивается слепо, его длина варьирует от 2,5 см при неполной форме до 5-8 см при полной форме синдрома. Половые железы могут быть расположены высоко в полости малого таза (у 86% больных с пСТФ), по ходу паховых каналов (по типу «скользящей грыжи») или локализоваться в толще больших половых губ. Паховое расположение яичек наблюдают у 77% больных с неполной и лишь у 20% с полной формой СТФ. Гормональный статус больных с СТФ характеризуется высоким уровнем гонадотропных гормонов с преимущественным повышением уровня ЛГ, начиная с пубертатного периода, высоким (для женщин) уровнем тестостерона и нормальным или низким для женщин, но умеренно повышенным (для мужчин) уровнем эстрадиола. Психологические особенности больных с СТФ - активная жизненная позиция, более высокая, чем у здоровых подростков обоего пола аналогичного возраста, способность к самостоятельному регулированию своей жизни, а также спутанность гендерных ролей при женском полоролевом поведении. Необходимо помнить, что на фоне смены гормонального пола в процессе лечения спутанность гендерных ролей у этих пациентов усугубляется. Осложнения Самое частое осложнение при СТФ - развитие опухолевого процесса в яичках. Другое возможное осложнение СТФ - гипертрофия гонадотрофов гипофиза и развитие аденомы, секретирующей ЛГ.
Диагностика Диагноз пСТФ может быть поставлен не раньше первого года жизни, а нСТФ - в первый месяц после рождения. Чаще всего пациентки с пСТФ впервые обращаются к врачу в пубертатном периоде по поводу первичной аменореи и отсутствия полового оволосения. Достаточно характерная клиническая картина (феминная фигура при первичной аменорее, отсутствие полового оволосения, слепо заканчивающееся влагалище, отсутствие матки, повышенный уровень ЛГ и тестостерона в сыворотке крови, мужской кариотип 46,XY) позволяет поставить правильный диагноз. При проведении эхографического исследования органов малого таза необходимо учитывать, что половые железы у данных пациенток располагаются высоко у внутренних отверстий паховых каналов или по ходу самих паховых каналов. МРТ информативна для выявления признаков начавшейся неопластической трансформации, но данный метод не всегда позволяет обнаружить яички неабдоминального расположения. В допубертатном периоде заподозрить наличие СТФ может помочь обнаружение яичек в паховых областях или половых губах, грыжевых мешках при грыжесечении. В связи с тем что наличие паховых грыж считается патогномоничным признаком для СТФ, рекомендуется проводить кариотипирование всем девочкам с паховыми грыжами в анамнезе. Распространённая ошибка хирургов при операции пахового грыжесечения - вправление обнаруженной в грыжевом мешке половой железы (тестикула), часто принимаемой за яичник, в брюшную полость. Для подтверждения диагноза проводят кариотопирование, пробу на резистентность к андрогенам и молекулярно-генетическое исследование, позволяющее выявить мутацию в гене АР. Проба на резистентность к андрогенам основана на биологическом эффекте анаболических андрогенных препаратов, например станозолола, снижать концентрацию секстероидсвязывающего глобулина, в современной трактовке обозначаемого тестостерон-эстрадиол-связывающий глобулин, в сыворотке крови. В норме после введения 0,2 мг/кг станозолола в течение 3 дней концентрация тестостерон-эстрадиол-связывающего глобулина в крови через 5-8 дней снижается наполовину. У пациенток с пСТФ такого снижения не происходит, а у пациенток с нСТФ концентрация тестостерон-эстрадиол-связывающего глобулина снижается в разной степени в зависимости от степени маскулинизации, но это снижение выражено в меньшей степени, чем в норме. Данная проба дополняет молекулярно-генетическое исследование, характеризуя степень дефекта рецепторного аппарата.
|
||||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 80; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.15.248 (0.008 с.) |