Окислительное дезаминирование аминокислот. Глутаматдегидрогеназа. Значение этой реакции.
Содержание книги
- Регуляция активности фосфорилазы гормонами.
- Основные пути превращения глюкозы в печени.
- Регуляция обмена углеводов инсулином, глюкагоном, адреналином, кортизолом.
- Пентозофосфатный путь окисления глюкозы, физиологическое значение.
- Гликолипиды и гликопротеины. Представления о строении и функциях их углеводных компонентов.
- I. Структура, классификация и свойства основных липидов организма человека
- Б. Структура и классификация фосфолипидов и сфинголипидов
- Пищевые жиры: норма суточного потребления, переваривание, всасывание продуктов.
- В поддержании гомеостаза холестерола в организме. Биохимия желчнокаменной болезни
- Тема 8. 3. Хиломикроны - транспортная форма экзогенных жиров
- Бета-Окисление жирных кислот. Последовательность реакций. Энергетическое значение.
- Механизмы биосинтеза жирных кислот. Регуляция этого процесса.
- Регуляция синтеза жирных кислот.
- Биосинтез жиров в печени и жировой ткани. Регуляция синтеза жиров
- Депонирование и мобилизация жиров в жировой ткани. Механизм регуляции активности липазы гормонами.
- Фосфолипиды, строение, биологическая роль.
- Холестерин, этапы биосинтеза, биологические функции, регуляция биосинтеза.
- Транспортные формы холестерина. Нарушения транспорта. Семейная гиперхолестеринемия. Атеросклероз.
- Причины и факторы риска развития атеросклероза
- Первичные эндогенные формы истощения
- Представления о биосинтезе фосфолипидов. Липотропные вещества.
- Связь между обменом белков и углеводов
- Влияние инсулина, глюкагона и адреналина на обмен жиров.
- Тема 9. 2. Переваривание белков в желудке и кишечнике, всасывание аминокислот
- Реакции трансаминирования, ферменты, их коферментная группа. Биологическое значение реакций. Определение аминотрансфераз с диагностической целью
- Окислительное дезаминирование аминокислот. Глутаматдегидрогеназа. Значение этой реакции.
- Непрямое дезаминирование аминокислот: последовательность реакций, ферменты, биологическое значение.
- Пути катаболизма безазотистого остатка аминокислот. Значение этого процесса.
- Тема 9. 5. Орнитиновый цикл и его биологическая роль
- Тема 9. 6. Гипераммониемия и ее причины
- Конечные продукты азотистого обмена. Источники аммиака в организме. Причины гипеаммониемии.
- Орнитиновый цикл и его биологическая роль
- Обмен фенилаланина и тирозина. Использование тирозина для синтеза катехоламинов, тироксина и меланинов. Распад тирозина.
- Роль гормонов в регуляции обмена белков.
- Катаболизм пуриновых нуклеотидов. Представления о биосинтезе пуриновых нуклеотидов. Подагра.
- Биосинтез и катаболизм пиримидиновых нуклеотидов. Регуляция синтеза.
- Место гормонов в регуляции метаболизма. Классификация гормонов по химическому строению.
- Тема 11. 3. Строение и биосинтез гормонов
- Механизм передачи гормонального сигнала в клетку. Рецепторы гормонов.
- Гормоны гипоталамуса, их биологическая роль.
- Регуляция обмена углеводов, жиров и аминокислот инсулином, глюкагоном, адреналином, кортизолом.
- Адреналин, химическая природа, биосинтез, роль в регуляции метаболизма.
- Кальций-фосфолипидный механизм
- Регуляция синтеза и секреции. Активируют: тиреолиберин, охлаждение (закаливание, обливание холодной водой); также
- Кортикостероиды, химическая природа, влияние на обмен веществ, регуляция биосинтеза.
- Противовоспалительное и иммунодепрессивное действие
- Биохимические нарушения при сахарном диабете. Механизмы развития диабетической комы.
- Гормональная регуляция обмена воды и электролитов. Механизм действия вазопрессина и альдостерона.
- Роль гормонов в регуляции фосфорно-кальциевого обмена. Причины гипо- и гиперкальциемии.
- Строение двух форм витамина D
3. Катаболизм аминокислот начинается с реакции дезаминирования - удаления α-аминогруппы, которая выделяется в виде аммиака и образования безазотистого остатка (α-кетокислоты). При дезаминировании в отличие от трансаминирования общее количество аминокислот уменьшается.
Продукт дезаминирования аммиак - токсичное соединение, в клетках подвергается обезвреживанию.
Безазотистый остаток представляет собой α-кетокислоту, которая включается:
• в реакции окисления до СО2 и Н2О;
• в реакции трансаминирования для синтеза заменимых аминокислот;
• в анаплеротические реакции для восполнения убыли метаболитов ОПК или для синтеза других соединений;
• в глюконеогенез;
• в кетогенез.
Дезаминированию подвергаются все аминокислоты кроме лизина и пролина (табл. 9.3).
Существует несколько типов реакций дезаминирования:
• окислительное - характерно только для Глу;
• неокислительное - характерно для Сер, Тре и Гис;
• непрямое - для остальных аминокислот.
Прямому окислительному дезаминированию подвергается только глутамат. Окислительное дезаминирование глутамата происходит под действием фермента глутаматдегидрогеназы, коферментом которого является NAD+. Реакция идет в митохондриях многих тканей, наиболее активно - в печени. В реакцию неокислительного дезаминирования вступают:
• серин и треонин - с отщеплением воды;
• гистидин - внутримолекулярным способом.
Большинство аминокислот подвергается в клетке непрямому дезаминированию, которое включает две стадии:
А. Трансаминирование с α-кетоглутаратом и образование Глу в цитозоле клетки;
Б. Окислительное дезаминирование Глу в митохондриях.
Центральную роль в непрямом дезаминировании играют глутамат и α-кетоглутарат.
Другой тип дезаминирования аминокислот - непрямое неокислительное - происходит с участием цикла ИМФ-АМФ и характерен для мышечной ткани и мозга, в которых глутаматдегидрогеназа малоактивна:
 Аминогруппа аминокислот с помощью двух последовательных реакций трансаминирования переносится на ИМФ с образованием АМФ, который гидролитически дезаминируется с выделением аммиака. Аминогруппа аминокислот с помощью двух последовательных реакций трансаминирования переносится на ИМФ с образованием АМФ, который гидролитически дезаминируется с выделением аммиака.
Таблица 9.3. Реакции дезаминирования аминокислот
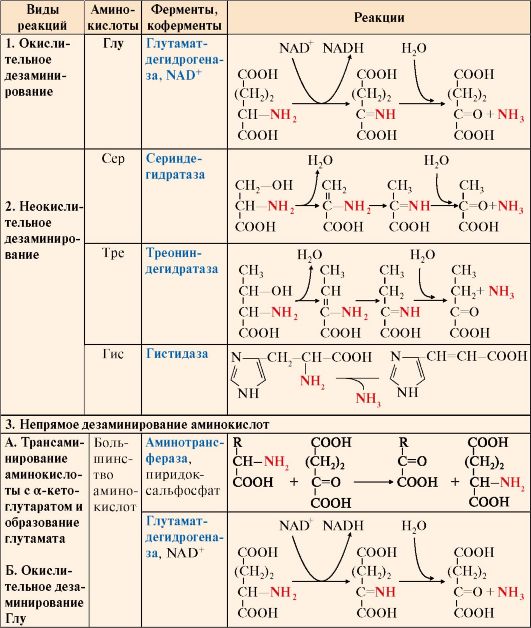 Катаболизм аминокислот и, соответственно, реакции дезаминирования ускоряются при: Катаболизм аминокислот и, соответственно, реакции дезаминирования ускоряются при:
• голодании в результате ускорения распада белков тканей;
• поступлении с пищей больших количеств белка;
• сахарном диабете и других длительно протекающих тяжелых заболеваниях, также сопровождающихся распадом тканевых белков.
ГЛУТАМАТДЕГИДРОГЕНАЗА
фермент, катализирующий взаимопревращение L-глутаминовой и2-оксоглутаровой к-т:
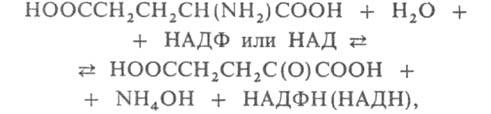
где НАДФ (НАД) и НАДФН (НАДН) соотв. окисленная и восстановленная форма коферментаникотинамидаденин-динуклеотидфосфата (никотинамидадениндинуклеотида) - акцепторы и переносчикиэлектронов и водорода на промежут. стадиях. Относится к классу оксидоредуктаз.
Различают Г. специфичные к НАД, НАД и НАДФ или только к НАДФ. Фермент имеет мол. м. 210-480 тыс. иобычно состоит из 4 или 6 одинаковых субъединиц. В активном центре содержатся остатки лизина, тирозинаи ци-стеина. Третичная структура характеризуется наличием доменов с мол. м. 20 тыс. Известна первичнаяструктура нескольких Г. Оптим. каталитич. активность при аминировании в области рН 7,5-8,5, придезаминировании 8,5-9,5.
Г. содержится в животных, растениях и микроорганизмах. В бактериях и синезеленых водоросляхпредставлена одной формой, в др. организмах - неск. изоферментами. Долгое время Г. рассматривали какосн. фермент первичной ассимиляции NH3. Низкое сродство Г. к NH4+, а также открытие глутаматсинтазы, обнаруженной во всех, кроме животных, организмах, свидетельствуют, что роль Г. в ассимиляции NH3незначительна.
|