
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Механизмы биосинтеза жирных кислот. Регуляция этого процесса.
БИОСИНТЕЗ ВЫСШИХ ЖИРНЫХ КИСЛОТ И ЕГО РЕГУЛЯЦИЯ Образование субстратов для биосинтеза высших жирных кислот. Субстратами для синтеза жирных кислот являются продукты катаболизма глюкозы, поэтому синтез жирных кислот происходит при высокой концентрации глюкозы в крови в абсорбтивный период, в основном, в печени. С меньшей активностью синтез жирных кислот идет в жировой ткани. В период лактации синтез жирных кислот активно происходит в молочных железах и жирные кислоты включаются в жиры молока. В клетках, где происходит синтез жирных кислот, активируются гликолиз и пентозофосфатный путь катаболизма глюкозы, в результате которых образуются субстраты для синтеза жирных кислот: ацетил-КоА, NADPH, ATФ. Синтезированные жирные кислоты быстро включаются в состав других молекул: жиров и фосфолипидов. Синтез жирных кислот и жиров называется липогенезом. Образование ацетил-КоА в результате окислительного декарбоксилирования пирувата - конечного продукта гликолиза - происходит в матриксе митохондрий, но ацетил-КоА не проникает через мембрану митохондрий в цитоплазму, где идет синтез жирных кислот. Поэтому ацетил-КоА конденсируется с оксалоацетатом, образуя цитрат, который с помощью транслоказы переносится в цитоплазму (рис. 8.7). В цитоплазме под действием фермента цитратлиазы идет реакция:
Ацетил-КоА, образующийся под действием пируватдегидрогеназного комплекса (1), не проникает через мембрану митохондрий в цитоплазму, где происходит синтез жирных кислот. Поэтому ацетил-КоА конденсируется ферментом цитратсинтазой с оксалоацетатом (2), образуя цитрат, который с помощью транслоказы переносится в цитоплазму, где он расщепляется под действием цитратлиазы (3), и ацетил-КоА используется как субстрат для синтеза жирных кислот. Реакция, катализируемая малик-ферментом (4), является одним из источников NADPH для синтеза жирных кислот
2. Первая реакция синтеза жирных кислот - это превращение ацетил-КоА в малонил-КоА:
3. Последующие реакции синтеза жирных кислот катализируются ферментным комплексом - синтазой жирных кислот или пальмитатсинтазой. Конечным продуктом синтеза является пальмитиновая кислота. Синтаза жирных кислот - полифункциональный фермент, состоящий из двух идентичных полипептидных цепей, каждая из которых имеет семь активных центров и ацилпереносящий белок, который переносит растущую цепь жирной кислоты из одного активного центра в другой. Каждый из белков имеет два центра связывания, содержащих SH-группы, одна из которых принадлежит цистеину, другая - фосфопантотеину. Схематично этот комплекс изображают таким образом:
Пальмитоил-Е - остаток пальмитиновой кислоты, связанный с синтазой жирных кислот. Пальмитиновая кислота отделяется от ферментного комплекса тиоэстеразой. В синтезированной жирной кислоте только два дистальных атома углерода (СН3 и соседний с ним), выделенные красным цветом, происходят из ацетил-КоА, остальные атомы углерода включаются в радикал жирной кислоты из молекул малонил-КоА
Реакции восстановления обеспечивают синтез насыщенного алифатического радикала жирных кислот 4. Другие жирные кислоты в организме человека синтезируются из пальмитиновой кислоты. Удлинение углеродного скелета происходит также с использованием малонил-КоА. Таким образом синтезируется, например, стеариновая кислота. В организме человека возможен синтез ненасыщенных кислот, однако двойная связь может быть образована у 9 атома углерода (С161 Δ9) и между карбонильной группой и С9. В организме человека не синтезируются жирные кислоты с двойными связями, расположенными дистальнее С9, поэтому полиеновые жирные кислоты с двойными связями между С9 и метильной группой являются эссенциальными и их необходимо получать с пищей. Для обеспечения потребностей организма в эссенциальных жирных кислотах суточная норма жиров (-80-100 г) должна на треть состоять из жиров растительного происхождения. Образованные жирные кислоты не остаются в клетках в свободном виде, а используются для синтеза жиров и фосфолипидов. Жиры, синтезированные в жировой ткани, запасаются в ней, а жиры, синтезированные в печени, упаковываются в ЛПОНП, которые секретируются в кровь.
|
|||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 428; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.141.6 (0.006 с.) |
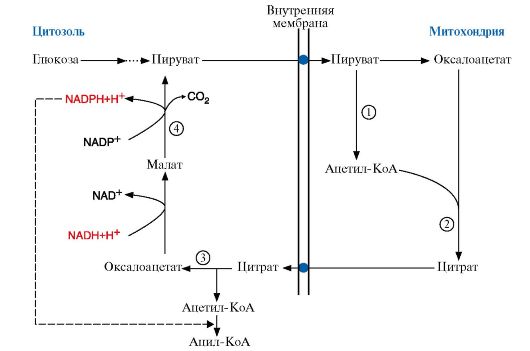 Рис. 8.7. Перенос ацетильных остатков из митохондрий в цитозоль.
Рис. 8.7. Перенос ацетильных остатков из митохондрий в цитозоль.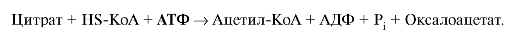 Ацетил-КоА, перенесенный в цитоплазму, является исходным субстратом для синтеза жирных кислот, а оксалоацетат подвергается следующим превращениям:
Ацетил-КоА, перенесенный в цитоплазму, является исходным субстратом для синтеза жирных кислот, а оксалоацетат подвергается следующим превращениям: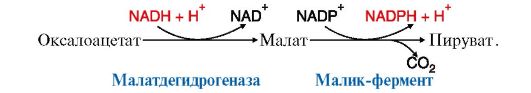 Пируват возвращается в матрикс митохондрий, a NADPH, восстановленный в результате действия малик-фермента, используется как донор водорода для последующих реакций синтеза жирных кислот. Другой источник NADPH - реакция, катализируемая ферментом пентозофосфатного пути - глюкозо-6-фосфатдегидрогеназой.
Пируват возвращается в матрикс митохондрий, a NADPH, восстановленный в результате действия малик-фермента, используется как донор водорода для последующих реакций синтеза жирных кислот. Другой источник NADPH - реакция, катализируемая ферментом пентозофосфатного пути - глюкозо-6-фосфатдегидрогеназой.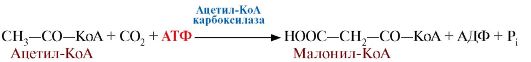 Фермент, катализирующий эту реакцию, ацетил-КоА-карбоксилаза, является регуляторным в биосинтезе жирных кислот. Он относится к классу лигаз и в качестве кофермента использует биотин.
Фермент, катализирующий эту реакцию, ацетил-КоА-карбоксилаза, является регуляторным в биосинтезе жирных кислот. Он относится к классу лигаз и в качестве кофермента использует биотин.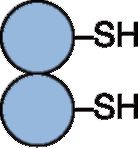 Синтез жирной кислоты начинается с переноса ацетильного, а затем малонильного остатков с помощью ферментов ацетилтрансацилазы и малонилтрансацилазы на активные центры синтазы жирных кислот (рис. 8.8, реакции 1, 2). Далее карбоксильная группа малонила выделяется в виде СО2 и по освободившейся валентности присоединяется ацетил с образованием ацетоацетил-Е (рис. 8.8, реакция 3). Последующие реакции восстановления, дегидратации, восстановления (реакции 4-6) приводят к образованию радикала бутирила, связанного с ферментом. Затем повторяется такой же цикл реакций и образуется радикал жирной кислоты с шестью углеродными атомами. Циклы повторяются вплоть до образования радикала пальмитиновой кислоты, который ферментом тиоэстеразой отщепляется от ферментного комплекса. Так как биосинтез жирных кислот является процессом, в котором повторяются одни и те же последовательности реакций, процесс называют циклическим; в каждом цикле радикал жирной кислоты увеличивается на два атома углерода, источником которых является малонил-КоА (рис. 8.8, 8.9). В каждом цикле происходят реакции восстановления с использованием NADPH + H+, одним из источников которого является пентозофосфатный путь окисления глюкозы, другим - малик-фермент. Реакции восстановления обеспечивают синтез насыщенного алифатического радикала жирных кислот.
Синтез жирной кислоты начинается с переноса ацетильного, а затем малонильного остатков с помощью ферментов ацетилтрансацилазы и малонилтрансацилазы на активные центры синтазы жирных кислот (рис. 8.8, реакции 1, 2). Далее карбоксильная группа малонила выделяется в виде СО2 и по освободившейся валентности присоединяется ацетил с образованием ацетоацетил-Е (рис. 8.8, реакция 3). Последующие реакции восстановления, дегидратации, восстановления (реакции 4-6) приводят к образованию радикала бутирила, связанного с ферментом. Затем повторяется такой же цикл реакций и образуется радикал жирной кислоты с шестью углеродными атомами. Циклы повторяются вплоть до образования радикала пальмитиновой кислоты, который ферментом тиоэстеразой отщепляется от ферментного комплекса. Так как биосинтез жирных кислот является процессом, в котором повторяются одни и те же последовательности реакций, процесс называют циклическим; в каждом цикле радикал жирной кислоты увеличивается на два атома углерода, источником которых является малонил-КоА (рис. 8.8, 8.9). В каждом цикле происходят реакции восстановления с использованием NADPH + H+, одним из источников которого является пентозофосфатный путь окисления глюкозы, другим - малик-фермент. Реакции восстановления обеспечивают синтез насыщенного алифатического радикала жирных кислот.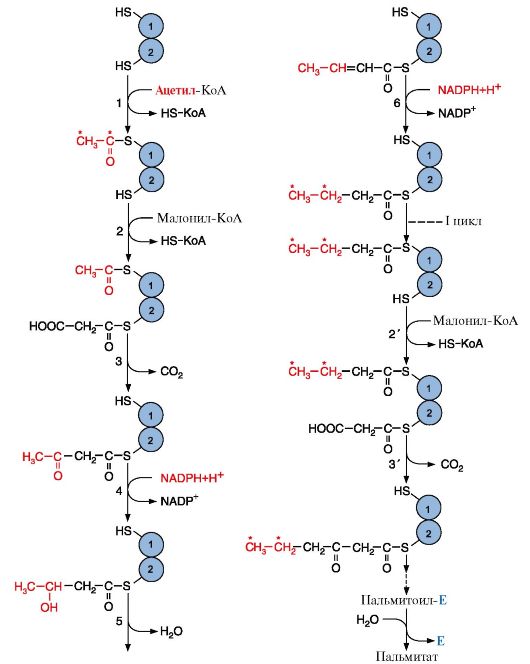 Рис. 8.8. Синтез пальмитиновой кислоты.
Рис. 8.8. Синтез пальмитиновой кислоты.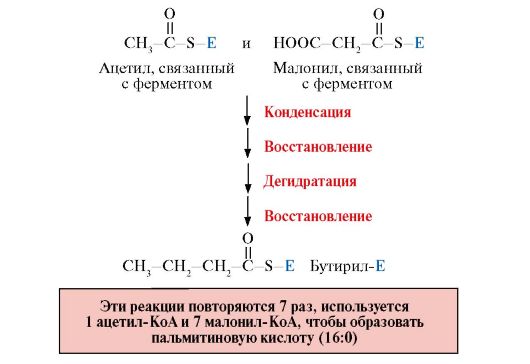 Рис. 8.9. Этапы синтеза пальмитиновой кислоты
Рис. 8.9. Этапы синтеза пальмитиновой кислоты


