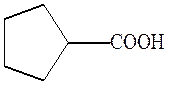Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нахождение в природе и значение для фармации
Карбоновые кислоты их функциональные производные очень широко распространены в природе и давно известны человечеству. Многие карбоновые кислоты имеют тривиальные названия, указывающие на природный источник из которого она была выделена. Например, масляная кислота образуется при прогоркании сливочного масла, валериановая кислота есть в валериановом корне. Капроновая, каприловая и каприновая кислоты получили своё название из-за того что содержатся в козьем молоке (латынь caper — козёл). В щавеле, в ревене содержится щавелевая кислота. Эта простейшая двухосновная кислота - продукт распада некоторых аминокислот, например глицина. При нарушении обмена веществ (например при недостатке витамина B6) в организме человека выделяется её малорастворимая кальциевая соль. Янтарная кислота была синтезирована ещё алхимиком Агриколой при прокалывании янтаря. Янтарная кислота оказывает положительное влияние на восстановление нервной и иммунной систем, повышает сопротивляемость организма к инфекциям, повышает внимание, концентрацию. Малоновая кислота получила своё название от лат. malum - яблоко. Бензойная кислота впервые была получена в XVIв. из росного ладана, были обнаружены и изучены антигрибковые свойства. Бензойноя кислота оказывает угнетающее воздействие на плесень, дрожжи и некоторые виды бактерий. В медицине её используют при кожных заболеваниях как наружное антисептическое и противомикробное средство. Лимонная кислота распространена в природе: содержится в ягодах, плодах цитрусовых, хвое, малине, свекловичном соке, особенно ее много в китайском лимоннике и незрелых лимонах. Натуральный антиоксидант. При приеме внутрь в небольших дозах активизирует цикл Кребса, что способствует ускорению метаболизма. Алифатические (от греч. aleiphar – жир) карбоновые кислоты с числом атомов углерода больше 6 называют также жирными кислотами, поскольку в виде сложных эфиров они входят в состав природных жиров и масел. Самая распространённая из высокомолекулярных непредельных кислот — олеиновая. Изомерна ей элаидиновая кислота - наибольшее их содержание в оливковом масле. Употребление данных мононенасыщенных кислот снижает риск развития сердечно-сосудистых заболеваний, диабета, ожирения и высокого кровяного давления (гипертонии). Наибольшей биологической активностью обладают кислоты с несколькими двойными связями: линолевая с двумя, линоленовая с тремя и арахидоновая с четырьмя. Полиненасыщенные кислоты организм человека сам синтезировать не может и должен получать их с пищей. Препарат «Линетол» применяют для профилактики заболеваний, связанных с недостатком ненасыщенных кислот.
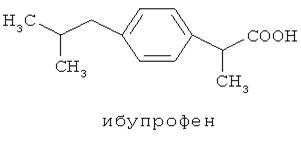
Многие лекарственные средства, содержат карбоксильную группу, которая указывает на их кислотные свойства. Например: азелаиновая кислота, ибупрофен, аспирин.
Такие лекарственные средства, как парацетамол, фенацетин - замещенные амиды уксусной кислоты
Изомерия и номенклатура. К классу карбоновых кислот относятся соединения, содержащие карбоксильную группу COOH. По числу карбоксильных групп в молекуле различают одноосновные R-COOH и многоосновные кислоты HOOC-CH2 -COOH В зависимости от строения углеводородного радикала, связанного с карбоксильной группой, кислоты подразделяются на алифатические (насыщенные и ненасыщенные), алициклические, ароматические, гетероциклические.
По заместительной номенклатуре алифатические монокарбоновые кислоты называют по соответствующим предельным углеводородам с добавлением окончания -овая кислота, нумерация цепи начинается от углерода карбоксильной группы. В тех случаях, когда карбоксильная группа не входит в состав углеводородной цепи, используется сочетание «карбоновая кислота», выполняющее роль суффикса.
циклопентанкарбоновая кислота
Номенклатура ИЮПАК разрешает использовать тривиальные названия, указывающие на природный источник, из которого была выделена кислота.
Для первого представителя ароматических кислот ИЮПАК сохранено название «бензойная кислота» (C6H5СОOH). Замещенные ароматические монокарбоновые кислоты называют, используя бензойную кислоту в качестве родоначальной структуры:
4-метилбензойная кислота 3-нитробензойная кислота
Применяют также систему, согласно которой за основу принимают тривиальное название кислоты, соответствующей самой длинной в молекуле цепи, а атомы обозначают, начиная с соседнего с карбоксильной группой, буквами греческого алфавита.
2-метилбутановая (α-метилмасляная) кислота Изомерия предельных одноосновных карбоновых кислот обусловлена разветвленностью углеродного скелета, взаимным расположением заместителей. Число изомеров увеличивается по мере возрастания углеродной цепи.
Вопросы с примерами решений. 1. Насыщенными дикарбоновыми кислотами являются: а. терефталевая, фумаровая, лимонная; б. винилуксусная, кротоновая, акриловая; в. малоновая, янтарная, глутаровая; г. изовалериановая, масляная, уксусная;
Решение -1: Насыщенные дикарбоновые кислоты содержат две карбоксильные группы, связанные с углеводородным радикалом, в котором все атомы углерода находятся в состоянии s p 3-гибридизации. Следовательно, это - малоновая (HOOCCH2COOH), янтарная (HOOCCH2CH2COOH), глутаровая (HOOCCH2CH2CH2COOH) кислоты. 2. Приведите систематические названия следующих карбоновых кислот: а. CH3CH2 CH(CH3)COOH б.(CH3)2CH CH2 CH2 COOH
в.CH3CH2 C(CH3)2 CH2COOH
Решение -2: а. Выбираем родоначальную структуру - это самая длинная углеводородная цепь, содержащая карбоксильную группу, нумеруем атомы углерода, начиная с углерода карбоксильной группы, всего четыре, у второго атома углерода- радикал метил. Корнем слова - бутан + окончание -овая кислота (указывает на наличие карбоксильной группы), префиксом слова - название радикала, цифра указывает его положение в цепи: 2-метилбутановая кислота (2-метилмасляная кислота) б. 4-метилпентановая кислота (4-метилвалериановая кислота) в. 3,3-диметилпентановая кислота (3,3-диметилвалериановая кислота)
3. Написать формулы возможных изомеров карбоновых кислот, отвечающих составу C5H10O2 Решение -3: Напишем структурную формулу кислоты, имеющий неразветвленный углеродный скелет: а.CH3-CH2-CH2-CH2-COOH Углеродную цепь сократим на один атом и пришьем его к любому (кроме первичного) атому углерода: б. CH3CH2 CH(CH3)COOH в. CH3 CH(CH3)CH2 COOH г. Сократим родоначальную структуру еще на один атом углерода, пришив два атома углерода к вторичному атому цепи: CH3 -C(CH3)2 -COOH
Вопросы для самостоятельного решения
4. Напишите формулы изомеров 2.3-диметилпентановой кислоты. 5. Среди перечисленных веществ выберите:1) изомеры 2) гомологи а) CH3-CH2-CH2- COOH в) HOOC- COOH б) HOOC- CH2-COOH г) CH3-CH(CH3 ) - COOH Назовите приведенные вещества.
Физические свойства. На физических свойствах карбоновых кислот сказывается значительная степень ассоциации молекул вследствие образования водородных связей. В газовой фазе и в неполярных растворителях монокарбоновые кислоты существуют в виде димеров.
Водородные связи, возникающие в карбоновых кислотах объясняют значительно высокие температуры кипения кислот. Монокарбоновые кислоты с числом атомов углерода от 1 до 3 – бесцветные жидкости, смешиваются с водой в любых соотношениях. Кислоты, в молекуле которых содержится от 4 до 9 атомов углерода – маслянистые жидкости, растворимость их в воде невелика. Растворимость в воде высших гомологов уменьшается по мере удлинения углеродного радикала. Практически все дикарбоновые и ароматические кислоты – твердые вещества. В ряду дикарбоновых кислот наблюдаются те же закономерности: низшие гомологи лучше растворяются в воде, чем высшие. Ароматические кислоты плохо растворимы в воде.
Вопросы для самостоятельного решения: 6. Между молекулами какого вещества имеются водородные связи: а) этаналь б) метан в) ацетон г)3-метилмасляная кислота. 7. Какая из приведенных ниже кислот имеет самую высокую температуру кипения: а) уксусная б) 3-метилмасляная в) масляная г) капроновая
Способы получения.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 68; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.20.238.187 (0.016 с.) |