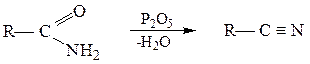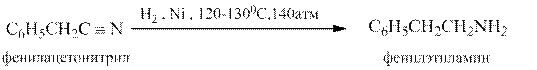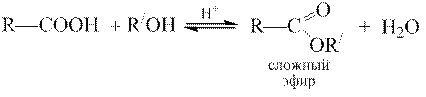Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Расщепление азотистой кислотой.
При взаимодействии с азотистой кислотой и другими нитрозирующими агентами амиды превращаются в соответствующие карбоновые кислоты.
Дегидратация.
Незамещенные амиды под действием оксида фосфора (V) и некоторых других реагентов (POCl3, PCl5, SOCl2) превращаются в нитрилы:
Восстановление. В зависимости от применяемого реагента амиды могут быть восстановлены в амины (без разрыва связей C─ N) или в альдегиды (с разрывом связи C─ N). При действии алюмогидрида лития амиды восстанавливаются в первичные, вторичные и третичные амины:
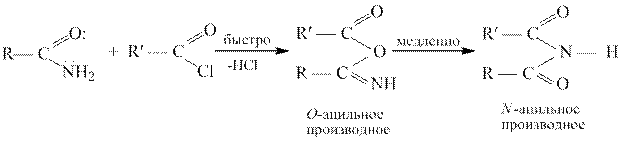
Ацилирование амидов.
При нагревании незамещенных или N -монозамещенных амидов с ангидридами или галогенангидридами образуются имиды, т.е. диацильные производные аммиака
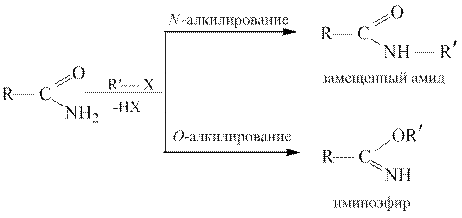
Алкилирование. Алкилирование амидов, как и ацилирование, можно осуществить по атомам азота и кислорода:
Продукты N -алкилирования термодинамически более устойчивы по сравнению с продуктами О -алкилирования, которые называются иминоэфирами или имидатами. Галогенирование.
Галогенирование амидов в избытке щелочи сопровождается расщеплением амидов (расщепление по Гофману) и приводит к образованию первичных аминов, имеющих в молекуле на один атом углерода меньше, чем в исходном амиде:
Нитрилы. Нитрилами (цианидами) называются соединения общей формулы R ─ C ≡ N Нитрилы отличаются по строению от ацильных производных, и к группе функциональных производных карбоновых кислот их относят потому, что они гидролизуются с образованием карбоновых кислот или амидов.
Гидролиз. Нитрилы относятся к очень слабым ацилирующим агентам, более слабым, чем даже амиды, поэтому они гидролизуются (в кислой или щелочной среде) значительно труднее ацильных производных:
Восстановление.
Нитрилы могут быть восстановлены в первичные амины разными методами – каталитическим гидрированием, натрием в этаноле, алюмогидридом лития, например:
По сравнению с другими функциональными производными карбоновых кислот нитрилы восстанавливаются значительно труднее.
Вопросы с эталоном решения.
27. Реакцией этерификации является:
Решение-27: При взаимодействии карбоновых кислот со спиртами в присутствии кислотных катализаторов образуются сложные эфиры, а реакция называется – этерификацией:
Ответ: 2.
Установите соответствие.
Решение-28: Этилбутаноат, бутилацетат, этилацетат – сложные эфиры низших спиртов и карбоновых кислот, образованные соответственно этиловым спиртом и бутановой кислотой, бутиловым спиртом и уксусной кислотой, этиловым спиртом и уксусной кислотой.
Ответ: 1-Д; 2-А; 3-Г.
9. Вопросы для самостоятельного решения. 29. Напишите схемы реакций получения этилпропионата и этилового эфира щавелевой кислоты из соответствующих кислот и спиртов.
30. Напишите уравнение реакций гидролиза этилбутаноата в кислой и в щелочной средах. Объясните как среда влияет на обратимость реакции.
31. Напишите структурные формулы амидов: N,N-диметилацетамида, N- фенилбутанамида, 3,4, N-триметилбензамида.
32. Предложите различные варианты получения N-метилбутанамида из бутановой кислоты.
33. Напишите уравнения реакций гидролиза этанамида в кислой и в щелочной средах. III.Гидроксикислоты. Общая характеристика.
Гидроксикислотами называются соединения, в молекулах которых содержатся гидроксильная и карбоксильная группы. Эти функциональные группы могут быть присоединены к алифатической цепи (алифатические гидроксикислоты) или к ароматическому кольцу, в последнем случае используют иногда родовое название фенолокислоты. Число карбоксильных групп определяет основность гидроксикарбоновых кислот, а суммарное число групп ОН (как спиртовых, так и карбоксильных) – их атомность. Так, например, молочная кислота СН3СНОН―СООН является одноосновной двухатомной кислотой, яблочная НООС―СНОН―СН2―СООН - двухосновной трехатомной и винная НООС―СНОН―СНОН―СООН - двухосновной четырехатомной. По взаимному расположению фунцкциональных групп различают α-, β-, γ-, δ-гидроксикислоты и т.д. Буквы греческого алфавита указывают положение гидроксильной группы относительно карбоксильной, причем отсчет ведется от ближайшего к карбоксильной группе атома углерода, т.е. от атома С-2. Взаместительной номенклатуре ИЮПАК для замещенных карбоновых кислот локанты α-, β-, γ- и т.д. не употребляются.
Систематические названия гидроксикислот строятся по общим принципам заместительной номенклатуры. По систематической номенклатуре названия гидроксикислот производят от названий карбоновых кислот, причем к этому названию прибавляется характерная для спирта приставка гидрокси-. Нумерацию обычно начинают от карбоксильной группы. Так, например, молочная кислота может быть названа 2-гидроксипропановой кислотой.
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 94; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.196.217 (0.012 с.) |