Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Номенклатура международная (систематическая или заместительная)
Для того чтобы назвать соединения, руководствуются общими правилами: 1 Выбирают в молекуле наиболее длинную цепь и нумеруют ее с того конца, к которому ближе стоит заместитель (R) или функциональная группа. 2 Углеводород называют в таком порядке: вначале (цифрой) указывают место расположения заместителя, затем называют этот заместитель (радикал), а в конце добавляют название главной (самой длинной цепи)
2-метил, 4-этилгептан
Если в главной цепи содержится несколько одинаковых заместителей, то их число обозначают приставками ди-, три-, тетра-. Заместители перечисляют по алфавиту.
2, 3 - диметил - 3 - этилгексан
Атомы углерода в алканах могут различаться по характеру своего соединения с другими атомами углерода. Атом углерода, связанный только с одним углеродным атомом, называется первичным, с двумя - вторичным, с тремя - третичньм, с четырьмя - четвертичным. Это можно пояснить на примере:
2,2,4 – триметилпентан Первичные атомы углерода - а, вторичный - б, третичный - в, четвертичный - г.
Методы получения алканов: 1 Гидрирование алкенов:
2 Реакция Вюрца: действие металлического натрия на галогенпроизводные алканов (галогеналкилы)
Если в реакцию вступают два различных алкилгалогенида, то в результате могут получиться три различных алкана. Пример:
3 Из солей карбоновых кислот:
Химические свойства алканов
Алканы проявляют высокую химическую устойчивость. Это обусловлено прочностью всех σ - связей, как углерод-углеродных, так и углерод-водородных. Для алканов характерны реакции: 1 Галогенирование (замещение галогеном). Сравнительно легко алканы вступают в реакцию замещения с хлором и бромом, очень трудно – с иодом. Реакция имеет цепной характер. Например, хлорирование метана, (схема):
2 Реакция нитрования. Реакция Коновалова. Алканы нитруются разбавленной азотной кислотой:
Легче всего замещается водород при третичном атоме углерода, труднее - при вторичном, ещё труднее - при первичном. 3 Реакция сульфохлорирования:
4 Крекинг
5 Изомеризация
6 Ароматизация
7 Окисление
Непредельные или ненасыщенные углеводороды (алкены или олефины)
Общая формула СnН2n
Ненасыщенные соединения, в молекуле которых имеется только одна двойная связь, называется алкенами. Двойную связь образует углерод в состоянии sр2 - гибридизации.
Этиленовые углеводороды имеют в названии суффикс «ен». Главную цепь нумеруют с конца, к которому ближе двойная связь. В состав цепи должна входить двойная связь.
Методы получения
В природе алкены встречаются редко. Газообразные алкены (этилен, пропилен, бутилены) выделяют из газов нефтепереработки (при крекинге) или попутных нефтяных газов. 1 В промышленности алкены получают а) дегидрированием алканов в присутствии катализатора Сr2Оз. Например:
б) Крекинг
В нашей стране более 80% этилена получают пиролизом бензина, около 10% -дегидрированием этана. 2 Лабораторные способы: а) дегидратация спиртов (отщепление воды)
В таких реакциях водород отщепляется от наименее гидрогенизованного атома углерода (с наименьшим числом атомов водорода) - правило Зайцева А.М. б) Отщепление галогеноводорода от галогеналкилов при действии на них спиртового раствора щелочи
Химические свойства
Алкены обладают значительной реакционной способностью. π - связь, как наименее прочная, при действии реагента разрывается, а освободившиеся валентности затрачиваются на присоединение атомов молекулы реагента (σ - связь сохраняется). 1 Гидрирование (присоединение водорода) в присутствии катализаторов Рt, Ni, Рd
2 Галогенирование
3 Гидрогалогенирование
Присоединение идёт по правилу В.В. Марковникова, при обычных условиях водород присоединяется по месту двойной связи к наиболее гидрогенизированному атому углерода, а галоген к менее гидрогенизованному.
4 Реакция гидратации (присоединение воды)
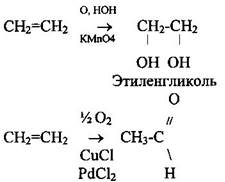
5 Окисление. Реакция Вагнера (качественная реакция):
6 Полимеризация
7 Реакции замещения (термическое хлорирование этилена) 1300°-600°С
8 Реакция алкилирования, в результате которой получаются разветвленные алканы ценные компоненты для повышения качества бензина.
|
||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 336; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.128.94.171 (0.015 с.) |