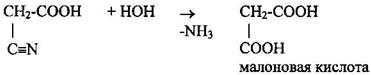Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Одноосновные непредельные кислоты
Методы получения
1 Акриловая кислота Гидролиз акрилонитрила
Карбонилирование ацетилена
2 Метакриловая кислота. В промышленности получают из ацетона и синильной кислоты.
Химические свойства Реакции, идущие с участием карбоксильной группы: 1 Образование солей 2 Образование сложных эфиров
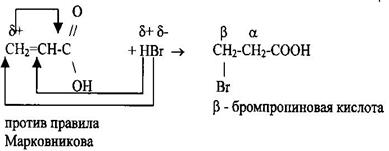
Реакции с участием двойной связи Присоединение водорода, галогена, галогеноводорода, окисление.
Двухосновные кислоты Кислоты, содержащие в молекуле две карбоксильные группы. НООС - СООН - щавелевая кислота (этандиовая кислота) НООС - СН2 - СООН - малоновая кислота (пропандиовая кислота)
Методы получения
1 Окисление гликолей
2 Малоновую кислоту в промышленности получают из монохлоруксусной кислоты, через нитрил с последующим гидролизом
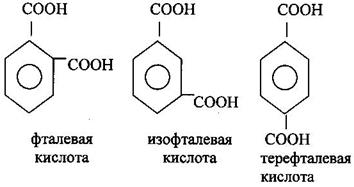
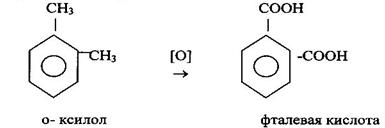
Ароматические фталевые кислоты получают окислением о - м - п – ксилолов.
Химические свойства
В реакциях двухосновных кислот может участвовать одна или две карбоксильные группы. Характерны типичные реакции карбоновых кислот.
Специфическое свойство двухосновных кислот - реакция декарбоксилирования.
Нитросоединения
Нитросоединениями называются органические вещества, содержащие в молекуле остаток азотной кислоты или нитрогруппу -NО2. В зависимости от природы радикала, с которым соединена нитрогруппа, различают нитросоединения предельные, непредельные, циклические и гетероциклические. По характеру углеродного атома, связанного с нитрогруппой подразделяют на первичные, вторичные, третичные (подобно галогенпроизводным и спиртам). В состав молекулы может входить одна или несколько нитрогрупп.
Способы получения
Главный способ получения нитросоединений - реакция нитрования (р. М.И. Коновалова) Нитрованию могут подвергаться: алканы, циклоалканы, ароматические, гетероциклические соединения. Реакция Коновалова
Химические свойства нитросоединений
1 Восстановление, с образованием первичных аминов.
метиламин
аминобензол (анилин)
2 Действие щелочей. Таутомерия.
Таутомерия - способность веществ существовать в нескольких взаимопревращающихся формах. Это явление характерно для первичных и вторичных нитросоединений, имеющих подвижный α- водородный атом. Амины
Амины - органические производные аммиака, в молекуле которого атомы водорода замещены углеводородными радикалами. В зависимости от числа замещённых на радикалы атомов водорода аммиака различают первичные RNН2
Способы получения
1 Реакция Гофмана (алкилирование аммиака).
Более дешево использовать для алкилирования метиловый спирт.
2 Восстановление нитросоединений (реакция Н.Н. Зинина).
нитробензол аминобензол Химические свойства Амины - органические основания, подобно аммиаку они проявляют свойства оснований, которые обуславливаются свободной электронной парой на атоме азота.
Присоединение алкилгалогенидов
Анилин -важнейший из ароматических аминов, получают:
1 Восстановлением нитробензола (р. Н.Н. Зинина)
2 Действием аммиака на хлорбензол.
3 Действие аммиака на фенол
Химические свойства анилина
1 Основные свойства
2 Анилин легко бромируется. Аминогруппа ориентант 1 рода (о-пара-ориентанты).
3 Сульфирование
Анилин легко окисляется. Диазосоединения [Ar-N≡N]X
Диазосоединения Ar-N2-X - это вещества с функциональной группой, составленной из двух атомов азота, соединённого с ароматическим остатком и неорганическим остатком(Сl, HSO4) Важнейший способ получения - реакция диазотирования.
Азотистая кислота неустойчива, поэтому берут её соли и сильную минеральную кислоту в избытке. Реакции диазосоединений разнообразны. Их разделяют на 2 группы - реакции с выделением азота и реакции без выделения азота. Первые имеют большое значение для синтеза ароматических соединений, вторые - для получения азокрасителей.
Реакции диазосоединений с выделением азота
1 Замена диазогруппы на гидроксил
С6Н5N2Сl+НОН → С6Н5ОН+N2+КСl диазобензол фенол
2 При действии иодида калия диазогруппа замещается на йод:
3 Замещение диазогруппы на группу СN при действии солей меди (I).
Реакции без выделения азота- реакции азотосочетания
Соединения формулы:
называются азосоединениями. Многие из них являются азокрасителями.
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 256; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.70.157 (0.016 с.) |