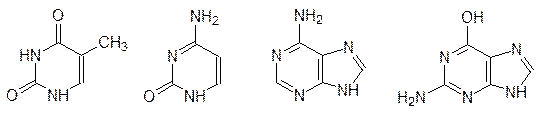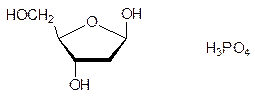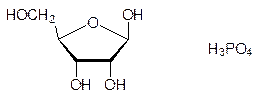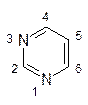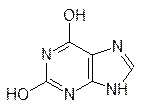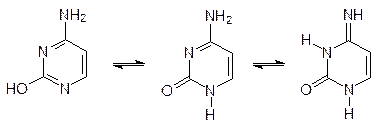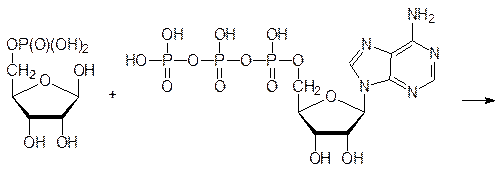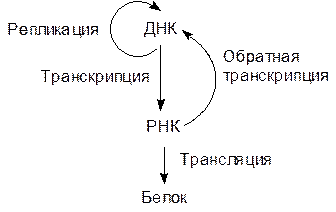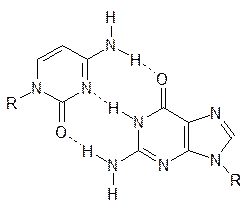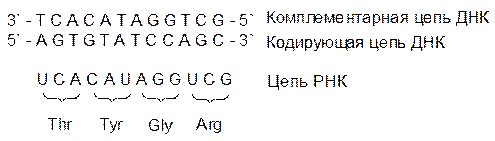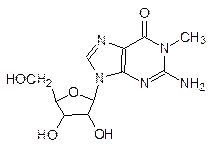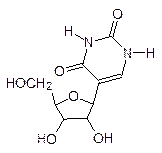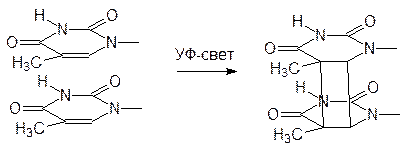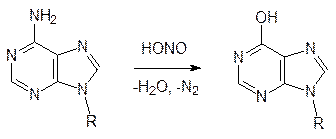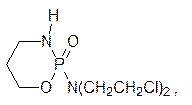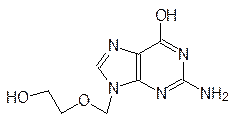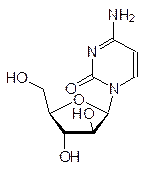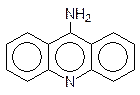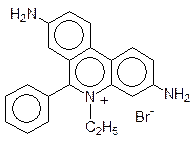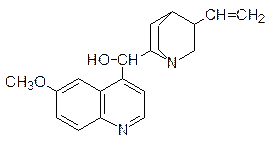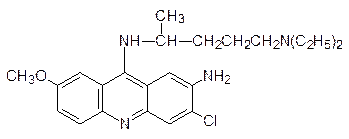Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Глава 2. Нуклеиновые кислотыСтр 1 из 14Следующая ⇒
Еще в XIX в. было показано, что клетки содержат значительно различающиеся по молекулярным массам полимерные кислоты, строение которых удалось установить только в конце 1940-х гг. Высокомолекулярные фракции этих биополимеров были собраны в ядрах (nucleus) клеток, и поэтому они получили общее название нуклеиновые кислоты. При гидролизе высокомолекулярные нуклеиновые кислоты разлагались на производные пиримидина – тимин и цитозин, на производные пурина – аденин и гуанин, а также на дезоксирибозу и фосфорную кислоту; по сахаридной компоненте их называли дезоксирибонуклеиновыми кислотами (ДНК):
При гидролизе нуклеиновых кислот меньшей молекулярной массы получали урацил, цитозин, аденин, гуанин, рибозу и фосфорную кислоту; их стали называть рибонуклеиновыми кислотами (РНК):
Наряду с этими структурными элементами в продуктах гидролиза нуклеиновых кислот содержались также состоявшие из этих же молекул продукты неполного гидролиза более сложного строения, среди которых были построенные по принципу N‑гликозидов продукты конденсации гетероциклов и рибозы или дезоксирибозы – нуклеозиды,а также продукты фосфорилирования нуклеозидов по 5¢-положению – нуклеотиды – и по 3¢‑положению рибозидного или, соответственно, дезоксирибозидного фрагмента, например:
Исходя из этого можно было сделать вывод о том, что нуклеиновые кислоты представляют собой линейные продукты поликонденсации нуклеотидов, в которых к полимерной цепочке из чередующихся фрагментов рибозы (или дезоксирибозы) и фосфорной кислоты присоединены гетероциклические основания:
Урацил, тимин и цитозин относятся к производным гетероциклического соединения пиримидина, а аденин и гуанин – это производные пурина. В метаболических процессах (но не в построении нуклеиновых кислот) участвуют также 6-гидроксипурин (гипоксантин) и 2,6-дигидроксипурин (ксантин), а 1,3,7-триметил-ксантин – это кофеин.
Гипоксантин Ксантин Одним из продуктов метаболического превращения пуриновых оснований является мочевая кислота – 2,6,8-тригидроксипурин. Это вещество плохо растворимо в воде и его отложение в тканях тела и в суставах является причиной болезни, известной под названием подагра.
Для всех оснований, входящих в состав нуклеиновых кислот, характерна так называемая лактам - лактимная таутомерия. Так, например, на цитозине это выражается равновесием:
В лактимных формах возможны реакции гидролитического дезаминирования, в результате которых, например, цитозин может превращаться в урацил, а гуанин – в ксантин:
Если в клетке есть эти гетероциклические основания, то биосинтез нуклеотидов идет следующим образом: 5¢-фосфат дезоксирибозы (или 5¢-фосфат рибозы) фосфорилируется аденозинтрифосфатом по аномерной гидроксильной группе с образованием соответствующего 1¢-пирофосфата. Например, для пирофосфата 5¢‑фосфо-a‑рибозы:
Затем пирофосфатное производное пентозы реагирует с азотистым основанием с образованием соответствующего b‑фосфорибозида и с выделением пирофосфата, который при этом гидролизуется на две молекулы фосфорной кислоты (чтобы реакция стала необратимой).
Так образуются аденозинмонофосфат (AMФ), гуанозинмонофосфат (ГМФ, на представленной выше схеме представлен его биосинтез) и другие нуклеотиды (в латинской транскрипции CMP, UMP, АМР, GМР, dAMP, dGMP, dCMP и TMP). Из представленной схемы следует, что роль азотистых оснований не сводится только к участию в образовании ДНК и РНК. В виде рибозидов они участвуют в образовании основного носителя свободной химической энергии аденозинтрифосфата (АТФ, АТР), его аналога гуанозинтрифосфата (ГТФ, GTP), некоторых участвующих в метаболизме веществ, относящихся к коферментам, и других биомолекул. По аналогичной схеме с участием АТФ идет и поликонденсация нуклеотидов с образованием ДНК или РНК. ДНК представляет собой вещество, несущее наследственную информацию. В этих биополимерах записана вся программа построения многих вирусов, прокариотических клеток (у многих из них молекула ДНК – плазмида – имеет кольцевую структуру), эукариотических клеток и многоклеточных организмов. Собранные в клеточном ядре эукариотической клетки молекулы ДНК включают генные участки. Ген – это часть гигантской молекулы ДНК, содержащая информацию о последовательности аминокислот, составляющих одну белковую молекулу. В эукариотических клетках в ходе их деления различаются компактные образования из различных белков и молекул ДНК, называемые хромосомами (от греч. chroma и soma – окрашиваемые тельца). Из всех содержащихся в клетках соединений только хромосомы подходили на роль носителей наследственности, и именно содержащиеся в них молекулы ДНК лучше всего соответствовали этой роли. Это было показано в различных экспериментах. Одно из таких доказательств роли ДНК было получено в опытах на пневмококках. Мутантный невирулентный штамм этого микроорганизма можно было снова сделать вирулентным, добавив в среду, на которой он развивается, ДНК из вирулентного штамма. Для полного исключения возможного участия в этом белков, от которых ДНК на том этапе исследований не удавалось очистить полностью, выделенную из вирулентных штаммов ДНК обрабатывали дезоксирибонуклеазой, гидролизующей только ДНК; после этого продукт гидролиза терял способность переносить свойство вирулентности.
Синтез белка идет в цитозоле на рибосомах, представляющих собой комплекс белков и рибосомальных рибонуклеиновых кислот (рРНК), а собранная в ядре эукариотических клеток ДНК передает информацию об аминокислотной последовательности белка с помощью еще одной РНК – матричной (мРНК), синтезируемой на основе кодирующей цепи генного участка ДНК. Взаимоотношения ДНК–РНК–белок строятся по схеме:
Основа полимерной цепи ДНК представлена чередующимися молекулами фосфорной кислоты и дезоксирибозы, аномерные гидроксильные группы которой замещены на остатки тимина, цитозина, аденина и гуанина. Эти фрагменты нуклеотидов и определяют пространственную организацию ДНК, образуя знаменитую двойную спираль из двух цепей ДНК за счет реализации водородных связей в парах аденин–тимин и цитозин–гуанин (одноядерный и двухядерный гетероцикл):
Цепи ДНК в паре антипараллельны, одну из них называют кодирующей (на ней идет синтез РНК), а другую комплементарной (по ней проверяются ошибки, нарушения структуры ДНК). Кодирование аминокислотной последовательности в белке осуществляется тройками из нуклеотидных фрагментов. Здесь простая арифметика: пара из четырех оснований даст только 16 различных сочетаний, а белковых аминокислот – 20. Число возможных комбинаций из четырех оснований по три равно 64. Из этого следует, что многие аминокислоты кодируются не одним, а несколькими триплетами (вырожденность генетического кода). Кодирующие аминокислоты тройки оснований называют кодонами, и лишь три кодона не относятся ни к одной аминокислоте. Их обычно называют бессмысленными, но на самом деле у них есть смысл – они обозначают конец гена, завершение информации о белковой цепи на этом участке ДНК. Молекула РНК подобна комплементарной цепи ДНК, но вместо тиминового фрагмента у нее стоит урацильный:
Можно представить себе, что есть рамка считывания информации с молекулы ДНК, в которую входят три нуклеотидных участка. Смещения рамки из-за выпадения одного нуклеотидного фрагмента (делеции) или добавления лишнего (вставки) приведут к транскрипции с образованием мРНК, трансляция с которой даст совсем другую аминокислотную последовательность, причем синтезируемый с этим сбоем белок может оказаться достаточно большим, поскольку из 64 вариантов кодонов только три останавливают биосинтез белка.
На самом деле процесс считывания информации с ДНК гораздо сложнее. Последовательность кодирующих белок участков ДНК в гене (экзоны) прерывается участками, которые не несут информации о белке – это так называемые интроны. При транскрипции сначала считывается вся последовательность экзонов и интронов с образованием первичного транскрипта РНК, из которого затем вырезаются участки, соответствующие интронам, а экзонные участки соединяются в одну цепь – идет процесс образования зрелой мРНК (сплайсинг). Понятно, что начало и конец интронов обозначены определенным сочетанием оснований: во всяком случае, все они начинаются с GU и кончаются AG [сплайсинг осуществляет аналог рибосомальной РНК – мяРНК (малая ядерная РНК)]. Биологическая роль интронов состоит, очевидно, в облегчении эволюции живого за счет ошибок в ходе сплайсинга с перетасовкой готовых блоков из РНК. Как отмечалось во Введении, именно РНК претендует сейчас на роль молекулы, с которой начиналось зарождение жизни. Одним из веских подтверждений этому является возможность самополимеризации фрагментов РНК с образованием более длинных цепей, сворачивающихся в компактные структуры с небольшими спиральными участками, которые аналогичны двойным спиралям ДНК. Кроме матричной и рибосомальной РНК, клетки содержат значительное количество других РНК с меньшей молекулярной массой, например, транспортные РНК (тРНК), которые при синтезе белка переносят аминокислоты к рибосомам, а также РНК с каталитической активностью (рибозимы). Интересно, что в составе этих «дополнительных» РНК есть гетероциклические структурные элементы, отличные от входящих в состав ДНК и мРНК, например, инозин, 1-метилгуанозин и псевдоуридин:
Повреждения структуры ДНК Сочетание кислотных и основных функциональных групп в молекуле ДНК делает ее достаточно чувствительной к рН среды и к присутствию в ней катионов металлов. Так, например, двухнитевая спираль устойчива только в среде с определенным содержанием ионов натрия и калия в достаточно узком интервале значений рН. В то же время ионы переходных металлов легко образуют комплексы с азотными функциями гетероциклических фрагментов молекулы ДНК, и поэтому они могут серьезно влиять на процессы репликации и транскрипции. Ионы металлов могут образовывать комплексы с ДНК как с участием воды (в гидратированной форме), так и без нее. Понятно, что включение в структуру ДНК дополнительных компонент нарушает естественный ход считывания информации с этой макромолекулы, что ведет к мутациям, то есть к изменению исходной структуры образовавшейся в результате репликации ДНК. В многоклеточном организме это может привести к появлению аномальных клеток, что лежит в основе тератогенного (отклонения в развитии плода) или онкогенного (возникновение злокачественных опухолей) эффекта ионов тяжелых металлов. В частности, установлено, что в присутствии повышенных концентраций ионов меди и марганца резко возрастает число мутантных клеток бактерий. Установлена канцерогенность солей хрома и никеля, токсичны соли кадмия, ртути, серебра, висмута. В отдельных случаях бактерицидные свойства таких солей (особенно серебра) используются для борьбы с патогенными микроорганизмами, хотя, конечно, токсическое действие этих металлов не ограничивается взаимодействием только с нуклеиновыми кислотами.
В полимерной молекуле ДНК, которая предназначена для длительного хранения информации, нет свободных гидроксильных групп. В отличие от этого молекула РНК достаточно легко деполимеризуется по реакции переэтерификации с образованием циклического фосфата:
И все же, ионы меди, ртути, кадмия даже в очень низких концентрациях приводят к появлению разрывов в цепях ДНК из-за гидролиза. Еще более серьезные повреждения молекул наследственного вещества вызываются совместным действием ионов таких металлов и ионизирующего (или коротковолнового электромагнитного) излучения. Это особенно важно в связи с растущим загрязнением окружающей среды тяжелыми металлами на фоне радиоактивного заражения и возрастающей интенсивности ультрафиолетового излучения в результате разрушения озонового слоя. Свой вклад в этот процесс вносят и высокочастотные излучения различного происхождения (радиоволны дециметрового и более коротковолновых диапазонов, спутниковые и сотовые телефоны, печи СВЧ). Постоянные повреждения структуры ДНК вызывает ультрафиолетовое и рентгеновское излучение, а также другие виды радиации. Известно, например, что УФ‑излучение вызывает димеризацию расположенных рядом тиминовых фрагментов в молекуле ДНК. Такое связывание приводит к изменению расстояния между основаниями и к сбою в рамке считывания:
Природа готова к такому повреждению структуры ДНК: специальная ферментная система обнаруживает участки со связанными тиминовыми молекулами и вырезает их, вставляя «исправные». Если эта ферментная система дефектна (наследственное заболевание), то это проявляется в виде болезни ксеродермии, которая заставляет больных избегать солнечного света, сильно сушащего кожу и даже вызывающего злокачественные опухоли на коже. В малой степени, но все же идет гидролиз образующихся в таутомерном превращении иминных функциональных групп в фрагментах цитозина и гуанина, в результате чего эти фрагменты превращаются, соответственно, в урациловый и ксантиновый. Превращение цитозинового остатка в урацильный по схеме:
также распознается репарирующей ферментной системой (именно поэтому в молекуле ДНК роль урацила выполняет тимин). Если бы возможность такого распознавания была исключена, то урацил, образовавшийся из цитозина, оказался бы в аномальной паре с гуанином, и тогда репарирующая система встала бы перед неразрешимым вопросом: что надо заменить – урацил на цитозин или гуанин на аденин? Именно для таких исправлений возможных ошибок и служит вторая комплементарная нить ДНК. Кодирующая и комплементарная нити взаимно контролируют друг друга. Возможность саморепарации показана в опыте с культурой дрожжей: после облучения летальной для них дозой радиации некоторые дрожжевые клетки могут восстановить жизнеспособность, если их на несколько дней поместить в холодильник. К химическим мутагенам относятся: ü дезаминирующие вещества и N-нитрозопроизводные; ü алкилаторы (диметилсульфат, метилиодид, метилбромид, бензилхлорид, азотистый и сернистый иприт, соединения с активированными двойными связями и т.д.); ü структурные аналоги азотистых оснований и нуклеозидов. На параметаболический процесс (химическое превращение без участия ферментов) гидролиза лактимной формы цитозинового, аденинового или гуанинового фрагментов может накладываться действие азотистой кислоты, образующейся, например, из нитратных удобрений или из добавляемых в мясные продукты нитратов и нитритов:
Пока число таких мутаций не превышает возможности их репарации соответствующими ферментными системами, контролирующими соответствие кодирующей и комплементарной нитей ДНК, отрицательные последствия минимальны. Если же ДНК с дезаминированными фрагментами включается в процесс транскрипции, то это приводит к фатальным последствиям, поэтому большие концентрации нитритов токсичны. Важными мутагенами и цитостатиками (вещества, останавливающие деление клеток) являются все N-нитрозопроизводные и многие вещества с алкилирующей способностью. Так, например, одним из мощнейших мутагенов является N‑нитрозодиметиламин и другие нитрозамины, которые легко образуются из нитритов и вторичных аминов. N-Нитрозодиметиламин образуется также из несимметричного диметилгидразина, используемого в качестве ракетного топлива. N‑Нитрозопроизводные реагируют с аминогруппами в ДНК с образованием триазенов, например:
Среди алкилаторов можно выделить вещества, которые более или менее избирательны по отношению к различным нуклеофильным центрам (зарядовый и орбитальный контроль); есть С-алкилаторы, S-алкилаторы, N-алкилаторы, О‑алкилаторы. Так, например, диметилсульфат алкилирует преимущественно атом кислорода в гуаниновом фрагменте ДНК:
Алкилирование, конечно, приводит к изменению системы водородных связей в молекуле ДНК, хотя небольшие количества метилированных азотистых оснований обязательно присутствуют в ДНК. В отличие от этого азотистый иприт атакует атом азота в имидазольном цикле пуриновых оснований, что приводит к отщеплению азотистого основания:
Первыми средствами для лечения злокачественных опухолей стали b‑хлорэтиламины. Их действие было направлено на клетки, которые часто делятся и система репарации которых не успевает заменить дефектные участки в ДНК, образовавшиеся в результате действия этих веществ. С этим механизмом действия связан и токсический эффект алкилаторов, так как в организме человека достаточно много нормальных тканей, в которых идет интенсивное деление клеток. Совершенствование структур b‑хлорэтиламинов улучшило их терапевтические показатели. В качестве примера можно привести современное химиотерапевтическое средство циклофосфан (циклофосфамид)
избирательность которого основана на гидролитическом отщеплении бис(b‑хлорэтил)амина от этого производного фосфорной кислоты. Алкилирующая способность хлорэтильных групп в амиде очень низка, а в злокачественных клетках очень активны ферменты, гидролизующие производные фосфорной кислоты (фосфорилазы), поэтому цитотоксичный бис(b‑хлорэтил)амин образуется преимущественно в клетках опухоли. Химические мутагены третьего типа относятся к антиметаболитам – структурным аналогам естественных метаболитов. Одним из примеров может служить 5-фторурацил. Его применение в роли антибактериального препарата основано на том, что часто делящиеся, интенсивно размножающиеся клетки испытывают острую потребность в строительных элементах ДНК и РНК, а ферментные системы бактерий не столь совершенны, чтобы различать присутствие лишнего заместителя. Поэтому они чаще встраивают этот структурный аналог урацила или тимина в свои РНК или ДНК, которые оказываются в результате этого дефектными. Для повышения избирательности 5‑фторурацила его ацилируют короткой пептидной цепью из D -аминокислот. В организме человека нет ферментов для разложения таких пептидных связей, а в клетках бактерий они есть. В клетках человека такой ацилированный 5-фторурацил не изменяется и, в конце концов, выводится, а в клетках бактерий гидролиз идет и в результате выделяется 5‑фторурацил, приводящий к образованию дефектной ДНК. Другими примерами антиметаболитов структурных элементов ДНК служат, в частности, 5-иодуридин, азидотимидин (лекарство от СПИДа), арабиноаденозин (антибиотик и лекарство от герпеса):
Антиметаболитами с противогерпесной активностью являются также ацикловир (Зовиракс) и ганцикловир:
Для лечения лейкозов и лейкемий используются антибиотики цитарабин и пентостатин:
Особое место в нарушении репликации и транскрипции занимают вещества, называемые интеркаляторами. Дело в том, что несмотря на плотную упаковку молекулы ДНК в двойной спирали, в ней все же остается место для встраивания плоских молекул, и это, конечно, сопровождается изменением геометрии спирали, ее витки растягиваются, освобождая место для «квартиранта». Чем больше у внедрившейся в спираль ДНК молекулы возможностей для образования ионных, водородных или иных типов связей, тем более прочное соединение включения она образует. Интеркаляторами являются многие полиядерные гетероциклические соединения, например 9-аминоакридин и этидийбромид:
По механизму интеркаляции действуют также многие средства для борьбы с болезнетворными микроорганизмами. Например, типичным интеркалятором является алкалоид хинин, в течение многих лет использовавшийся для лечения малярии:
Интеркаляторами являются также синтетические аналоги хинина акрихин:
и хлорохин:
Большая группа интеркаляторных антибиотиков используется для лечения злокачественных новообразований. Так, например, рубомицин
плоской системой четырех сконденсированных циклов встраивается между парами оснований в молекуле ДНК, а дидезоксиаминосахаридный фрагмент служит подобием якоря, фиксируясь в пространстве между полиэфирными цепями двух нитей ДНК с фосфатными группами.
|
|||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 80; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.128.199.162 (0.037 с.) |