
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Особенности строения и функции гипофиза, эпифиза, щитовидной и паращитовидной и вилочковой желез, надпочечников, поджелудочной и половых желез.
2. Сахарный диабет: определение, формы, этиология, патогенез, 3. Клиническая картина, лабораторная диагностика, лечение. 4. Особенности введения инсулина. 5. Осложнения, комы и неотложная помощь при них. 6. Профилактика. Прогноз.
Эндокринная система является главным регулятором роста и развития организма. К эндокринной системе относятся: гипофиз, эпифиз, щитовидная, поджелудочная, паращитовидные, вилочковая, половые железы, надпочечники. Некоторые эндокринные железы начинают функционировать уже в период эмбрионального развития. Существенное влияние на рост и развитие ребенка оказывают гормоны материнского организма, которые он получает во внутриутробном периоде и с грудным молоком. В различные периоды детства может выявляться относительное преобладающее влияние одной определенной эндокринной железы. Например, в 5-6 месяцев начинает усиленно функционировать щитовидная железа, ведущая роль которой сохраняется до 2-2,5 года. Действие передней доли гипофиза становится особенно заметным у детей 6-7 лет. В препубертатном периоде возрастает функциональная деятельность щитовидной железы и гипофиза. В препубертатном и особенно в пубертатном периоде основное влияние на рост и развитие организма оказывают гормоны половых желез. Гипофиз. Это эндокринная железа, от деятельности которой во многом зависит структура и функции щитовидной железы, надпочечников, половых желез. К моменту рождения гипофиз обладает отчетливой секреторной активностью. Гиперфункция передней доли гипофиза влияет на рост и приводит к гипофизарному гигантизму, а по окончании периода роста - к акромегалии. Гипофункция вызывает гипофизарный нанизм (карликовость). Недостаточное выделение гонадотропных гормонов сопровождается задержкой пубертатного развития. Повышение функции задней доли гипофиза приводит к нарушению жирового обмена с отставанием в половом созревании. При недостаточной выработке антидиуретического гормона развивается несахарный диабет. Эпифиз (шишковидная железа). У детей он имеет большие размеры, чем у взрослых, вырабатывает гормоны, влияющие на половой цикл, лактацию, углеводный и водно-электролитный обмен. Щитовидная железа. У новорожденных она имеет незаконченное строение. Ее масса при рождении составляет 1-5 г. До 5-6-летнего возраста отмечается формирование и диффе- ренцировка паренхимы, интенсивное увеличение массы железы. Новый пик роста размеров и массы железы наступает в период полового созревания. Основными гормонами железы являются тироксин, трийодтиронин (Т3, Т4), тиреокальцито- нин. Функция щитовидной железы контролируется гормонами гипофиза и мозгового вещества надпочечников (по механизму обратной связи). Гормоны Т3 и Т4 являются основными стимуляторами обмена веществ, роста и развития организма. Недостаточность функции щитовидной железы у плода может не сказаться на его развитии, так как плацента хорошо пропускает материнские тиреоидные гормоны.
Паращитовидные железы. У детей они имеют меньшие размеры, чем у взрослых. В железах происходит синтез парат- гормона, имеющего вместе с витамином D большое значение в регуляции фосфорно-кальциевого обмена. Недостаточность функции паращитовидных желез в первые недели жизни ребенка ведет к гипокальциемии новорожденных, чаще встречающейся у недоношенных детей. Вилочковая железа (тимус). У новорожденных и детей младшего возраста она имеет относительно большую массу. Ее максимальное развитие происходит до 2 лет, затем начинается постепенная инволюция железы. Как центральный орган иммунитета тимус формирует популяцию Т-лимфоцитов, которые осуществляют реакцию клеточного иммунитета. Преждевременная инволюция вилочковой железы сопровождается у детей склонностью к инфекционным заболеваниям, отставанием в нервно-психическом и физическом развитии. С деятельностью тимуса связаны активация роста и торможение функции половых желез, надпочечников и щитовидной железы. Установлено участие вилочковой железы в контроле за состоянием углеводного и кальциевого обмена, за нервно-мышечной передачей импульсов. Надпочечники. У новорожденных надпочечники крупнее, чем у взрослых. Их мозговое вещество у детей младшего возраста недоразвито, перестройка и дифференцировка его элементов заканчивается к 2 годам. Корковое вещество вырабатывает более 60 биологически активных веществ и гормонов, которые по воздействию на обменные процессы делятся на глюкокортикоиды, минералокортикоиды, андрогены и эстрогены. Глюкокортикоиды регулируют углеводный обмен, обладают выраженным противовоспалительным и гипосенсибилизирующим действием. Минералокортикоиды участвуют в регуляции водно-солевого обмена и метаболизме углеводов. В функциональном отношении кора надпочечников тесно связана с АКТГ, половыми и другими эндокринными железами. Гормоны мозгового вещества - адреналин и норадреналин - оказывают влияние на уровень артериального давления. У новорожденных и грудных детей корковое вещество надпочечников вырабатывает все необходимые для организма кортикостероиды, но суммарная экскреция их с мочой низкая. Снижение функции надпочечников возможно у детей с лимфатикогипопластическим диатезом, при токсических воздействиях, кровоизлияниях, опухолевых процессах, туберкулезе, тяжелой дистрофии. Одной из форм дисфункции является острая надпочечниковая недостаточность.
Поджелудочная железа. Эта железа обладает внешнесекреторной и внутрисекреторной функциями. Масса ее у новорожденных составляет 4-5 г, к периоду полового созревания увеличивается в 15-20 раз. Гормоны поджелудочной железы синтезируются в островках Лангерганса: в-клетки продуцируют инсулин, а-клетки - глюкагон. К моменту рождения ребенка гормональный аппарат поджелудочной железы анатомически развит и обладает достаточной секреторной активностью. Эндокринная функция поджелудочной железы тесно связана с действием гипофиза, щитовидной железы, надпочечников. Важная роль в ее регуляции принадлежит нервной системе. Недостаточное образование инсулина приводит к развитию сахарного диабета. Половые железы. К ним относят яичники и яички. Эти железы начинают усиленно функционировать только к периоду полового созревания. Половые гормоны обладают выраженным действием на рост и развитие половых органов, вызывают формирование вторичных половых признаков.
2. Сахарный диабет: определение, формы, этиология, патогенез, Сахарный диабет (СД) - группа обменных заболеваний различной этиологии, характеризующихся хронической гипергликемией, возникающей в результате абсолютной или относительной недостаточности инсулина. Наиболее распространенными формами СД являются инсулинзависимый (ИЗСД, 1-й тип) и инсулиннезависимый (ИНСД, 2-й тип). В детском возрасте преимущественно развивается СД 1-го типа. Он характеризуется абсолютным дефицитом инсулина, вызванным аутоиммунным процессом, который приводит к прогрессирующему, избирательному повреждению в-клеток поджелудочной железы. Сахарный диабет 1-готипа. Наибольшая частота манифестации СД приходится на зимние месяцы, что совпадает с максимальной заболеваемостью вирусными инфекциями. В первые месяцы жизни заболевание наблюдается редко. В дальнейшем выделяют два возрастных пика заболеваемости - в 5-7 лет и 10-12 лет. В последние годы отмечена тенденция к более высокой распространенности заболевания детей в возрасте 0-5 лет. Этиология. В основе развития СД 1-го типа имеет значение сочетание генетической предрасположенности и влияние факторов внешней среды. Наследственная предрасположенность связана с иммунореактивными генами, контролирующими в организме различные звенья аутоиммунных процессов. Для начала аутоиммунного процесса необходим инициирующий или провоцирующий фактор внешней среды (триггер). К триггерам, принимающим участие в запуске процессов разрушения в-клеток, относятся:
• вирусы краснухи, эпидемического паротита, кори, ветряной оспы, Коксаки В4, цитомегаловирус, энтеровирусы, ротавирусы, ЕСНО и др.; • нерациональное питание (раннее искусственное и смешанное вскармливание, употребление пищи, содержащей избыточное количество жиров и углеводов); • воздействие токсинов. Иммунологический процесс, приводящий к манифестации СД, начинается за годы до появления клинических симптомов заболевания. Во время преддиабетического периода в крови можно обнаружить повышенные титры различных аутоантител к островковым клеткам и инсулину либо к белку, находящемуся в островковых клетках. Патогенез. В развитии заболевания выделяют шесть стадий. I стадия - генетическая предрасположенность, ассоциированная с HLА (реализуется менее чем у половины генетически идентичных близнецов и у 2-5% сибсов); II стадия - воздействие фактора, провоцирующего аутоиммунный инсулит; III стадия - хронический аутоиммунный инсулит; IV стадия - частичная деструкция в-клеток, сниженная секреция инсулина на введение глюкозы при сохраненной базальной гликемии (натощак); V стадия - клиническая манифестация заболевания, при которой сохраняется остаточная секреция инсулина, она развивается после гибели 80-90% в-клеток; VI стадия - полная деструкция в-клеток, абсолютная инсу- линная недостаточность. В основе механизма повреждения в-клеток вирусами лежит: • прямое разрушение (лизис) в-клеток вирусами; • молекулярная мимикрия, при которой иммунный ответ, направленный на вирусный АГ, сходный с собственным АГ в-клетки, повреждает и саму островковую клетку; • нарушение функции и метаболизма в-клетки, в результате чего на ее поверхности экспрессируются аномальные АГ, что приводит к запуску аутоиммунной реакции; • взаимодействие вируса с иммунной системой. Инсулин - главный гормон, регулирующий обмен веществ в организме. К органам - мишеням действия инсулина относятся печень, мышечная и жировая ткань. При дефиците инсулина снижается транспорт глюкозы в клетки органов-мишеней, увеличивается образование глюкозы из белков и жиров. В результате этих процессов повышается содержание глюкозы в крови. Гипергликемия приводит к глю- козурии, так как большое количество глюкозы не может реаб- сорбироваться в почках. Наличие глюкозы в моче увеличивает относительную плотность мочи и вызывает полиурию (частое и обильное мочеиспускание). Вместе с водой организм теряет электролиты, калий, магний, натрий, фосфор. Уменьшение объема крови обусловливает развитие полидепсии (жажды).
В результате нарушения превращения углеводов в жиры, нарушения синтеза белков и усиленной мобилизации жирных кислот из жировых депо уменьшается масса тела больного и возникает полифагия (чрезмерный аппетит). Инсулиновая недостаточность приводит к значительным нарушениям жирового обмена: снижается синтез жира, усиливается его распад. В крови накапливаются недоокисленные продукты жирового обмена (кетоновые тела и др.) - происходит сдвиг кислотно-основного состояния в сторону ацидоза. Обезвоживание организма, резкие электролитные нарушения, ацидоз обусловливают развитие коматозного состояния при поздней диагностике сахарного диабета. 3. Клиническая картина, лабораторная диагностика, лечение. Клиническая картина. Сахарный диабет в детском возрасте чаще всего начинается остро. Период с момента появления первых симптомов до возникновения коматозного состояния составляет от 3-4 недель до 2-3 месяцев. У трети больных первыми клиническими проявлениями заболевания становятся признаки диабетического кетоацидоза. Для СД характерна триада так называемых больших симптомов: полидипсия, полиурия и снижение массы тела. Полидипсия бывает более заметной в ночные часы. Сухость во рту заставляет ребенка в течение ночи несколько раз просыпаться и пить воду. Грудные дети жадно захватывают грудь или соску, беспокойны, успокаиваются на короткое время только после питья. Полиурия при СД бывает как дневной, так и ночной. В дневное время на нее не обращают внимания ни сами дети, ни их родители. Первым замечаемым симптомом СД, как правило, становится ночная полиурия. При тяжелой полиурии развивается дневное и ночное недержание мочи. Характерный признак детского диабета - снижение массы тела в сочетании с чрезмерным аппетитом. При развитии кетоацидоза полифагия сменяется снижением аппетита, отказом от еды. Постоянным симптомом заболевания, часто регистрируемым уже в дебюте СД, являются кожные изменения. Кожа сухая, с выраженным шелушением на голенях и плечах. На волосистой части головы возникает сухая себорея. Слизистая оболочка полости рта обычно ярко-красная, сухая, язык яркий, темно-вишневого цвета («ветчинный»). Тургор кожи, как правило, снижен, особенно при резком обезвоживании. При медленно развивающемся заболевании имеют значение так называемые спутники СД - рецидивирующая инфекция кожи и слизистых оболочек (пиодермия, фурункулы, молочница, стоматиты, вульвиты и вульвовагиниты у девочек).
Дебют СД у девочек в пубертатном периоде могут сопровождать нарушения менструального цикла. Особенности сахарного диабета у детей раннего возраста. У новорожденных иногда наблюдается синдром преходящего (транзиторного) СД, который начинается с первых недель жизни, через несколько месяцев наступает спонтанное выздоровление. Чаще он встречается у детей с низкой массой тела и характеризуется гипергликемией и глюкозурией, приводящей к умеренной дегидратации, иногда к обменному ацидозу. Уровень инсулина в плазме крови нормальный. Течение. Сахарный диабет имеет, как правило, прогрессирующее течение. С увеличением длительности заболевания развиваются различные осложнения. Осложнения. К осложнениям сахарного диабета относятся: диабетическая ангиопатия различной локализации (диабетическая ретинопатия, диабетическая нефропатия, диабетическая нейропатия и др.), задержка физического и полового развития, диабетическая катаракта, гепатоз, диабетическая хай- ропатия (ограничение подвижности суставов). Диабетическая ретинопатия - типичное сосудистое осложнение СД. Она занимает одно из первых мест среди причин, приводящих к снижению зрения и слепоте у лиц молодого возраста. Инвалидность по причине нарушения зрения наблюдают более чем у 10% больных СД. Заболевание представляет собой специфическое поражение сетчатой оболочки и сосудов сетчатки. Начальные стадии ретинопатии могут не прогрессировать в течение продолжительного времени (до 20 лет). Прогрессирование процесса связано с длительностью заболевания при плохой компенсации метаболических нарушений, повышенным АД, генетической предрасположенностью. Диабетическая нефропатия - первично хронический процесс, приводящий к прогрессирующему гломерулосклерозу с постепенным развитием ХПН. Клинически выраженной стадии нефропатии всегда предшествуют годы транзиторной или постоянной микроальбуминурии. Для диабетической нейропатии характерно поражение чувствительных и двигательных нервных волокон дистального отдела нижних конечностей. К основным проявлениям нейропатии у детей относятся болевой синдром, парестезия, снижение сухожильных рефлексов. Реже отмечаются нарушение тактильной, температурной и болевой чувствительности. Возможно развитие вегетативной полинейропатии, проявляющейся дисфункцией пищевода, гастропатией, диареей, запорами. Задержка физического и полового развития наблюдается при возникновении СД в раннем возрасте и плохой компенсации заболевания. Крайняя степень выраженности этих симптомов (карликовость, отсутствие вторичных половых признаков у подростков, диспропорциональное ожирение с отложением жира на лице и верхней половине туловища, гепатоме- галия) носит название синдрома Мориака. Лабораторная диагностика. Лабораторными признаками СД являются: 1) гипергликемия (диагностически значим уровень глюкозы в плазме венозной крови выше 11,1 ммоль/л; в норме содержание глюкозы в плазме крови натощак составляет 3,3-3,5 ммоль/л); 2) глюкозурия различной степени выраженности (в норме глюкоза в моче отсутствует, глюкозурия возникает при повышении уровня глюкозы в крови выше 8,8 ммоль/л). Убедительный критерий для подтверждения диагноза СД 1-го типа (иммунологические маркеры инсулита) - аутоантитела к в-клеткам (1СА, GADA, 1АА) и белку в-клеток - глутаматдекарбоксилазе в сыворотке крови. Одним из современных методов диагностики нарушения углеводного обмена является определение содержания глико- зилированного гемоглобина. Для диагностики СД у детей этот показатель имеет большое значение. Кроме того, этот метод используют для оценки степени компенсации углеводного обмена у больных СД, находящихся на лечении. Содержание гликозилированного гемоглобина зависит от концентрации глюкозы в плазме крови и служит интегральным показателем состояния углеводного обмена в течение последних 3 месяцев, учитывая, что продолжительность жизни эритроцита 120 дней. Содержание гликозилированного гемоглобина составляет 4-6% общего гемоглобина в крови у здоровых лиц. Высокий уровень гликемии при СД способствует повышению процессов неферментативного гликозилирования белков гемоглобина, поэтому у больных СД его содержание в 23 раза превышает норму. При кетозе отмечаются гиперкетонемия, кетонурия (у детей кетонурию можно наблюдать при инфекционных заболеваниях, протекающих с высокой температурой, при голодании, особенно у детей раннего возраста). Для диагностики доманифестных стадий заболевания применяют стандартный глюкозотолерантный тест. Толерантность к глюкозе нарушена, если ее уровень в цельной капиллярной крови через 2 ч после пероральной нагрузки глюкозой (1,75 г/кг массы тела) находится в пределах 7,8-11,1 ммоль/л. В этом случае диагноз СД может быть подтвержден обнаружением аутоантител в сыворотке крови. Оценить функциональное состояние в-клеток у лиц с высоким риском развития СД, а также помочь в дифференциальной диагностике СД 1-го и 2-го типов дает возможность определение С-пептида в сыворотке крови. Базальная секреция С-пептида у здоровых лиц составляет 0,28-1,32 пг/мл. При СД 1- го типа его содержание снижено или не определяется. После стимуляции глюкозой, глюкагоном или сустакалом (питательной смесью с высоким содержанием кукурузного крахмала и сахарозы) концентрация С-пептида у больных СД 1-го типа не повышается, у здоровых - значительно возрастает. Лечение. Больные с впервые выявленным сахарным диабетом подлежат госпитализации. В дальнейшем лечение осуществляется в амбулаторно-поликлинических условиях. Основной задачей лечения является достижение и поддержание стойкой компенсации диабетического процесса. Это возможно только при использовании комплекса мероприятий, которые включают: соблюдение диеты, инсулинотерапию, обучение больного самоконтролю за проводимым лечением, дозированные физические нагрузки, профилактику и лечение осложнений, психологическую адаптацию к болезни. Диета с учетом пожизненной терапии должна быть физиологической и сбалансированной по белкам, жирам и углеводам, чтобы обеспечивать нормальное физическое развитие ребенка. Особенность диеты при СД - ограничение продуктов, содержащих большое количество быстровсасывающихся углеводов и уменьшение доли жиров животного происхождения (стол № 9). Оптимальное содержание питательных веществ в дневном рационе должно составлять 55% углеводов, 30% жиров, 15% белков. Больному рекомендуется 6-разовый прием пищи: три основных (завтрак, обед и ужин по 25% сахарной ценности пищи) и три дополнительных (второй завтрак и полдник по 10%, второй ужин - 5% сахарной ценности). Пищевые продукты с легкоусвояемыми углеводами (сахар, мед, конфеты, пшеничная мука, макаронные изделия, манная, рисовая крупы, крахмал, виноград, бананы, хурма) ограничивают. Их заменяют на продукты с большим количеством пищевых волокон, замедляющих всасывание глюкозы и липопротеидов общей и низкой плотности в кишечнике (ржаная мука, гречневая, пшенная, перловая, овсяная крупы, картофель, капуста, морковь, свекла, огурцы, помидоры, баклажаны, кабачки, брюква, перец). Для упрощения расчетов содержания углеводов в пищевых продуктах пользуются понятием «хлебная единица». Одну хлебную единицу составляют 12 г углеводов, содержащихся в продукте. Эквивалентная замена продуктов приведена в табл. 11. На 1 хлебную единицу обычно вводится 1,3 ЕД инсулина (12 г углеводов повышают уровень глюкозы в крови на 2,8 ммоль/л). Табл. 11. Эквивалентная замена продуктов по углеводам
Замена сахара осуществляется цикломатом, сорбитом, ксилитом и др. При применении сахарозаменителей необходимо учитывать возможность их побочного действия. Больных сахарным диабетом необходимо обучить основным принципам диетотерапии, расчету суточной калорийности пищи, адекватной замене продуктов питания, планированию питания в домашних условиях и вне дома. Инсулинотерапия. Лечение инсулином проводится больным пожизненно. Инсулинотерапия в детском возрасте должна осуществляться только человеческими генно-инженерными препаратами инсулина. Это связано с тем, что человеческие инсулины обладают минимальной иммуногенностью и хорошо переносятся больными. Для терапии заболевания используются препараты инсулина различной продолжительности действия (табл. 12). Табл. 12. Фармококинетическая характеристика препаратов инсулина
Инсулинотерапию необходимо начинать сразу после установления диагноза. Лечение начинают с препаратов инсулина короткого действия, инсулин при этом вводится 4-6 раз в сутки. Доза подбирается индивидуально, в зависимости от
уровня гликемии. Корригируют уровень глюкозы в крови, учитывая, что 1 ЕД инсулина снижает гликемию на 2,2 ммоль/л. В среднем доза составляет 0,5-0,8 ЕД/кгсут. После достижения нормогликемии переходят на сочетание в течение суток препаратов инсулина продленного действия (базальный инсулин) и препаратов короткого действия (инсулин, имитирующий посталиментарную секрецию). Соотношение пролонгированного и короткого инсулина подбирают индивидуально в соответствии с показателями уровня глюкозы в плазме крови в течение суток (рис. 54). Основные режимы инсулинотерапии: • 2 инъекции инсулина в день: перед завтраком 2/3 суточной дозы и перед ужином 1/3 суточной дозы - сочетание инсулина короткого действия и инсулина средней продолжительности действия. Причем 1/3 дозы каждой инъекции должен составлять инсулин короткого действия, а 2/3 - инсулин средней продолжительности действия; • 3 инъекции инсулина в день: комбинация инсулина короткого действия и инсулина средней продолжительности действия перед завтраком (40-50% суточной дозы), инъекция инсулина короткого действия перед ужином (10-15% суточной дозы) и инъекция инсулина средней продолжительности действия перед сном (40% суточной дозы); • базис-болюсная инсулинотерапия. Она заключается в том, что перед каждым основным приемом пищи вводят препарат инсулина короткого действия, а препарат инсулина пролонгированного действия - 1-2 раза в сутки, перед завтраком и перед сном (30-40% суточной дозы); • введение инсулина с помощью системы непрерывного подкожного введения инсулина («инсулиновой помпы»). Этот способ введения инсулина в настоящее время считается «золотым стандартом» инсулинотерапии. В «помпе» используются инсулиновые аналоги ультракороткого действия. В соответствии с заданной программой в непрерывном режиме вводится инсулин, имитируя базальную секрецию гормона в-клетками, а после еды - инсулин вводится в болюсном режиме, имитируя посталиментарную секрецию. Доза инсулина подбирается индивидуально. Для инсулинотерапии могут быть использованы смешанные препараты инсулина (миксты), сочетающие инсулины короткого действия и средней продолжительности действия: в детском возрасте применяется микстард ИМ 10; 20; 30; 40; 50, в котором содержится соответственно 10, 20, 30, 40 и 50 ЕД инсулина короткого действия. Начало действия смешанных препаратов соответствует инсулинам короткого действия, продолжительность действия - инсулинам средней продолжительности действия. В лечении сахарного диабета могут использоваться травы, усиливающие действие инсулина: листья черники, земляники, крапивы, одуванчика, а также стручки фасоли, элеутерококк, овес. Обязательным компонентом терапии является лечебная физкультура. При физических нагрузках усиливается утилизация глюкозы, снижается потребность в инсулине. Больным рекомендуется гигиеническая гимнастика, ходьба до 4-5 км в день, плавание, игра в бадминтон.
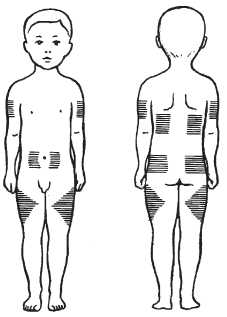
4. Особенности введения инсулина. Особенности введения инсулина. При введении инсулина необходимо строго соблюдать дозу, время и кратность введения. Сестра не имеет права производить замену одного препарата на другой. Перед введением инсулина флакон с суспензией необходимо встряхнуть до образования равномерной взвеси и подогреть до температуры 25-30 °С. Запрещается смешивать в одном шприце разные препараты инсулина, так как они способны инактивировать друг друга. Концентрированные препараты инсулина вводят специальными шприцами-ручками «Новопен», «Пливапен». Перед выполнением инъекции следует дождаться испарения спирта с обработанного участка кожи. Для профилактики липодистрофии (исчезновение подкожной жировой клетчатки) необходимо чередовать места введения инсулина (рис. 55). Между инъекциями в один и тот же участок должно пройти 2- 3 недели. Следует учитывать, что при подкожном введении в живот инсулин всасывается быстрее, чем в плечо или бедро. Горячие ванны, грелка, массаж ускоряют всасывание. При введении инсулина сестра должна контролировать прием пищи больными: через 15-20 мин после инъекции инсулина и через 33,5 ч при введении больших доз. Инсулин необходимо хранить в холодильнике при температуре +4... +6 °С.
5. Осложнения, комы и неотложная помощь при них.
Постинсулиновые липодистрофии захватывают подкожную клетчатку и достигают несколько сантиметров в диаметре. В основе Рис. 55. Места инъекций инсу- их развития лежит длительная лина (показаны штрихами) инъекционная травматизация мелких ветвей периферических нервов с последующими местными нейротрофическими нарушениями. Определенное значение в их возникновении имеет нарушение техники введения инсулина. Неотложные состояния. К острым неотложным состояниям при СД относят диабетический кетоацидоз, гипогликемию и гипогликемическую кому. Гиперосмолярную некетоацидоти- ческую кому и лактатацидоз в детском возрасте наблюдают крайне редко. Диабетический кетоацидоз - тяжелая метаболическая декомпенсация СД. Причинами развития диабетического кетоацидоза в 80% случаев является поздняя диагностика заболевания (нераспознанный СД) либо откладывание назначение инсулина по тем или иным причинам при установленном диагнозе. У больных, получающих инсулинотерапию, к развитию диабетического кетоацидоза приводят: 1) неправильное лечение (назначение недостаточной дозы инсулина или ее неравномерное распределение в течение суток); 2) нарушение режима инсулинотерапии (пропуск инъекций инсулина, использование просроченных препаратов); 3) грубые погрешности в диете (злоупотребление жирной и сладкой пищей); 4) нарушение техники введения инсулина (многократные инъекции в одно и то же место); 5) увеличение потребности в инсулине, которое может возникнуть в связи с интеркуррентными заболеваниями, хирургическим вмешательством, травмой и др. Тяжесть состояния при диабетическом кетоацидозе обусловливают резкая дегидратация организма, декомпенсированный метаболический ацидоз, выраженный дефицит электролитов, гипоксия и в большинстве случаев - гиперосмоляр- ность. Выделяют три стадии диабетического кетоацидоза. 1-я стадия (умеренный кетоацидоз) характеризуется слабостью, головокружением, головной болью. Появляются жажда, полиурия, боли в животе. Возникают расстройства со стороны желудочнокишечного тракта (анорексия, тошнота, рвота). Кожа бледная, сухая. Характерен рубеоз (диабетический румянец на скуловых дугах, над бровями, на подбородке). Слизистые оболочки сухие, яркие. Язык сухой, обложен густым налетом, в углах рта трещины. Выдыхаемый воздух имеет запах ацетона (прелых фруктов). 2- я стадия (прекома) наступает с декомпенсацией метаболического ацидоза на фоне прогрессирующей дегидратации. Клинический критерий 2-й стадии - шумное глубокое дыхание (дыхание Куссмауля). Больные заторможены, на вопросы отвечают с опозданием, односложно. Речь невнятная. Усиливается рвота. Нарастают симптомы обезвоживания. Слизистая оболочка рта, губы, язык - с трещинами, покрыты коричневым налетом. Снижен тонус глазных яблок. Развивается акро- и периоральный цианоз, увеличивается печень. Тоны сердца приглушенные. Отмечается тахикардия, снижается АД. Прекоматозное состояние может продолжаться от нескольких часов до нескольких дней. 3- я стадия - кетоацидотическая кома. К развитию комы при диабетическом кетоацидозе приводят: резкое обезвоживание клеток головного мозга, повышенное содержание азотистых шлаков, тяжелая гипоксия мозгая, гипокалиемия, ДВС- синдром, общая интоксикация и другие факторы. Клиническая картина кетоацидотической комы характеризуется отсутствием сознания, угнетением рефлексов. На фоне резкой дегидратации снижается диурез, прекращается рвота, нарастают тяжелые гемодинамические расстройства (тахикардия, нарушения сердечного ритма, падение АД и др.). Лабораторные критерии диабетического кетоацидоза: • кетоз - гипергликемия 11,1-20 ммоль/л, глюкозурия, ке- тонурия, рН крови не ниже 7,3, ВЕ до - 10; • прекома - гипергликемия 20-40 ммоль/л, глюкозурия, кетонурия, рН крови 7,3-7,1; ВЕ - 10-20; К+ и N+ эритроцитов снижены; гемоглобин и гематокрит повышены; • кома - гипергликемия 20-40 ммоль/л, глюкозурия, кето- нурия, рН крови ниже 7,1, ВЕ - ниже 20; К+ и N+ эритроцитов и сыворотки крови снижены, мочевина в крови повышена, гемоглобин и гематокрит повышены; осмолярность сыворотки 310-320 мосм/л. Лечение. Больные в состоянии кетоацидоза должны быть немедленно госпитализированы. Лечение кетоацидоза включает: 1) регидратацию организма; 2) ликвидацию инсулиновой недостаточности; 3) коррекцию электролитных нарушений; 4) купирование ацидоза; 5) симптоматическую терапию. После доставки больного в лечебное учреждение срочно определяется уровень глюкозы и кетоновых тел в крови и моче, рН, щелочной резерв, электролиты и остаточный азот. Затем каждый час контролируют уровень гликемии, глюкозурии, рН, измеряют АД, подсчитывают частоту дыхания и пульс. Больным с I и II стадией кетоацидоза для выведения кетоновых тел ставят очистительную клизму с 4%раствором натрия гидрокарбоната. Ребенка согревают, обеспечивают окси- генотерапию. При низком АД больному придают положение с опущенным изголовьем. Регидратационную терапию вне зависимости от стадии диабетического кетоацидоза начинают с внутривенного введения 0,9% раствора натрия хлорида. При гликемии ниже 14 ммоль/л вводят 5% раствор глюкозы с инсулином (на 5 г сухого вещества глюкозы - 1 ЕД инсулина). В связи с высокой вероятностью развития отека головного мозга жидкость следует вводить осторожно: 1-й час - 20 мл/кг, 2-й час - 10 мл/кг, 3-й час и далее - 5 мл/кг. Учитывая склонность больных к гипотермии, все растворы вводят подогретыми до 37 °С. Инсулинотерапия начинается одновременно с регидратацией. Для оказания неотложной помощи используется инсулин только короткого действия. Его вводят внутривенно. Инсулин нельзя смешивать с вводимыми жидкостими, его вводят отдельно со скоростью 0,1 ЕД/кг-ч. У детей раннего возраста эта доза может составлять 0,05 Ед/кг-ч. Снижение гликемии должно составлять не больше 45 ммоль/л-ч, поскольку более быстрое снижение влечет за собой развитие отека головного мозга. Коррекция уровня калия в крови проводится со второго часа лечения инсулином. Начальная доза 7,5% раствора калия хлорида - 0,3 мл/кг-ч. В последующем необходимо поддерживать уровень калия в крови в пределах 4-5 ммоль/л. Купирование ацидоза обычно не требуется, так как нормализация КОС происходит одновременно с лечением кетоацидоза благодаря регидратации и введению инсулина. Показанием для назначения бикарбонатов является снижение рН крови ниже 6,8. Обычно вводят 4%раствор гидрокарбоната натрия (2,5 мл/кг) внутривенно капельно медленно (в течение 1 ч). Необходимость симптоматической терапии определяется индивидуально. Гипогликемическая кома является исходом тяжелого гипогликемического состояния, если своевременно по разным причинам не предприняты меры к его купированию. Гипогликемия развивается при снижении содержания глюкозы в крови ниже 3 ммоль/л. Установлено, что среди больных СД она наблюдается в 25-58% случаев. Гипогликемия возникает при неправильном расчете дозы инсулина (ее превышении), погрешностях в диете (отсутствие приема пищи при введении инсулина), лабильном течении диабета (особенно у детей младшего возраста). В некоторых случаях она может развиться при чрезмерных физических нагрузках в часы максимального действия инсулина, психическом стрессе. При использовании препаратов короткого действия гипогликемия развивается вскоре или спустя 2-3 ч после инъекции. При введении инсулина продленного действия - в часы, соответствующие максимальному действию препарата. Симптомами гипогликемии являются острое чувство голода, быстро нарастающая слабость, повышенная потливость, мелькание «мушек» в глазах, дрожание рук и ног или всего тела, головокружение, головная боль. Характерно онемение губ, языка, подбородка. Часто отмечаются сонливость или, наоборот, немотивированное беспокойство, возбуждение, агрессивное поведение. При глубокой гипокликемии могут развиться гемиплегия, парезы, загруженность сознания, гипо- кликемическая кома (табл. 13).
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 60; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.109.201 (0.075 с.) |

 Осложнения инсулинотерапии. К ним относят гипогликемию (см. «Неотложные состояния») и постинсулиновые липодистропии.
Осложнения инсулинотерапии. К ним относят гипогликемию (см. «Неотложные состояния») и постинсулиновые липодистропии.


