
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Побудова градуювального графіку
У ряд мірних колб на 50 мл послідовно вносять робочий стандартний розчин 3. Визначення вмісту нітрит-іонів в аналізованій пробі води У колбу на 50 мл наливають пробу води, додають 0,1 г сухого реактиву Грисса або 5 мл 10%–вого розчину реактиву Грисса й перемішують. Через 40 хв. (без нагрівання) або 10 хв. (при нагріванні на водяній бані при 50 – 600С) вимірюють оптичну густину розчину. Вміст нітритів (мг/л) знаходять за градуювальним графіком.
13.5. Визначення вмісту Загальні положення Визначення Для визначення вмісту Контрольним параметром перевірки придатності електроду ЕЛІС – 121 Перед початком роботи ІСЕ–
(pNO3) складають у такий спосіб:
ІСЕ – розчин Пробу відбирають і аналізують у день проведення аналізу її консервують, додаючи на 1 л води 2 -4 мл хлороформу або 1 мл концентрованої сульфатної кислоти. Об'єм проби води для визначення вмісту нітратів не повинен бути меншим за 200 мл. Робота в лабораторії Посуд, реактиви, прилади 1. Іономер І–160 М. 2. Плівковий іон – селективний електрод для виміру активності іонів 3. Допоміжний хлоридсрібний електрод (ЕВЛ–1М3.1). Підготовку електродів до роботи здійснюють згідно з інструкціями, наведеними в паспортах до електродів. 4. Мірні колби ємкістю 100 мл 5. Піпетки ємкістю 10 мл. 6. Головний стандартний 0,1М розчин
Методика визначення
|
|||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 119; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.14.253.152 (0.007 с.) |
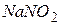 у кількості 0; 0,2; 0,5; 1,0; 2,0; 5,0;10; 15 мл і доводять до позначки дистильованою водою. Концентрація
у кількості 0; 0,2; 0,5; 1,0; 2,0; 5,0;10; 15 мл і доводять до позначки дистильованою водою. Концентрація  –іонів у цих розчинах відповідно дорівнює 0–0,004– 0,01–0,02– 0,04– 0,1– 0,2 – 0,3 мг/л. У колби додають 0,1 г сухого реактиву Грисса або 5 мл 10 %– вого розчину реактиву Грисса і перемішують. Забарвлення з'являється через 40 хв. без нагрівання або через 10 хв. при нагріванні на водяній бані при 50– 600 С і зберігається незмінним протягом 3 годин. Через 40 хв. розчини фотометрують у кюветах з товщиною оптичного шару 2 –5 см з зеленим світлофільтром (
–іонів у цих розчинах відповідно дорівнює 0–0,004– 0,01–0,02– 0,04– 0,1– 0,2 – 0,3 мг/л. У колби додають 0,1 г сухого реактиву Грисса або 5 мл 10 %– вого розчину реактиву Грисса і перемішують. Забарвлення з'являється через 40 хв. без нагрівання або через 10 хв. при нагріванні на водяній бані при 50– 600 С і зберігається незмінним протягом 3 годин. Через 40 хв. розчини фотометрують у кюветах з товщиною оптичного шару 2 –5 см з зеленим світлофільтром (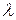 = 520 нм) відносно нульової проби, до якої доданий реактив Грисса. Градуювальний графік будують у координатах оптична густина - вміст нітритів (мг/л).
= 520 нм) відносно нульової проби, до якої доданий реактив Грисса. Градуювальний графік будують у координатах оптична густина - вміст нітритів (мг/л).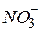 - іонів потенціометричним методом
- іонів потенціометричним методом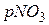 досліджуваної води здійснюють потенціометричним методом за допомогою іономера лабораторного І –160 М. При вимірюванні
досліджуваної води здійснюють потенціометричним методом за допомогою іономера лабораторного І –160 М. При вимірюванні 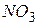 ( ІСЕ –
( ІСЕ – 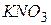 відносно хлоридсрібного електроду порівняння. Значення цього потенціалу при
відносно хлоридсрібного електроду порівняння. Значення цього потенціалу при 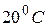 повинно бути в межах 420 ± 30 мВ.
повинно бути в межах 420 ± 30 мВ.
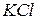 (нас.)
(нас.) 



