
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Розрахунок вмісту нітрат - іонів у воді (мг/л)
Визначене значення
де 62 - молярна маса нітрат - іона (г/моль).
Лабораторна робота № 14 Визначення вмісту іонів натрію потенціометричним методом Проробити такі питання: Сутність потенціометричного методу аналізу. Пряма потенціометрія (іонометрія). Будова іон–селективних і допоміжних електродів. Загальні положення У природних водах іони натрію займають одне з провідних місць серед катіонів за поширеністю. Оскільки всі солі натрію мають добру розчинність у воді, тому міграційні можливості іонів натрію досить широкі. Вміст іонів у природних водах коливається від декількох мг/л до сотень г/л. ГДК іонів натрію для питної води становить 200 мг/л. Визначення активності іонів натрію Для визначення вмісту Особливостями використання Контрольним параметром перевірки придатності електроду ЕЛІС – 112 Перед початком роботи ІСЕ –
Вимірювальний ланцюг при калібруванні електродів і вимірах показників активності (pN a) складають у такий спосіб:
розчин
Робота в лабораторії Посуд, реактиви, прилади 1. Іономер І–160 М. 2. Скляний іон – селективний електрод для виміру активності іонів 3. Допоміжний хлоридсрібний електрод (ЕВЛ–1М3.1). Підготовку електродів до роботи здійснюють згідно з інструкціями, наведеними в паспортах до електродів. 4. Мірні колби ємкістю 100 мл 5. Піпетки ємкістю 10 мл. 6. Головний стандартний 0,1М розчин 7. 25%-вий розчин
Методика визначення
|
|||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 123; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.45.92 (0.007 с.) |
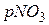 для проби води, що досліджують, занотовують до табл. 13.3. Виходячи з того, що
для проби води, що досліджують, занотовують до табл. 13.3. Виходячи з того, що 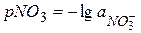 методом потенціювання визначають значення активності нітратних іонів
методом потенціювання визначають значення активності нітратних іонів 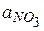 (у моль/л). Оскільки
(у моль/л). Оскільки 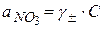 , то для знаходження
, то для знаходження 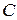 спочатку необхідно знайти коефіцієнти активності нітрат-іонів g± у досліджуваному розчині. Для цього за даними табл. 13.3 будують графік залежності g± = f (pNO3), за яким знаходять коефіцієнт активності нітратних іонів у досліджуваному розчині. Вміст нітрат–іонів (мг/л) розраховують за формулою
спочатку необхідно знайти коефіцієнти активності нітрат-іонів g± у досліджуваному розчині. Для цього за даними табл. 13.3 будують графік залежності g± = f (pNO3), за яким знаходять коефіцієнт активності нітратних іонів у досліджуваному розчині. Вміст нітрат–іонів (мг/л) розраховують за формулою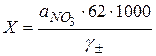
 [мг/л],
[мг/л],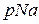 досліджуваної води здійснюють потенціометричним методом за допомогою іономера лабораторного І –160 М.
досліджуваної води здійснюють потенціометричним методом за допомогою іономера лабораторного І –160 М. – іонів у воді в якості індикаторного електроду використовують скляний іон–селективний електрод ЕЛИС–112
– іонів у воді в якості індикаторного електроду використовують скляний іон–селективний електрод ЕЛИС–112  (
(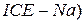 , електрод порівняння – хлоридсрібний електрод ЕВЛ–1М3.1.
, електрод порівняння – хлоридсрібний електрод ЕВЛ–1М3.1.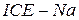 електроду є те, що його діапазон вимірювання
електроду є те, що його діапазон вимірювання  з обов’язковим контролем рН.
з обов’язковим контролем рН.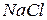 відносно хлоридсрібного електроду порівняння. Значення цього потенціалу при
відносно хлоридсрібного електроду порівняння. Значення цього потенціалу при 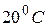 повинно бути в межах мінус 42 ± 10 мВ.
повинно бути в межах мінус 42 ± 10 мВ.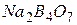 ), не допускаючи висихання його індикаторної частини. Перед виміром електрод калібрують не менше, ніж за двома контрольними розчинами
), не допускаючи висихання його індикаторної частини. Перед виміром електрод калібрують не менше, ніж за двома контрольними розчинами  ІСЕ –
ІСЕ – 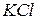 (нас.)
(нас.) 



