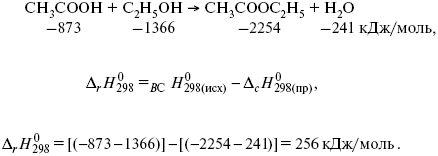Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Первое начало термодинамики.
Энтальпия. 3. Стандартная энтальпия образования вещества Стандартная энтальпия сгорания вещества. Стандартная энтальпия реакции. Закон Гесса. Применение первого начала термодинамики к биосистемам. 1. Если к закрытой системе подводить тепло, энергия будет расходоваться на увеличение внутренней энергии и совершение работы 2. Энтальпия - тепловой эффект химической реакции образования одного моля сложного вещества из соответствующих простых. H = U + pV 3. Стандартная энтальпия образования вещества - тепловой эффект реакции образования одного моля вещества из простых веществ, его составляющих, находящихся в устойчивых стандартных состояниях. Энтальпия образования простых веществ принято считать равной нулю
4. Стандартная энтальпия сгорания – тепловой эффект реакции сгорания одного моля вещества до образования высших оксидов. Для органических веществ – до CO2 и H2O. Теплота сгорания негорючих веществ принимается равной нулю. 5. Стандартная энтальпия реакции - разность между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ, умноженных на соответствующие коэффициенты в реакции (закон Гесса)
6. Поступление пищи обеспечивает энергию, которая используется для выполнения различных функций организма или сохраняется для последующего использования. Энергия высвобождается из пищевых продуктов в процессе их биологического окисления, которое является многоступенчатым процессом.
Энергия пищевых продуктов используется в клетках первоначально для синтеза ATФ. ATФ, в свою очередь, может использоваться как источник энергии почти для всех процессов в клетке.
Второе начало термодинамики. Обратимые и необратимые в термодинамическом смысле процессы. Энтропия. Энергия Гиббса. Прогнозирование направления самопроизвольно протекающих процессов в изолированной и закрытой системах; роль энтальпийного и энтропийного факторов. Термодинамические условия равновесия. 7. Стандартная энергия Гиббса образования вещества. Стандартная энергия Гиббса реакции. Примеры экзергонических и эндергонических процессов, протекающих в организме.
Принцип энергетического сопряжения. Энтропия
1. В изолированных системах самопроизвольно протекают только процессы, не сопровождающиеся уменьшением энтропии.
2. Обратимый процесс – процесс, в котором энтропия в замкнутой системе, включающей все участвующие в процессе тела, сохраняется. Этот процесс связан с изменением внешних условий.
3. Энтропия – мера беспорядка системы, состоящей из многих элементов
4. Энергия Гиббса(свободная) – функция, учитывающая оба фактора G = H - TS (TS-характеризует ту часть энергии, которую нельзя превратить в работу)
5. Энергия Гельмгольца – критерий направленности самопроизвольного протекания процесса. ▲ F =▲ U - T ▲ S ▲F<0 самопроизвольный ▲F=0 равновесный ▲F>0 несамопроизвольный
6. Условия равновесия: В изолированной системе – максимум энтропии, ▲G<0
7. Стандартная Энергия Гиббса образования вещества - ΔG°, изменение энергии Гиббса при реакции образования 1 моль вещества, находящегося в стандартном состоянии Для простых веществ равна нулю
8. Стандартная Энергия Гиббса реакции – разность между суммой энергий образования продуктов реакции и суммой энергий образования исходных веществ, умноженных на соответствующее количество вещества
9. Экзергонические реакции –системой совершается работа (гидролиз АТФ): Эндергонические реакции – над системой совершается работа (фосфорилирование глюкозы) 10. Принцип энергетического сопряжения, заключается в том, что энергия, необходимая для протекания эндергонической реакции, поступает за счет осуществления экзергонической реакции
Химическое равновесие.
|
|||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 234; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.77.114 (0.007 с.) |