Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Часть А. Дайте полное решение заданий. Укажите номер правильного ответа:
Укажите номер правильного ответа: 1. Массовая доля серной кислоты в растворе, полученном при смешивании 120 г 20%-ного и 40 г 50%- ного раствора, равна ____________________ г 1) 27,5 2) 42,3 3) 36,5 4) 37,7
2. Давление паров воды при 25оС составляет 3,167 кПа. Давление пара (кПа) над раствором в 450 г которого содержится 180 г глюкозы, равно ______ кПа 1) 1,267 2) 2,969 3) 1,198 4) 1,900
3. Уравнению реакции CaCO 3 + 2 HCl → CaCl 2 + CO 2 + H 2 O соответствует сокращенное ионное уравнение 1) 2) 3) 4)
4. Метилоранж красный при растворении в воде каждой из двух солей: 1) Fe(NO3)2 и CuSO4 3) ZnCl2 и Li2CO3 2) Na2SO4 и K2S 4) CrCl3 и KCl
5. В уравнении реакции, схема которой Fe(OH)3 +Br2 +KOH→ K2FeO4 +KBr +H2O, сумма коэффициентов 1) 31 2) 40 3) 45 4) 47 Дайте полное решение задания, используя ионно-электронный метод
Часть В. Выполните тестовые задания
Дополните: 1. Молярная концентрация раствора (См) показывает _____________________
2. Эквивалент металла рассчитывают по формуле Эме = ___________________
3. Процесс испарения любой жидкости протекает с ________________ тепла 4. Понижение температуры замерзания раствора от концентрации растворенного вещества отражает закон __________ и имеет математическое выражение ____________________________, где ________________________
5. Электролитическая диссоциация – это _______________________________ 6. Закон разбавления Оствальда устанавливает зависимость между __________ и имеет следующее математическое выражение ___________________________
7. Гидролиз соли протекает по аниону, если соль образована _____ рН = ___
8. Раствор, в 500 мл которого растворено 1,825 г HCl, имеет рН, равный ___
9. ЭДС рассчитывают по формуле _________________________________
10. В щелочной среде: а) недостаток кислорода в частице берём из _____ с образованием ______________________________________________ б) избыток кислорода в частице связываем _______ с образованием ______________________________________________________ Укажите номер правильного ответа: 11. Объём 0,1Н раствора NaOH, необходимый для нейтрализации 20 мл 0,2Н раствора хлороводородной кислоты равен __________________________ мл 1) 40 2) 35 3) 30 4) 20
12. Осмотическое давление раствора, содержащего 0,2 г растворенного вещества в 300 мл раствора при 27оС равно 27,7 кПа. Молярная масса растворенного вещества равна _____________________
1) 60 2) 30 3) 90 4) 66
13. Диссоциация по трём ступеням возможна в растворе: 1) хлорида алюминия 3) нитрата алюминия 2) ортофосфата калия 4) ортофосфорной кислоты
14. К сильным электролитам относятся (несколько вариантов ответа): 1) PbI2 2) H2CO3 3) NaOH 4) Al2(SO4)3
15. Уравнение реакции практически осуществимой в водном растворе имеет вид 1) Ba(NO3)2 + K2SO4 → BaSO4 + 2KNO3 2) BaCl2 + 2KOH → Ba(OH)2 + 2KCl 3) ZnCl2 + H2SO4 → ZnSO4 + 2HCl 4) Na2SO4 + 2KOH → K2SO4 + 2NaOH 16. Одним из продуктов гидролиза ортофосфата натрия по второй ступени является 1) NaH2PO4 3) Na2HPO4 2) H3PO4 4) NaHPO4
17. Щелочная среда образуется при растворении в воде каждой из двух солей 1) KNO3 и K3PO4 3) K2S и K3PO4 2) FeSO4 и KCl 4) K2SO4 и CH3COOK
18. В уравнении для расчета константы гидролиза цианида натрия не учитывается значение концентраций 1) 19. Только окислительные свойства проявляет вещество 1) KClO4 2) KCl 3) KClO3 4) Cl2
20. Окислительно-восстановительную двойственность проявляют (два варианта ответа) 1) H2SO4 2) Na2SO3 3) H2S 4) S
ВАРИАНТ № 4
|
|||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 149; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.105.239 (0.008 с.) |
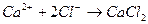
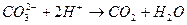
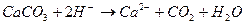
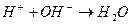
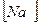 2)
2) 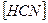 3)
3)  4)
4)