Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Часть А. Дайте полное решение заданий
Укажите номер правильного ответа: 1. Электронная формула 1)
2. Пространственная конфигурация молекулы – тетраэдрическая соответствует частицам (два варианта ответа): 1)
3. Реакция протекает по уравнению: SO3 (г) + 2KOH = K2SO4 + H2О ∆Н = – 472,22 КДж ∆Н0обр. КДж/Моль –425,93 –1433,44 −285,84
Теплота образования SO3 (∆Н0 обр. SO 3) равна: 1) − 395,2 КДж/Моль 3) + 790,4 КДж/Моль 2) + 395,2 КДж/Моль 4) − 790,4 КДж/Моль 4. Если энтальпия образования Р2O3 равна (− 820 КДж/моль), то количество теплоты, выделяемое при сгорании 31 г фосфора, равно _____________ КДж 1) 200 2) 410 3) 600 4) 820 5. При проведении обратимой реакции 2SО2 (г) + О2 (г) ↔ 2SО3 (г) начальные концентрации SО2 и О2 были соответственно равны 0,4 и 0,3 моль/л, а в состоянии равновесия концентрация SО3 составила 0,2 моль/л, тогда константа равновесия равна _____________________________________ 1) 5 2) 10 3) 9,5 4) 15 Часть В. Выполните тестовые задания Дополните: 1. Химический элемент − это _________________________________________
2. Магнитное квантовое число обозначают буквой ______________, принимает значения _______________, характеризует ___________________ 3. В I группе (главной подгруппе
4. Ковалентная неполярная связь встречается в молекулах, образованных _____
5. Особенности 2) _________________________________________ 3) _________________________________________ 6. Тепловой эффект реакции – это _____________________________________ 7. Стандартная теплота образования – это ______________________________ 8. Принцип Ле Шателье читается так _________________________________ 9. Математическое выражение Кр для реакции: СO(г) + Н2О(г) ↔ СO2 (г) + Н2 (г) имеет вид: ________________________________________________________ Укажите номер правильного ответа: 10. Четыре свободные
1)
11. Электронная формула иона 1) К 2) Ar 3) S 4) Cl
12. Атому 1)
13. Низшая степень окисления для элемента с электронной формулой 1)
14. Вещества с ковалентной неполярной связью это: 1) водород 3) фтороводород 2) алюминий 4) вода 15. 1)
16. Оксид легко разлагается при нагревании: 1) ½ О2 + Са → СаО, ∆Н= − 635,97 КДж/Моль 2) ½ О2 + 2Ag → Ag2O, ∆H= − 30,56 КДж/Моль 3) ½ O2 + Ba → BaO, ∆H= −558,51 КДж/Моль 4) ½ O2 + Fе → FеO, ∆H= − 263,68 КДж/Моль 17. Основные свойства преобладают в большей степени у оксида (подтвердите расчётами): 1) MgO (k) + CO2 (г) → MgCO3 (k) ∆G0 КДж/Моль –602,22 –394,38 –1029,3 2) ВaO + CO2 → ВaCO3 ∆G0 КДж/Моль –528,4 –394,38 –1139 18. Если температурный коэффициент скорости химической реакции равен 2, то при понижении температуры от 60оС до 20оС скорость реакции _________ 1) увеличивается в 16 раз 3) увеличивается в 6 раз 2) уменьшается в 8 раз 4) уменьшается в 16 раз
19. Для смещения равновесия в системе N2 (г) + О2 (г) ↔ 2NО(г) ∆Н > 0 в сторону продуктов реакции необходимо _____________________________ 1) повысить давление 3) повысить температуру 2) ввести катализатор 4) уменьшить давление
20. При повышении давления в 4 раза скорость реакции СO(г)+Cl2 (г)→СOCl2(г) увеличивается 1) в 64 раза 2) в 8 раз 3) в 16 раз 4) в 12 раз
ВАРИАНТ № 2
|
|||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 158; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.218.184 (0.008 с.) |
 соответствует атому:
соответствует атому: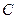 2)
2) 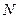 3)
3)  4)
4) 
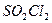 2)
2) 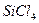 3)
3) 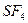 4)
4) 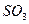
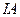 ) от лития к францию радиус атома _____, энергия ионизации ____, ОЭО _____, металлические свойства _______
) от лития к францию радиус атома _____, энергия ионизации ____, ОЭО _____, металлические свойства _______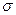 – связи: 1) _________________________________________
– связи: 1) _________________________________________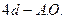 имеет атом:
имеет атом: 2)
2) 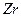 3)
3) 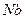 4)
4) 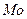
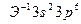 соответствует атому:
соответствует атому: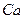 в возбужденном состоянии соответствует электронная формула:
в возбужденном состоянии соответствует электронная формула: 2)
2) 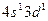 3)
3)  4)
4) 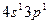
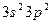 равна:
равна: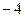 2)
2) 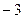 3)
3) 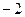 4)
4) 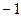
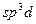 − гибридизация в следующей частице:
− гибридизация в следующей частице: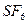 2)
2) 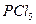 3)
3) 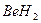 4)
4)