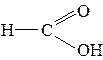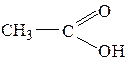Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Карбоновые кислоты, краткая характеристика и свойства. Уксусная кислота ⇐ ПредыдущаяСтр 10 из 10
Карбоновые кислоты – это кислородосодержащие органические вещества, имеющие в составе одну или несколько карбоксильных групп:
По характеру радикала карбоновые кислоты делятся на: – предельные:
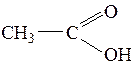
– непредельные:

– ароматические:
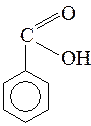
Уксусная кислота является бесцветной жидкостью, летучая, с резким запахом, очень едкая, между молекулами есть водородные связи, хорошо растворяется в воде. Уксусная кислота является органической кислотой средней силы, поэтому для нее характерны все свойства кислот, вступает в реакции замещения и обмена: реагирует с металлами, оксидами металлов, гидроксидами с образрванием солей ацетатов, также может реагировать со спиртами с образованием эфиров.
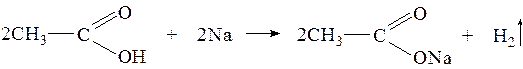
2СН3СООН + 2Na = 2CH3COONa + H2↑ 2НСООН + CaO = (HCOO)2Са + H2О 2CН3СООН + Cu(OH)2 = (CH3COO)2Сu + 2H2О Также уксусная кислота может вступать в реакции обмена с солями 2CН3СООН + Na2CO3 = 2CH3COONa + H2О + CO2↑ При сгорании на воздухе образуется СО2 и вода. Аминокислоты, краткая характеристика и свойства. Глицин и аланин
Аминокислоты – это органические соединения, имеющие в составе, одновременно, одну или несколько карбоксильных групп –СООН, а также одну или несколько аминогрупп – NH 2 Основные представители:
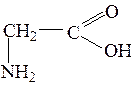 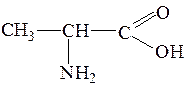
Аминокислоты имеют свойства оснований и кислот, то есть обладают амфотерными свойствами: могут реагировать как с кислотами, так и с гидроксидами и оксидами металлов, также могут образовывать внутренние соли. При взаимодействии аминокислот друг с другом образуются пептиды и белки.
Жиры, белки, углеводы Жиры – это сложные эфиры, образованные глицерином и жирными кислотами. Жиры являются основными источниками энергии для многих животных, образуя подкожные жировые клетчатки, также выполняют строительную функцию, входят в состав клеточных мембран (фосфолипиды), рпедают эластичность костям и хрящам, образуют многие гормоны, например, женский гормон астроген.
При действии щелочей на жиры образуются соли жирных кислот (мыла) и глицерин, поэтому такие реакции называют омылением жиров. Жидкие жиры содержат остатки непредельных кислот (растительные жиры), а твердые жиры содержат остатки предельных кислот (животные жиры), и при пропускании водорода жидкие жиры переходят в твердые – этот процесс называется гидрогенизация, таким образом из дешевых растительных жиров получают дорогие твердые жиры, используемые как заменители молочного жира в продуктах питания. Таблица жирных кислот
Белки являются природными биополимерами, содержат остатки аминокислот, имеют различную структуру: линейную (первичная),спиральную (вторичная), клубочную (глобулины) – третичная. Белки содержатся в мясе, яйцах, рыбе, бобовых, морепродуктах. При варке идет разрушение вторичной и третичной структуры – этот процесс называется денатурацией белка. Белки имеют прочную структуру, обеспечивают строительную функцию – из белков построены мышцы, из белка коллагена состоят волосы и ногти, транспортную – перенос веществ в организме, защитную – имуноглобулины и т-фаги поедают и уничтожают вирусные тела. При сжигании белков образуется запах жженых перьев.
Углеводы – это кислородосодержащие органические соединения, общая формула которых Cn (H 2 O) m Простейший углевод – глюкоза С6Н12О6. Входит в состав обычного сахара, который называется сахарозой. Является белым кристаллическим веществом, хорошо растворимым в воде, без запаха, имеет сладкий вкус, имеет в составе 5 гидроксильных групп и обладает свойствами многоатомных спиртов, а также имеет альдегидную группу и обладает также свойствами альдегидов.
Поэтому может реагировать с кислотами, гидроксидом меди, щелочными металлами, аммиачным раствором оксида серебра. В твердом виде образует циклическую форму. Входит в состав многих углеводов, таких как крахмал и целлюлоза. Углеводы как правило имеют энергетическую функцию и являются источниками энергии, содержатся в овощах, фруктах, растительных продуктах, крупах. Для растений еще выполняют и строительную функцию – образуют кору, клетчатку. Горят на воздухе, образуя СО2 и воду.
68. Взаимодействие солей меди и серебра, оксида и гидроксида меди и серебра с раствором аммиака, образование комплексных соединений. Cu2O + 4NH3 + H2O = 2[Cu(NH3)2]OH Ag2O + 4NH3 + H2O = 2[Ag(NH3)2]OH Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2
Соли меди и серебра также способны реагировать с раствором аммиака NH3 с образованием растворимых комплексных солей: CuSO4 + 4NH3 = [Cu(NH3)4]SO4 AgCl + 2NH3 = [Ag(NH3)2]Cl
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 54; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.111.9 (0.01 с.) |