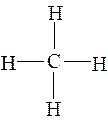Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Качественные реакции на ионы. Реакции обнаружения.
Cu2+ - добавление щелочи КОН – выпадение голубого осадка Cu(OH)2 Fe2+ - добавление щелочи КОН – выпадение зеленого осадка Fe(OH)2 постепенно буреющего Fe3+ - добавление щелочи КОН – выпадение бурого осадка Fe(OH)3 Pb2+ - добавление KI – выпадение золотистого осадка PbI2 Ag+ - добавление KCl или HCl – выпадение белого осадка AgCl, нерастворимого в кислотах Ва2+ - добавление H2SO4 – выпадение белого осадка ВаSO4, нерастворимого в кислотах Са2+ - добавление Na2CO3 – выпадение белого осадка СаCO3, который при добавлении кислоты растворяется и выделяется углекислый газ СО2 Zn2+ Al3+ - добавление щелочи КОН, при этом выпадает белый осадок, который растворяется при дальнейшем добавлении щелочи NH4+ - добавление щелочи КОН – выделяется бесцветный газ аммиак NH3 SO42- - добавление BaCl2 при этом выпадает белый осадок ВаSO4, нерастворимый в кислотах NO3- - добавление концентрированной серной кислоты, выделяется бурый газ NO2 S2- - добавление кислоты, выделяется газ с запахом тухлых яиц H2S, или добавить Pb(NO3)2, выпадет черный осадок PbS SO32- - добавить кислоту, при этом выделиться бесцветный газ SO2 PO43- - добавить СaCl2 выпадет белый осадок Са3(РО4)2 или добавить AgNO3, выпадет желтый осадок Ag3 PO4 CO32- - добавить СaCl2 выпадение белого осадка СаCO3, который при добавлении кислоты растворяется и выделяется углекислый газ СО2 Или добавить кислоту и выделится газ СО2 SiO32- - добавить кислоту и выпадет белый осадок Н2SiO3 Cl- добавить AgNO3 выпадет белый осадок AgCl не растворимый в кислотах Br- добавить AgNO3 выпадет желтоватый осадок AgBr не растворимый в кислотах I- Добавить азотную кислоту, перекись водорода, перманганат калия или другой сильный окислитель, при этом выпадет фиолетовый осадок I2 Алканы, краткая характеристика и свойства. Метан Алканы – это предельные углеводороды, общая молекулярная формула которых C n H 2 n +2
К алканам относится следующий ряд веществ (гомологический ряд):
Метан – газ без цвета и запаха, легче воздуха, взрывоопасен, является предельным углеводородом, все связи одинарные, прочные, насыщенные,
Валентность атома С во всех органических соединениях равна IV Алканы вступают в реакции замещения с галогенами (хлором, бромом) на свету, также с азотной и серной кислотой, могут разлагаться с отщеплением водорода или разлагаться на две более мелких углеводорода (крекинг). Они не растворимы в воде, и поэтому с ней не реагируют При горении в кислороде (на воздухе) образуют СО2 и воду 2С2Н6 + 7О2 = 4СО2 + 6Н2О
Алкены, краткая характеристика и свойства. Этилен
Алкены – это непредельные углеводороды, имеющие в составе одну двойную связь, общая молекулярная формула которых C n H 2 n
Они вступают в реакции присоединения с разрывом двойной связи, могут реагировать с водородом (гидрирование) с образованием алканов, с галогенами (галогенирование) – хлором, бромом (обесцвечивать бромную воду) при обычных условиях, с галогенводородами (гидрогалогенирование), с водой с образованием спиртов (гидратация), могут окисляться – обесцвечивать раствор KMnO4. Горят они также как и алканы с выделением СО2 и воды. Этилен может всупать в реакцию полимеризации – образуя полимер полиэтилен. Этилен – газ без цвета и запаха, легче воздуха, также взрывоопасен, является непредельным углеводородом, так как имеет двойную связь, которая в отличие от одинарных слабая и легко рвется.
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 59; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.81.94 (0.005 с.) |