
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Влияние температуры на скорость реакции
(правило Вант-Гоффа) При повышении температуры на каждые 10° скорость большинства химических реакций увеличивается в 2–4 раза, и, наоборот, при понижении температуры – понижается соответственно во столько же раз. Математическая зависимость скорости реакции от температуры приближенно выражается уравнением Вант-Гоффа
где Шведский ученый С. Аррениус на основании экспериментальных данных показал, что число активных частиц, а следовательно, скорость и константа скорости возрастает с температурой по экспоненциальному закону. Выведенная им зависимость константы скорости
где k0 – предэкспоненциальный множитель; R – универсальная газовая постоянная 8,31 Дж/(моль К); Т – абсолютная температура; Энергия активации – минимальная энергия, которой должны обладать сталкивающие молекулы, чтобы преодолеть потенциальный барьер, разделяющий исходное и конечное состояние системы. Она зависит от природы реагирующих веществ, температуры, ее значения включают в специальные справочники и используют в химической технологии для расчета скоростей реакций в различных условиях.
Влияние катализатора на скорость реакции Одним из способов увеличения скорости реакции является снижение энергетического барьера, т. е. уменьшение Катализ – изменение скорости химической реакции веществами (катализаторами), которые участвуют в промежуточных стадиях реакции, но не входят в состав конечных продуктов. Катализатор – вещество, влияющее на скорость реакции, но к концу реакции остающиеся химически неизменными. На применении катализаторов основано получение большинства продуктов химического производства. Каталитическое действие является основой жизнедеятельности и в природе. Все химические превращения в организмах инициируются особыми катализаторами – ферментами.
В зависимости от того, находится ли катализатор в той же фазе, что и реагирующие вещества, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе. Механизм каталитического действия для них не одинаков, однако, и в том и в другом случае происходит ускорение реакции за счет снижения Ea .
Химическое равновесие Различают обратимые и необратимые реакции. Необратимыми реакциями называются такие, после протекания которых систему и внешнюю среду одновременно нельзя вернуть в прежнее состояние. Многие химические реакции являются обратимыми, т.е. одновременно протекают в двух противоположных направлениях и не доходят до конца. Особенность обратимых реакций состоит в том, что по мере накопления продуктов реакции возрастает скорость обратной реакции. Если они сравняются, то наступает равновесное состояние. Химическое равновесие характеризуется константой химического равновесия Для реакции аА + вВ «сС + dD, из ЗДМ (7.2) следует:
где Константа химического равновесия определяется отношением произведений равновесных концентраций продуктов реакции на произведение равновесных концентраций исходных веществ, взятых в степенях их стехиометрических коэффициентов. В выражение константы равновесия входят только концентрации газообразных и растворенных веществ.
В условиях равновесия все реагенты связаны друг с другом через концентрации, и изменение одной из них вызовет изменение других, только соотношение равновесных концентраций останется постоянным при данной температуре. Константа химического равновесия может быть рассчитана из изотермы Вант-Гоффа при DG = 0, являющейся термодинамическим условием химического равновесия:
Константа равновесия имеет большое теоретическое значение и практическое значение. По ее величине можно судить о полноте протекания реакции. Если
|
||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 141; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.234.83 (0.006 с.) |
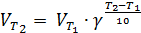 , (7.4)
, (7.4)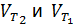 — скорости реакции при температурах Т1 и Т2 соответственно;
— скорости реакции при температурах Т1 и Т2 соответственно; 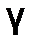 – температурный коэффициент скорости реакции для многих реакций у лежит в пределах 2–4.
– температурный коэффициент скорости реакции для многих реакций у лежит в пределах 2–4.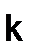 от температуры Т называется уравнением Аррениуса:
от температуры Т называется уравнением Аррениуса: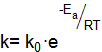 , (7.5)
, (7.5)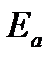 – энергия активации, кДж/моль.
– энергия активации, кДж/моль.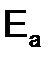 . Это достигается введением катализаторов.
. Это достигается введением катализаторов.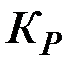 .
.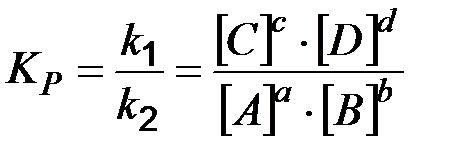 , (7.6)
, (7.6)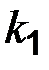 и
и 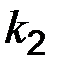 – константы скоростей прямой и обратной реакций;
– константы скоростей прямой и обратной реакций; 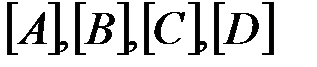 – равновесные концентрации веществ соответственно.
– равновесные концентрации веществ соответственно.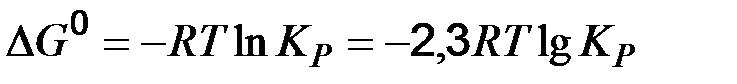 , следовательно,
, следовательно,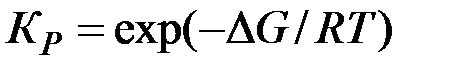 . (7.7)
. (7.7)


