
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Роль молекул растворителя в процессах электролитической диссоциации. Гидратация и гидратная оболочка ионов.
Установлено, что в растворах содержится относительно устойчивые молекулярные группы растворителя Н2О и растворенного вещества – гидраты. Гидратация – процесс образования гидратов. Энергия гидратации – энергия, выделяющаяся за счет образования гидратов. В полярных растворителях она тем больше, чем больше плотность заряда q / r частицы (c зарядом q и радиусом r), окружаемой молекулами воды. Энергия гидратации понижает энтальпийную часть свободной энергии ΔG и, т.о. процесс гидратации способствует стабилизации системы. В отличие от процессов гидролиза при гидратации не происходит обменного взаимодействия вещества с водой. При кристаллизации из растворов выделяются кристаллогидраты, например, CuSO4∙ 5 H2O, Na2SO4∙ 10 H2O и т.п. 1. Ионные соединения. Процесс растворения ионных соединений связан с разрушением кристаллической решетки. Если энергия кристаллической решетки (ЭКР) больше энергии гидратации, то кристаллическое вещество не растворится в воде, если ЭКР меньше энергии гидратации, то кристаллическое вещество растворится. NaCl(крист.) + H2O(растворитель) → Na+ H2O + Cl-H2O, где ионы окружены гидратной оболочкой. Обратный процесс (←) – молизация происходит при удалении растворителя. Роль растворителя для ионных соединений – разделение готовых ионов и препятствие к их объединению 2. Ковалентные соединения. HCl + H2O(растворитель) → H+ H2O + Cl-H2O Роль растворителя для ковалентных соединений – разрыв связей с переносом электрона (гетеролитический разрыв связей) Более точное представление этой реакции соединениями с гидратными оболочками: благодаря связыванию иона Н+ с неподеленной электронной парой атома кислорода молекулы растворителя Н2О образуется достаточно прочный комплекс Н2О---Н+ (или ион гидроксония Н3О+) и гидратированный анион [Cl ∙nH2O]-: HCl + H2O(растворитель) → Н3О++ [Cl ∙nH2O]- Обычно, чтобы не загромождать уравнения диссоциации гидратные оболочки не указывают. Наиболее сильные растворители – полярные. Силы притяжения частиц в растворах подчиняются закону Кулона: Fпритяж. = q1q2/ 4πε0r2 (47) Значения диэлектрической постоянной ε0(H2O) = 80, ε0(NH3) = 28, ε0(HF) = 84, то есть сила притяжения ионов уменьшается в полярных растворителях. В растворах некоторых электролитов диссоциирует лишь часть молекул. Для количественной характеристики электролитической диссоциации было введено понятие степени диссоциации - это отношение числа распавшихся на ионы молекул (n1) к общему числу молекул (n0), изначально попавших в раствор:
α = n1/n0 (48) Например, в растворе НСl более 99% молекул хлороводорода распадаются на ионы H+ и Cl–. Таким образом, НСl в водном растворе– это не просто электролит, а сильный электролит: Поэтому обратную стрелку в уравнении диссоциации HCl часто вообще не пишут: HCl → H+ и Cl– Вместе с тем похожее соединение – раствор HF – не проявляет свойств сильного электролита и в растворе ток проводит плохо. Здесь, наоборот, в уравнении диссоциации нужна более длинная обратная стрелка: HF Теорию электролитической диссоциации в 80-х годах XIX века предложил выдающийся шведский химик Сванте Аррениус (1859-1927) Исходя из степени диссоциации, все электролиты делятся на две группы 1. Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, основания щелочных и щелочноземельных металлов, а также кислоты (HCl, HBr, HI, HClO4, HClO3, HMnO4, HNO3, H2SO4, H2SeO4, H2Cr2O7 и некоторые другие). 2. Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят растворы все остальных электролитлв. Между этими двумя группами чёткой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого. Такое деление условно, но оно очень удобно для написания ионных уравнений химических реакций: достаточно принять за правило, что только сильные электролиты можно записывать в ионном виде, а слабые – нет. В растворах электролитов, наряду с процессом диссоциации на ионы, происходит и обратный процесс – ассоциация ионов в нейтральные молекулы. Таким образом, электролитическая диссоциация – это обратимая химическая реакция или динамическое равновесие, к которому применимы те же закономерности, что и к любому другому химическому равновесию. Для описания процесса диссоциации можно использовать константу равновесия Кр, которая в данном случае будет называться константой диссоциации Ка. Маленький индекс (а) означает «acid - кислота». Значения Ка для сильных электролитов часто бывают настолько велики, что их не удается измерить непосредственно. Эти значения получают косвенно, из термодинамических данных, и в разных справочниках они могут отличаться, хотя и остаются очень большими. Для нас важно то обстоятельство, что ионов H+ и Cl– в растворе очень много (их концентрация – в числителе дроби), а недиссоциированных молекул [HCl] чрезвычайно мало. Напротив, значения Ка для слабых электролитов намного меньше единицы, например, для раствора фтороводорода Ка = 6,8 ∙ 10-4. Следовательно, в растворе много недиссоциированных молекул HF и мало ионов H+ и F–.
K процессу диссоциации применим принцип Ле Шателье. Рассмотрение с позиций этого принципа уравнения HCl + H2O(растворитель) → Н3О++ [Cl ∙nH2O]- указывает нам на еще одну важную закономерность: если разбавлять раствор хлороводородной кислоты, т.е. добавлять в него воду, то по принципу Ле Шателье должен активизироваться процесс, связанный с расходованием воды, т.е. прямая реакция (распад на ионы). В этом случае в растворе должен активизироваться процесс образования ионов из молекул. Иными словами, при разбавлении растворов слабых электролитов степень диссоциации возрастает.
|
||||||
|
Последнее изменение этой страницы: 2021-01-14; просмотров: 484; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.217.67.16 (0.005 с.) |
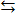 H+ и F–
H+ и F–


