Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Параметры тела при заданных параметрах и при заданных параметрах окружающей среды.
а) Р = const
П = Тос∆S – потеря энергии Всякое увеличение энтропии системы есть качественная мера потери ее работоспособности, вследствие протекания в системе необратимых процессов, протекающих в системе.
Основные термодинамические процессы. 1) Изобарный процесс Р = const; 2) Изохорный процесс V = const; 3) Изотермический процесс T = const; 4) δq = 0 (q = 0) адиабатный процесс; 5) Политропный процесс – CП = const
Этапы исследования термодинамических процессов. 1) 1)Вывод уравнения процесса и установление взаимосвязи между параметрами состояния; 2) 2)расчет работы и теплоты процесса; 3) 3)определение изменения калориметрических параметров (∆U, ∆h, ∆S)
При исследовании за основу берется уравнение PV = const. PV = RT Уравнение I закона термодинамики:
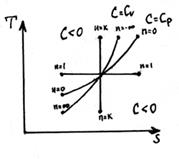
Политропный процесс. СП = const PVn = const – уравнение политропы, n - показатель политропы, - ∞ ≤ n ≤ + ∞ n = 0 → P = const, n = 1 → T = const, n = k → адиабатный n = ∞ → ν = const 1 < n < k для (реальных) идеального газа
Определение работы в политропном процессе.
P, V – текущие значения
для идеального газа:
Теплота политропного процесса:
Изменение ∆U, ∆h, ∆S:
Изображение процесса в P – V и T – S координатах:
Адиабатный и изоэнтропийный процесс.
Водяной пар. Термодинамические свойства воды и водяного пара. Существует 7 видов льда: 1) 0,001˚ С, Р = 611 кПа; 2) - 22˚ С, Р = 207,5 МПа; 3) - 34,7˚ С, Р = 213 МПа; 4) - 24,3˚ С, Р = 344 МПа; 5) - 17˚ С, Р = 346 МПа; 6) 0,16˚ С, Р = 637 МПа; 7) 81,6˚ С, Р = 2200 МПа.
Критическая температура – это максимально возможная температура сосуществования двух фаз: жидкости и насыщенного пара. Тройная точка – это то единственное состояние, в котором могут одновременно находиться в равновесии лед, вода и пар. Пар можно получить при кипении и испарении. Пар при испарении теоретически образуется при любой Т, а при кипении - при Т насыщения. Процесс конденсации обратный парообразованию.
Пар. 1) Насыщенный – при параметрах насыщения Рн и tн 2) перегретый – имеет Т больше, чем температура насыщения пара такого же давления.
- влажный насыщенный – содержит капли влаги; - сухой насыщенный – не содержит влаги;
Вводится дополнительный параметр: х – степень сухости, 0 ≤ х ≤ 1
х = 0 – кипящая жидкость (V’, h’, S’); х = 1 – сухой насыщенный пар (V’’, h’’, S’’) 0 ≤ х ≤ 1 – влажный насыщенный пар (Vx, hx, Sx)
V, h, S – параметры воды и перегретого пара.
¦ (Р, t)
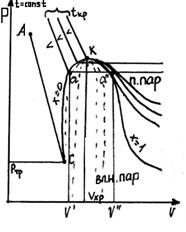
Тройная точка: tтр = 0,01˚ С Ртр = 611 Па, V = 0,001 Критическая точка: tкр = 374,12˚ С Ркр = 221,15 бар = 22,115 МПа, V = 0,003147
P, V; T, S; h, S
C – тройная точка; t > tн Изобарно-изотермический процесс К – критическая точка; АС – таяние льда. Удельная теплота парообразования – это теплота, которую необходимо подвести к 1 кг кипящей жидкости с тем, чтобы ее полностью превратить в сухой насыщенный пар. B, T, S – r площадь, а b, h, s – r длина отрезка. Первая часть таблицы связана с рассмотрением водяного пара в состоянии насыщения.
1 бар 99,63 100 1,003 Вторая часть таблица для воды и перегретого пара.
V, h, S → ¦ (P, t) (Истечение газов и паров) Влажный воздух. O2 N2 CO2 Ar H2O Влажный воздух = сухой воздух + пары Н2О
Закон Дальтона:
Парциальное давление компонента – это давление, которое имел бы компонент, если бы занимал весь объем. Параметры влажного воздуха. 1) абсолютная влажность численно равна массе пара в 1 м3 влажного воздуха.
2) относительная влажность – отношение действ. абсолютной влажности к ее максимальному значению при той же t смеси.
3) влагосодержание – это отношение массы водяного пара к массе сухого воздуха.
4) температура точки россы – это t, при которой влажность воздуха достигает температуры насыщения, и водяной пар будет конденсироваться.
5) теплоемкость смеси:
6) энтальпия влажного воздуха:
ЛЕКЦИЯ №8
j - относительная влажность воздуха d - влагосодержание воздуха.
Рв.п. – абсолютная влажность.
|
||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 93; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.66.13 (0.019 с.) |
|||||||||||||||||||||||||||||||



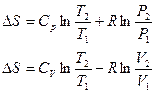




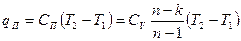

 уравнение Майера
уравнение Майера



 ¦ (Pн, tн)
¦ (Pн, tн)
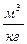


 удельная теплота парообразования
удельная теплота парообразования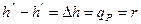
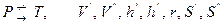




 , max значение имеет при параметрах насыщения.
, max значение имеет при параметрах насыщения.
 - давление насыщения
- давление насыщения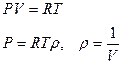 (R, T) = const
(R, T) = const
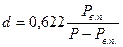 , Р –общее давление смеси.
, Р –общее давление смеси.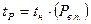
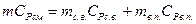 ,
, 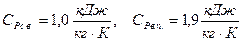
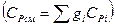 -обладает свойствами аддитивности
-обладает свойствами аддитивности


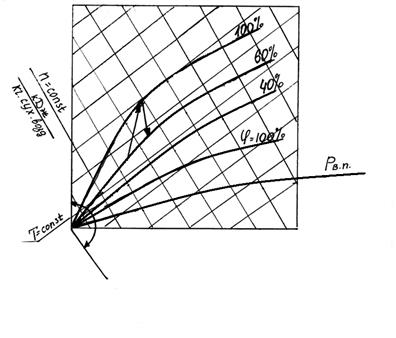

 Если - процесс сопровождается увеличением температуры.
Если - процесс сопровождается увеличением температуры.