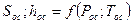Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Классификация теплоемкостей.
1) Количество вещества: - общее количество вещества – полная теплоемкость С, - единица количества вещества – удельная теплоемкость c, 2) единица количества вещества: - 1 кг – массовая c, - 1м3 – объемная с´,
- 1 моль – молярная c =
3) условия проведения процесса. - P = const – изобарная теплоемкость cр, с’р, сμр - V = const - изохорная cv, c’v, cμv
Cp – Cv = R – уравнение Майера
R – газовая постоянная
Физический смысл R: работа, которую надо совершить в изобарном процессе над 1 кг газа, чтобы его температура изменилась на 1К (1˚ С)
Rμ – универсальная газовая постоянная
Для воздуха К = 1,4
4) температурный интервал - ∆t = 0 – истинная теплоемкость Сх, С’х, Сμх (х → P или V) - ∆t ≠ 0 – средняя теплоемкость
Теплоемкость смеси (истинная).
gi – массовая доля
ri – объемная доля
ψi – молярная концентрация.
Законы термодинамики. Техническая термодинамика – это закономерности преобразования теплоты и работы. I закон: невозможно создать вечный двигатель I-го рода.
Для открытой системы:
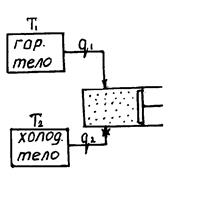
II закон термодинамики: невозможно создать вечный двигатель II-го рода.
Не вся теплота преобразуется в работу, часть ее нужно отвести к холодному источнику, без холодного источника – это вечный двигатель II-го рода.
Форм. Карно: превращение теплоты в работу возможно в двигателях при наличии двух источников теплоты, Т1>Т2, т.е.необходимым условием для получения работы является разность температур.
Форм. Томсона: не вся теплота, полученная от горячего источника, может перейти в работу, а только часть ее, другая часть должна перейти к холодному источнику.
Форм. Клаузиуса: теплота сама собой не может переходить от холодного тела к более нагретому. Форм. Оствальда: невозможно создать вечный двигатель II-го рода, т.е. двигатель без холодного источника.
т.к.
> - для необратимых процессов, = для обратимых
III закон термодинамики (Теория Нернста): невозможно создать вечный двигатель III-го рода.
Вблизи абсолютного нуля температур теплообмен с окружающей средой не происходит, так как изотермический процесс одновременно является адиабатным. Невозможно охладить систему до абсолютного нуля температур путем отвода теплоты. Абсолютный ноль температуры недостижим. Невозможно создать вечный двигатель III-го рода, у которого в качестве холодного источника было бы тело с абсолютным нулем температур, Т = 0 К. В любой термодинамической системе процесс, проведенный при Т = 0 К, сопровождается изменением энтропии равном 0. Эксэргия – работоспособная часть энергии Q = e + a – объединенное выражение для всех законов термодинамики. Анергия – неработоспособная часть энергии. Работа любого вида есть чистая эксэргия.
e – функция состояния второго порядка.
|
|||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 175; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.1.136 (0.015 с.) |
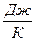
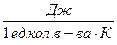
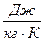
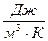
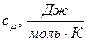
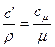 - связь
- связь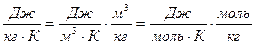


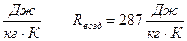
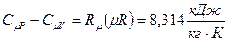
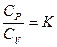 - показатель адиабаты, коэффициент Пуассона, зависит от числа атомов газа.
- показатель адиабаты, коэффициент Пуассона, зависит от числа атомов газа.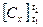 ;
; 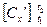 ;
; 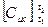
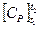 −
− 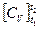 = R
= R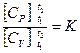
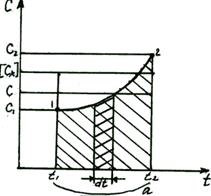

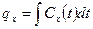

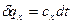
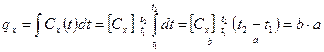

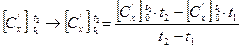
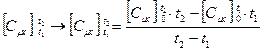
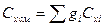
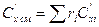
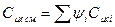
 Q ~ L
Q ~ L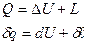
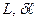 - работа изменения объема.
- работа изменения объема.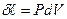


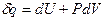 в дифференциальной форме
в дифференциальной форме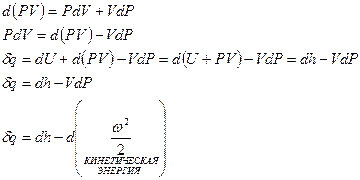
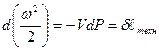 - техническая работа, знак “-“ говорит о том, что эта работа прикладывается к макротелу, расположенному в точке.
- техническая работа, знак “-“ говорит о том, что эта работа прикладывается к макротелу, расположенному в точке.
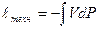
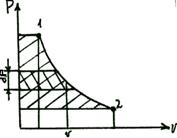

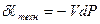
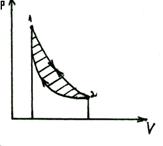
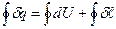 , рассматривается идеальный газ.
, рассматривается идеальный газ.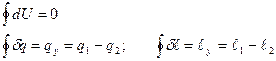
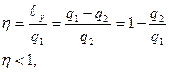
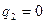

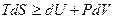
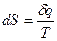
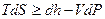 - для открытой системы
- для открытой системы
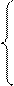
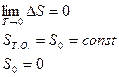
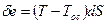
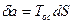
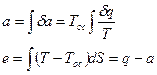
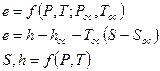 ос – окружающая среда.
ос – окружающая среда.