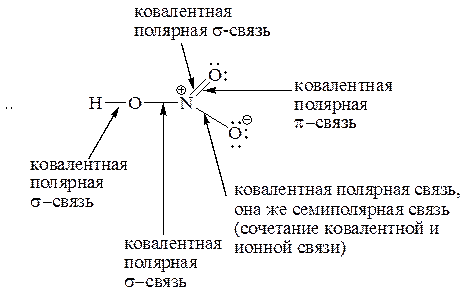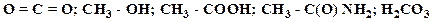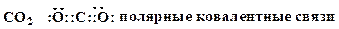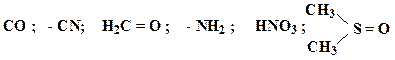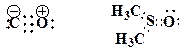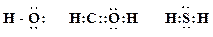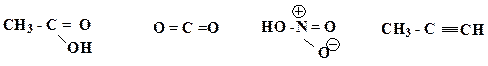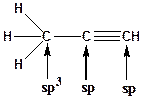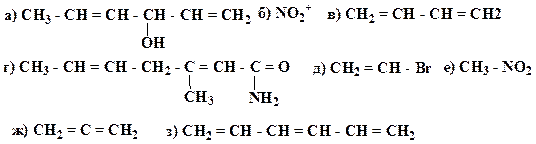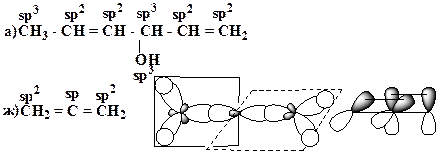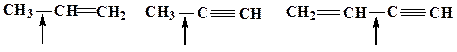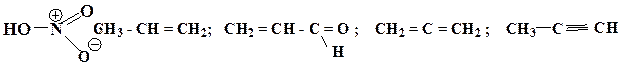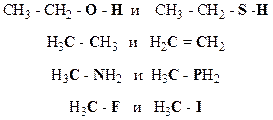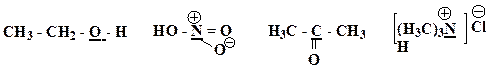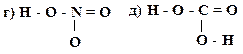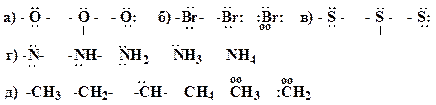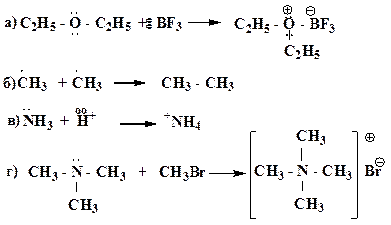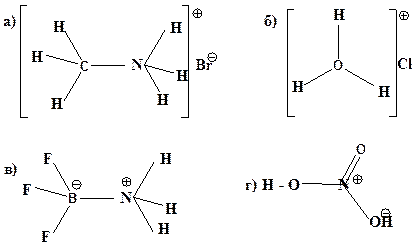Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Глава 1. Теоретические основы органической химии
Электронное строение органических соединений и реакционных частиц Задачи 1. Приведите электронные конфигурации атомов элементов второго периода. Определите значение высшей валентности каждого элемента.
2. Дайте определения следующим понятиям: атом, катион, анион, радикал. Приведите примеры.
3. Укажите внешние электроны в следующих частицах: а) H, H +, H -; б) Br, Br +, Br -; в) CH 3, CH 3 +, CH 3 -; г) OH, OH +, OH - Назовите эти частицы.
4. Охарактеризуйте типы химических связей в приведенных соединениях (ковалентная неполярная, ковалентная полярная, ионная): F2, CH4, NaI, HCl, H2O, NaNH2 KF, CH3CN.
Образец выполнения задания: 5. Охарактеризуйте типы химических связей (обычная ковалентная, координационная, семиполярная) в приведенных соединениях: H3C – Br, HNO3, CO, NH4Cl, H3C – CH3, C2H5ONa, NH3. Образец выполнения задания:
6. Представьте следующие молекулы в виде структур Льюиса, укажите типы химических связей:
Образец выполнения задания:
7. Представьте следующие молекулы в виде структур Льюиса и поставьте, где необходимо, формальные заряды на атомах, укажите типы химической связи:
Образец выполнения задания:
8. Дополните указанные формулы соединений неподеленными электронными парами (НЭП), выберите заряженные частицы, проставьте заряды: BH3; CH3; H3O; NH3; NH4; CH4; NH2; H2O, CH3NH2, CH3OH, CH3OCH3, CH3SCH3, CH3C(O)OC(O)CH3, [CH3OH2]Cl.
9. Какие из приведенных пар соединений являются изоэлектронными: а) CH 3 + и BH 3; б) NH 3 и H 3 O +; в) CH 4 и H 2 O
10. Выберите соединения, в молекулах или ионах которых валентность центрального атома равна четырем: CH 4; NH 4 +; H 2 O; CH 3 +
11. Выберите соединения, в молекулах или ионах которых валентность центрального атома равна трем: CH 4; NH 3; H 3 O +; CH 3 +; CH 3 -; BF 3; NH 4 +
12. Выберите соединения, в молекулах или ионах которых координационное число центрального атома равно трем: CH 4; NH 3; H 3 O +; CH 3 +; CH 3 -; BF 3; NH 4 +
13. Представьте следующие молекулы в виде структур Льюиса и объясните, почему они изоэлектронны: N 2, CO, CN -.
14. Докажите, что приведенные структуры изоэлектронны: а) CO 3 2- и NO 3 -; б) CO 2 и NO 2 +; в) CO и N 2.
15. В приведенных рядах соединений выберите изоэлектронные структуры, напишите для них формулы Льюиса:
1) NO+, NO, CO2, CN- 2) N2, NO+, CO, CN-, NO, NH2- 3) CH4, NH4+, BH4- 4) CO2, HNO2, NO2+, N2, CN
16. Какие из перечисленных структур являются ионами:
17. Для приведенных молекул укажите тип гибридизации каждого атома:
Образец выполнения задания:
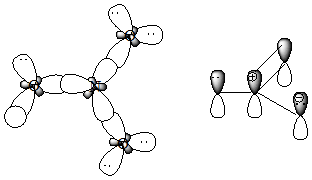
18. Для приведенных молекул и частиц укажите тип гибридизации каждого атома, используя правило октета, проставьте все неподеленные электронные пары и укажите орбитали, на которых они находятся:
Приведите схемы s- и p-связей. Образец выполнения задания:
19. Определите длину одинарных (σ-) связей в приведенных соединениях с учетом ковалентных радиусов атома углерода (RСsp3 = 0.767 Ǻ, RCsp2 = 0.742 Ǻ, RCsp = 0.668 Ǻ):
20. Из каждой пары веществ выберите такие, в молекулах которых выделенная связь имеет большую длину: а) CH 3 - CH 3 или CH 2 = CH 2; б) > C = O или CH 3 – OH; в) HC º CH или CH 3 - Cl.
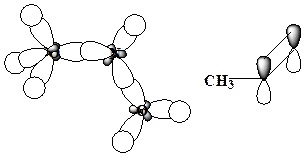
21. Приведите схемы σ- и π- связей для молекул следующих соединений, укажите орбитальные углы:
Образец выполнения задания: Схема s – и π-связей для молекулы азотной кислоты: Схема σ- и p -связей для молекулы пропена: 109 ° 28 ¢ и 120 °
22. Какая из связей в каждой паре более полярна, какая более поляризуема: а) C – C и C º C; б) C – Cl и С - I; в) C - N и C º N; г) C - O и C = O; д) C - S и C - O; е) C - O и C - F; ж) C - F и C - Br; з) C = N и C º N; и) C = C и C º C
23. Сопоставьте полярность и поляризуемость выделенных связей в следующих парах соединений:
(Указание: воспользуйтесь данными табл.10 в Приложении).
24. Определите ковалентность и координационное число для выделенных атомов в следующих соединениях:
25. Рассчитайте формальные заряды на выделенных атомах: а)[ CH 3 – OH 2 ] Br; б) [ NH 4 ] Cl; в) [ CH 3 – C º C:] K;
26. Рассчитайте формальные заряды в следующих фрагментах молекул:
27. Приведите конкретные примеры для каждого случая образования ковалентной связи по донорно-акцепторной схеме: A: + B+ → A+ - B A:- + B+ → A - B A:- + B → A – B- A:- + B + → A – B
28. Какие способы обобщения электронной пары реализуются при образовании приведенных соединений:
29. В каком случае донорно-акцепторное взаимодействие приводит к образованию семиполярной связи? В чем ее отличие от ионной и ковалентной? В каких из приведенных соединений имеются семиполярные связи?
|
||||||
|
Последнее изменение этой страницы: 2020-11-11; просмотров: 388; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.175.182 (0.011 с.) |
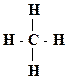 четыре C – Н связи, все ковалентные неполярные.
четыре C – Н связи, все ковалентные неполярные.